Clear Sky Science · nl
SMC-LUD: Groot-schalige B-Mode leverultrasounddataset voor classificatie van hepatocellulair carcinoom en hemangioom
Waarom dit van belang is voor dagelijkse gezondheid
Leverkanker behoort tot de dodelijkste vormen van kanker ter wereld, deels omdat het lastig is om de ziekte vroeg genoeg en nauwkeurig genoeg te detecteren voor effectieve behandeling. Artsen vertrouwen vaak op echografie, een snelle en betaalbare scan, om verdachte plekken in de lever op te sporen. Maar op deze korrelige zwart-witbeelden kunnen gevaarlijke tumoren en goedaardige gezwellen er verwarrend gelijkend uitzien, zelfs voor experts. Dit artikel introduceert een grote nieuwe beeldverzameling die bedoeld is om computers te helpen het verschil te leren zien, wat leveronderzoeken mogelijk nauwkeuriger en breder beschikbaar kan maken.
Een nadere blik op levervlekken
Twee veelvoorkomende bevindingen op leverscans bevinden zich aan tegenovergestelde uiteinden van het risicospectrum. Hepatocellulair carcinoom is een primaire leverkanker die levensbedreigend kan zijn als deze gemist of laat ontdekt wordt. Hemangiomen daarentegen zijn meestal onschuldige clusters van bloedvaten die zelden behandeling vereisen. Op eenvoudige echobeelden zijn deze twee echter vaak moeilijk te onderscheiden, vooral wanneer het leverweefsel al beschadigd is of wanneer de plekken klein zijn. Tegenwoordig moeten artsen vaak aanvullende onderzoeken zoals CT- of MRI-scans aanvragen om zekerheid te krijgen, wat extra kosten, tijd en blootstelling aan straling of contrastmiddelen met zich meebrengt.
Het opbouwen van een grote bibliotheek met leverbeelden
Om dit probleem aan te pakken stelde een onderzoeksteam van het Samsung Medical Center in Seoul SMC-LUD samen, een nieuwe openbare verzameling van 5.385 leverechografiebeelden van 1.021 echte patiënten gescand tussen 2015 en 2024. Elk beeld toont een leverlaesie die zorgvuldig is geclassificeerd in één van twee groepen: kanker (hepatocellulair carcinoom, 2.716 beelden) of goedaardig hemangioom (2.669 beelden). Kankergevallen werden bevestigd door weefsel te onderzoeken dat tijdens chirurgie of biopsie was verwijderd, terwijl hemangiomen werden gediagnosticeerd met behulp van karakteristieke scankenmerken geïnterpreteerd door ervaren radiologen. Alle beelden werden geanonimiseerd, per patiënt gegroepeerd en door specialisten dubbel gecontroleerd om betrouwbare labels te waarborgen. 
De data voorbereiden voor slimme algoritmen
Het team organiseerde de dataset zodanig dat deze eenvoudig door onderzoekers op het gebied van kunstmatige intelligentie te gebruiken is. Beelden werden aangepast in grootte en gestandaardiseerd zodat computermodellen ze in een consistent formaat te zien krijgen, en de data werden opgesplitst in afzonderlijke groepen voor training, fine-tuning en definitieve toetsing, waarbij er zorgvuldig op werd toegezien dat beelden van dezelfde patiënt nooit in meer dan één groep voorkomen. De dataset is ook in twee varianten beschikbaar: een "Clean" versie zonder meetmarkeringen en een "Caliper" versie die deze markeringen wel bevat. Voor eerlijke toetsing trainden de onderzoekers hun modellen alleen op de Clean-beelden om te voorkomen dat algoritmen zouden 'valsspelen' door markeringspatronen te associëren met bepaalde diagnoses in plaats van zich op de laesies zelf te concentreren. Een aanvullende tabel met patiëntinformatie, zoals tumorgrootte en stadium voor kankergevallen, maakt diepgaandere klinische analyses mogelijk.
Hoe de computer leert zien
Om te demonstreren wat met deze bron mogelijk is bouwden de auteurs een deep learning-model gebaseerd op een bekend beeldherkenningskader en versterkten dit met speciale "attention"-modules. Deze componenten helpen het netwerk te focussen op de meest informatieve delen van het beeld en de meest veelzeggende patronen van helderheid en textuur. Het ontwerp gebruikt twee parallelle takken die dezelfde kenmerken op net iets andere manieren verwerken voordat ze weer samenkomen en vervolgens een ruimtelijke filter toepassen die belangrijke regio's benadrukt, vergelijkbaar met hoe een radioloog mentaal inzoomt op een verdachte plek. Getraind op de SMC-LUD Clean-subset werd dit model vergeleken met verschillende populaire neurale netwerkontwerpen voor medische beeldvorming. 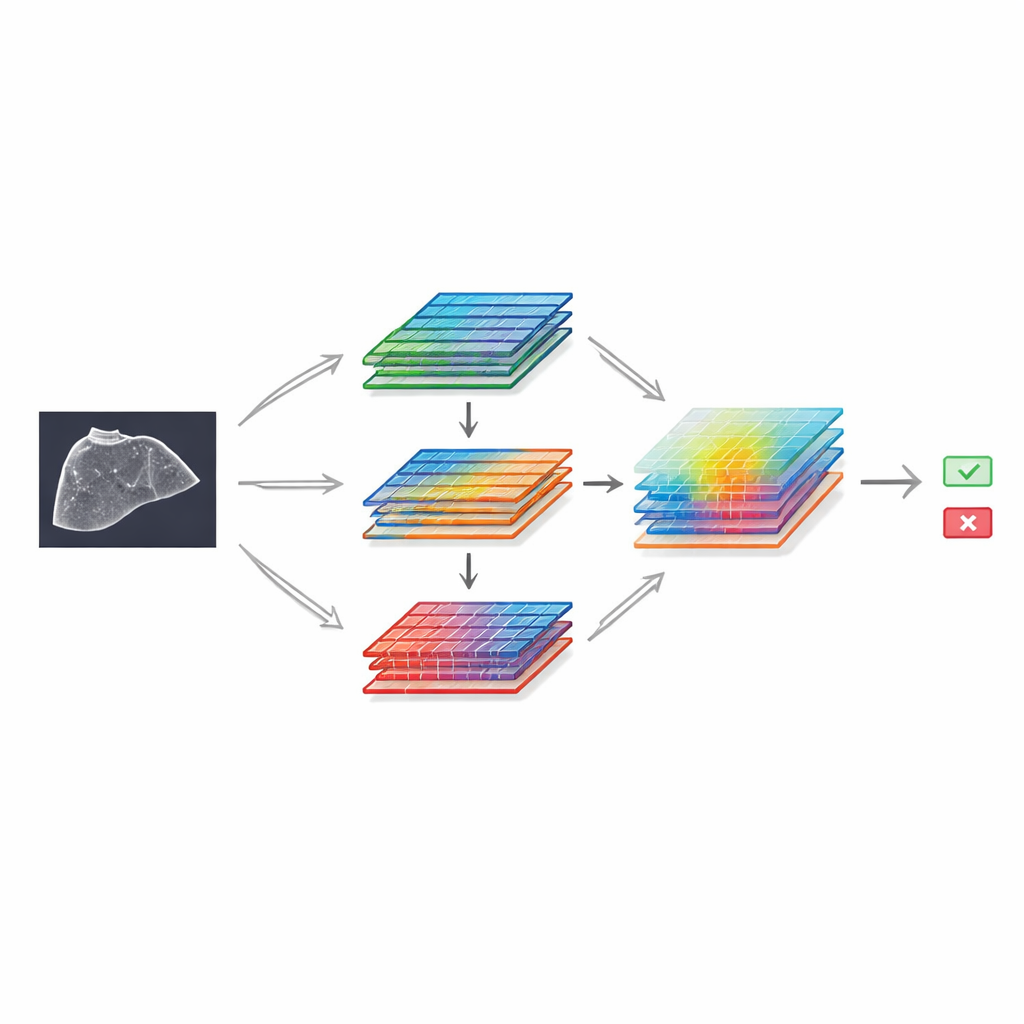
Wat de resultaten laten zien
Op de apart gehouden testbeelden wist het met attention verrijkte model bijna 99% van de tijd correct het verschil te maken tussen leverkanker en hemangioom, en overtrof het daarmee de vergelijkingsmodellen. Heatmaps afgeleid van de interne berekeningen van het netwerk toonden aan dat het de neiging had zich op de laesies zelf te richten in plaats van op niet-gerelateerde beelddetails, wat erop wijst dat het medisch relevante signalen leerde. Hoewel deze studie slechts een tweedelige onderscheidingen tussen één malign en één benign type laesie evalueert, benadrukt de prestatie zowel de kwaliteit van de beeldlabels als het potentieel van echografie-gebaseerde computergestuurde diagnose wanneer die wordt gevoed met voldoende grote, goed georganiseerde data.
Wat dit voor patiënten kan betekenen
Voor niet-specialisten is de kernboodschap dat deze dataset op zichzelf niet verandert hoe uw arts uw volgende scan zal beoordelen — maar hij legt belangrijk fundament. Door vrijelijk een grote, zorgvuldig geverifieerde bibliotheek van echobeelden te delen, bieden de auteurs onderzoekers wereldwijd het ruwe materiaal dat nodig is om slimmere hulpmiddelen voor leveronderzoek te trainen en te testen. In de toekomst zouden dergelijke hulpmiddelen als een tweede paar ogen kunnen dienen, door zorgwekkende plekken te markeren die nader onderzoek verdienen en onnodige vervolgonderzoeken bij duidelijke goedaardige bevindingen te verminderen. Uiteindelijk kan dit helpen leverkankerdiagnose naar eerdere, beter behandelbare stadia te verschuiven, terwijl kosten en complexiteit beperkt blijven.
Bronvermelding: Tak, J., Ko, RE., Kwon, R.D. et al. SMC-LUD:Large-Scale B-Mode Liver Ultrasound Dataset for Hepatocellular Carcinoma and Hemangioma Classification. Sci Data 13, 649 (2026). https://doi.org/10.1038/s41597-026-07023-7
Trefwoorden: leverultrasound, hepatocellulair carcinoom, hemangioom, deep learning, medische beeldvorming dataset