Clear Sky Science · de
SMC-LUD: Groß angelegtes B‑Mode-Leber-Ultraschall‑Datenset zur Klassifikation von hepatozellulärem Karzinom und Hämangiom
Warum das für die alltägliche Gesundheit wichtig ist
Leberkrebs gehört zu den tödlichsten Krebserkrankungen weltweit, teilweise weil er schwer früh genug zu erkennen und zu klassifizieren ist, um wirksam behandelt werden zu können. Ärztinnen und Ärzte verlassen sich oft auf Ultraschall, eine schnelle und kostengünstige Untersuchung, um nach auffälligen Stellen in der Leber zu suchen. Auf diesen körnigen Schwarz-Weiß-Aufnahmen können jedoch gefährliche Tumoren und harmlose Wucherungen selbst für Expertinnen und Experten verwirrend ähnlich aussehen. Dieser Artikel stellt eine neue, umfangreiche Bildsammlung vor, die Computern helfen soll, die Unterschiede zu lernen, wodurch Leberuntersuchungen möglicherweise genauer und breiter verfügbar werden können.
Ein genauerer Blick auf Leberherde
Zwei häufige Befunde in Leberuntersuchungen liegen am jeweils entgegengesetzten Ende des Risikospektrums. Das hepatozelluläre Karzinom ist ein primärer Leberkrebs, der lebensbedrohlich sein kann, wenn er übersehen oder spät entdeckt wird. Hämangiome dagegen sind in der Regel harmlose Ansammlungen von Blutgefäßen, die selten einer Behandlung bedürfen. Auf einfachen Ultraschallbildern sind diese beiden jedoch schwer zu unterscheiden, insbesondere wenn das Lebergewebe bereits geschädigt ist oder die Herde klein sind. Heute müssen Ärztinnen und Ärzte oft zusätzliche Untersuchungen wie CT- oder MRT-Scans anordnen, um sicher zu sein, was zusätzliche Kosten, Zeitaufwand sowie Strahlen- oder Kontrastmittelbelastung mit sich bringt.
Aufbau einer großen Bibliothek von Leberbildern
Um dieses Problem anzugehen, haben Forschende des Samsung Medical Center in Seoul SMC-LUD zusammengestellt, eine neue öffentliche Sammlung von 5.385 Leber‑Ultraschallbildern von 1.021 realen Patientinnen und Patienten, die zwischen 2015 und 2024 untersucht wurden. Jedes Bild zeigt eine Leberläsion, die sorgfältig einer von zwei Gruppen zugeordnet wurde: Krebs (hepatozelluläres Karzinom, 2.716 Bilder) oder gutartiges Hämangiom (2.669 Bilder). Krebserkrankungen wurden durch Untersuchung von während einer Operation oder Biopsie entnommenem Gewebe bestätigt, während Hämangiome anhand charakteristischer Bildmerkmale von erfahrenen Radiologinnen und Radiologen diagnostiziert wurden. Alle Bilder wurden anonymisiert, nach Patient sortiert und von Spezialistinnen und Spezialisten doppelt geprüft, um verlässliche Labels zu gewährleisten. 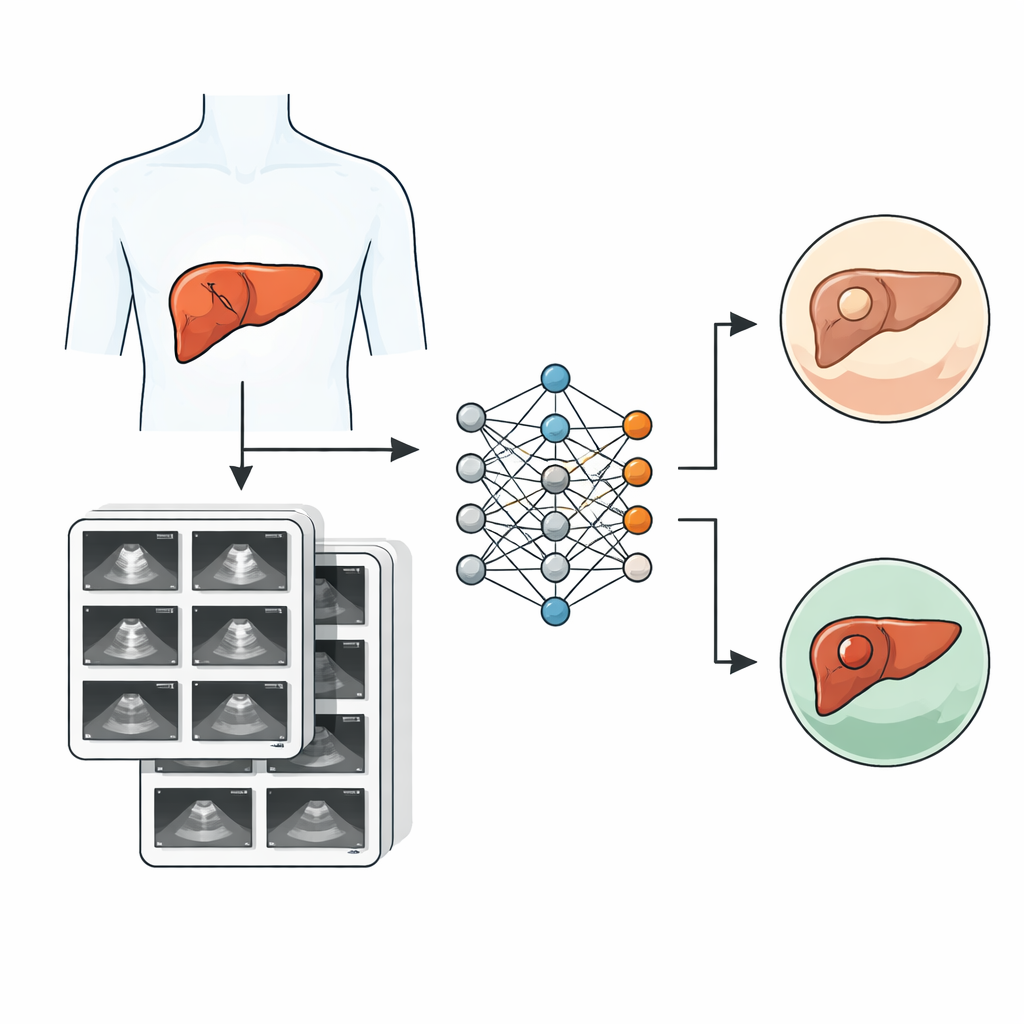
Aufbereitung der Daten für intelligente Algorithmen
Das Team organisierte den Datensatz so, dass er für Forschende im Bereich künstliche Intelligenz leicht nutzbar ist. Bilder wurden skaliert und standardisiert, sodass Modelle sie in einem konsistenten Format sehen, und die Daten wurden in getrennte Gruppen für Training, Feinabstimmung und abschließende Tests aufgeteilt, wobei darauf geachtet wurde, dass Bilder desselben Patienten nie in mehr als einer Gruppe erscheinen. Der Datensatz liegt außerdem in zwei Varianten vor: einer „Clean“-Version ohne Messmarkierungen und einer „Caliper“-Version, die solche Markierungen enthält. Für faire Tests trainierten die Forschenden ihre Modelle ausschließlich mit den Clean‑Bildern, um zu vermeiden, dass Algorithmen durch das Erlernen von Marker‑Mustern diagnostische Abkürzungen nehmen, anstatt sich auf die Läsionen selbst zu konzentrieren. Eine begleitende Tabelle mit Patientendaten, etwa Tumorgröße und Stadium bei Krebserkrankungen, ermöglicht tiefere klinische Analysen.
Wie der Computer das Sehen lernt
Um zu zeigen, was mit dieser Ressource möglich ist, bauten die Autorinnen und Autoren ein Deep‑Learning‑Modell auf der Basis eines bekannten Bilderkennungs‑Frameworks und erweiterten es mit speziellen „Attention“-Modulen. Diese Komponenten helfen dem Netzwerk, sich auf die informativsten Bildbereiche und die aussagekräftigsten Helligkeits‑ und Texturmuster zu konzentrieren. Das Design nutzt zwei parallele Zweige, die dieselben Merkmale leicht unterschiedlich verarbeiten, bevor sie wieder zusammengeführt werden, und wendet dann einen räumlichen Filter an, der wichtige Regionen hervorhebt, ähnlich wie eine Radiologin oder ein Radiologe gedanklich in einen verdächtigen Bereich hineinzoomt. Auf dem Clean‑Subset von SMC‑LUD trainiert, wurde dieses Modell mit mehreren verbreiteten neuronalen Netzarchitekturen für die medizinische Bildverarbeitung verglichen. 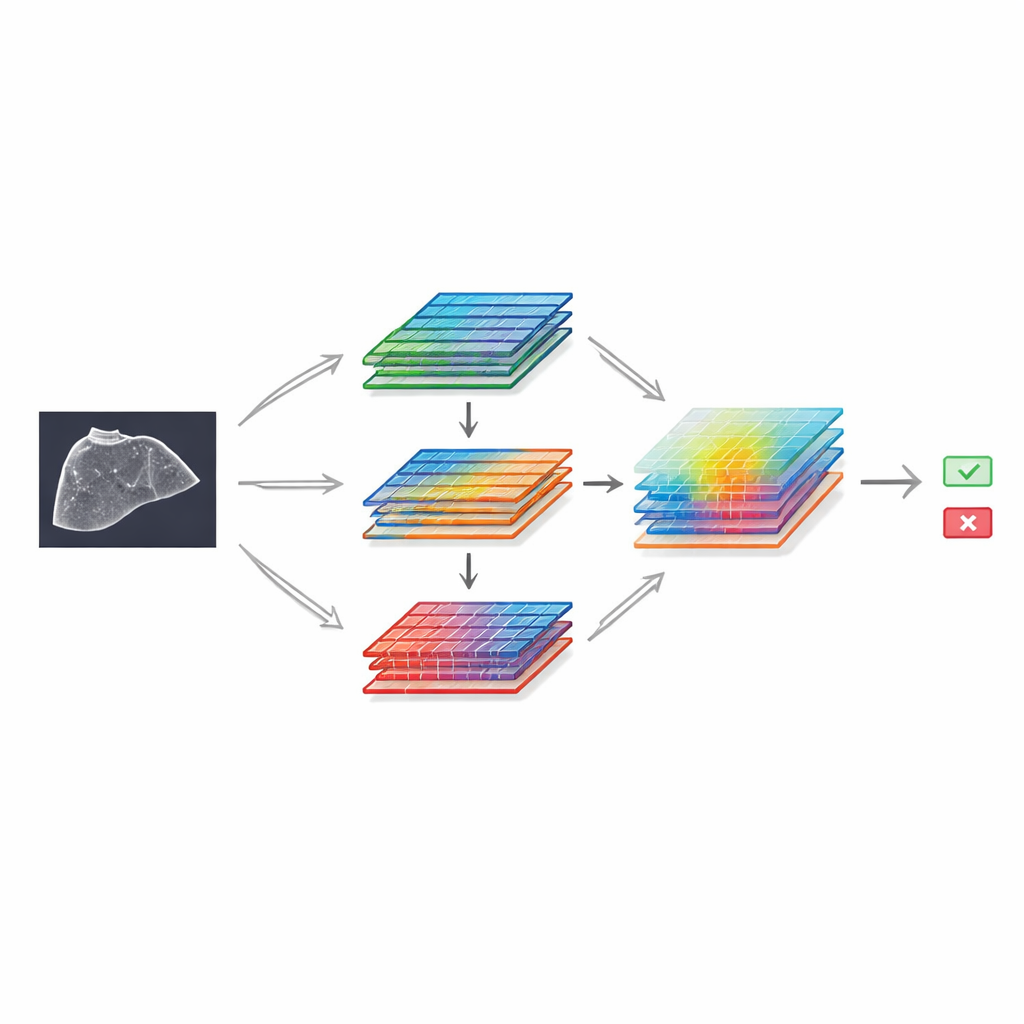
Was die Ergebnisse zeigen
Bei den zurückgehaltenen Testbildern unterschied das mit Attention erweiterte Modell Krebs und Hämangiom in fast 99 % der Fälle korrekt und übertraf die Vergleichsmodelle. Heatmaps, die aus den internen Berechnungen des Netzwerks abgeleitet wurden, zeigten, dass es dazu neigte, sich auf die Läsionen selbst statt auf unbeteiligte Bilddetails zu konzentrieren, was darauf hindeutet, dass es medizinisch sinnvolle Hinweise lernte. Obwohl diese Studie nur eine Zweiweg‑Unterscheidung zwischen einer malignen und einer benignen Läsionsart bewertet, unterstreicht ihre Leistung sowohl die Qualität der Bildlabels als auch das Potenzial ultraschallbasierter Computerdiagnostik, wenn ausreichend große und gut organisierte Daten bereitgestellt werden.
Was das für Patientinnen und Patienten bedeuten könnte
Für Nicht‑Spezialisten ist die Hauptbotschaft, dass dieser Datensatz für sich genommen nicht ändert, wie Ihre Ärztin oder Ihr Arzt Ihre nächste Untersuchung interpretiert – er schafft jedoch wichtige Grundlagen. Durch das freie Teilen einer großen, sorgfältig verifizierten Bibliothek von Ultraschallbildern bieten die Autorinnen und Autoren Forschenden weltweit das Rohmaterial, das nötig ist, um intelligentere Werkzeuge für die Leber‑Screenings zu trainieren und zu testen. In Zukunft könnten solche Werkzeuge als zweite Sicht fungieren, auffällige Stellen markieren, die einer genaueren Betrachtung bedürfen, und unnötige Nachuntersuchungen bei eindeutig benignen Befunden reduzieren. Letztlich könnte dies dazu beitragen, die Diagnose von Leberkrebs früher und damit besser behandelbar zu stellen, bei gleichzeitiger Begrenzung von Kosten und Komplexität.
Zitation: Tak, J., Ko, RE., Kwon, R.D. et al. SMC-LUD:Large-Scale B-Mode Liver Ultrasound Dataset for Hepatocellular Carcinoma and Hemangioma Classification. Sci Data 13, 649 (2026). https://doi.org/10.1038/s41597-026-07023-7
Schlüsselwörter: Leberultraschall, hepatozelluläres Karzinom, Hämangiom, Deep Learning, medizinischer Bilddatensatz