Clear Sky Science · zh
趋化因子界定的巨噬细胞微环境建立了肿瘤免疫的空间组织
肿瘤内部“街区”如何塑造免疫之争
为何有些肿瘤能被控制,而有些即便有大量免疫细胞仍失控生长?这项研究在极高分辨率下审视肺肿瘤,发现并非所有免疫细胞都相同。特别是,不同群体的巨噬细胞——既负责清理又负责协调的免疫细胞——建立了截然不同的“街区”,这些街区要么帮助机体抗癌,要么在暗中助长肿瘤。理解这种内在的“好坏免疫区”地图,可能为更聪明的癌症治疗和更有效的疫苗指明方向。
肿瘤巨噬细胞的两面性
巨噬细胞常被视为单一细胞类型,但在肺中它们属于数个驻留与迁入的群体。作者关注了组织间隙巨噬细胞——生活在气囊与血管之间的细胞——以及疾病发生时自血液招募而来的巨噬细胞。利用单细胞基因表达谱,他们显示驻留的间隙巨噬细胞分化为两大阵营。一类位于气道与血管附近,表现出与免疫支持相关的分子谱,并携带已知能吸引有益淋巴细胞的信号。另一类与迁入的巨噬细胞一道,位于肿瘤核心内部,携带更多与肿瘤生长和抑制免疫攻击相关的基因程序。
在三维空间绘制免疫景观
为了确定这些细胞在肿瘤内部的实际位置,研究者将单细胞数据与空间转录组学结合——一种直接在组织切片中描绘基因活性的成像方法。他们发现,具有保护性的驻留巨噬细胞排列在支气管和血管区域,产生能招募T细胞和B细胞的趋化因子,促进形成称为第三淋巴结构的小型、有组织的免疫枢纽。 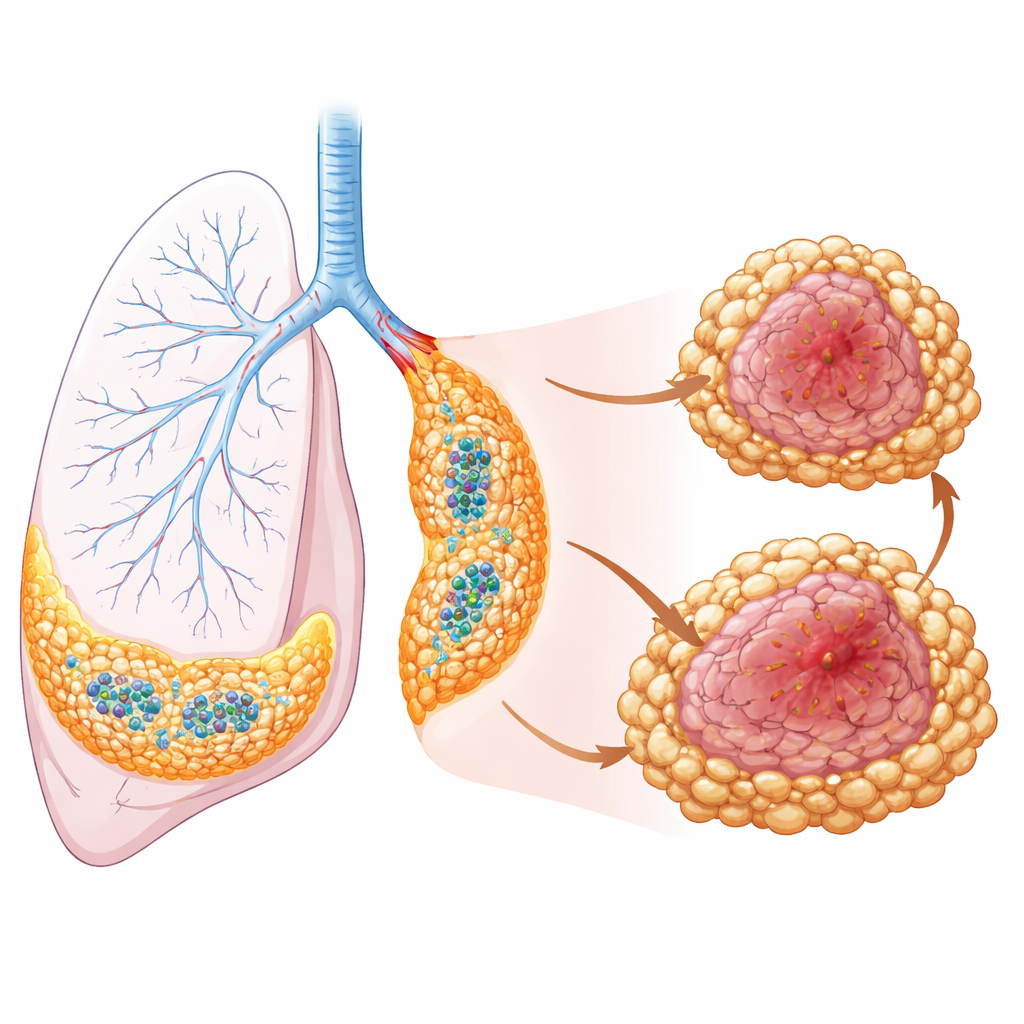
促肿瘤信号与防守信号
通过在黑色素瘤和肺腺癌小鼠模型中选择性去除保护性的驻留巨噬细胞,研究团队观察到肿瘤生长加速且第三淋巴结构消失。吸引淋巴细胞的关键趋化因子在肺中的水平下降,肿瘤邻近的T细胞和B细胞也减少。另一方面,主要由间隙巨噬细胞产生的趋化因子CCL2,对从血液招募巨噬细胞至关重要。当研究者仅从骨髓来源的免疫细胞,或更具体地从短寿命髓系细胞中去除CCL2产生,同时保留长寿命的驻留巨噬细胞时,进入肺部的迁入巨噬细胞减少,肿瘤生长明显受抑。这些实验表明,巨噬细胞来源的CCL2作为一条不可替代的“燃料线”,用于招募支持肿瘤的细胞。
迁徙细胞如何压制疫苗反应
故事并不止于肿瘤内部。一部分迁入的巨噬细胞会分化为单核细胞来源的树突状细胞,将肿瘤物质带到附近的淋巴结,免疫反应在那儿被启动。令人意外的是,在这种情境中,这些迁徙细胞更像是刹车而非加速器。研究团队发现,这些细胞依赖另一种归巢信号CCR5到达淋巴结。在仅使单核细胞来源细胞缺失CCR5的小鼠中,黑色素瘤和肺癌的生长都减少了。 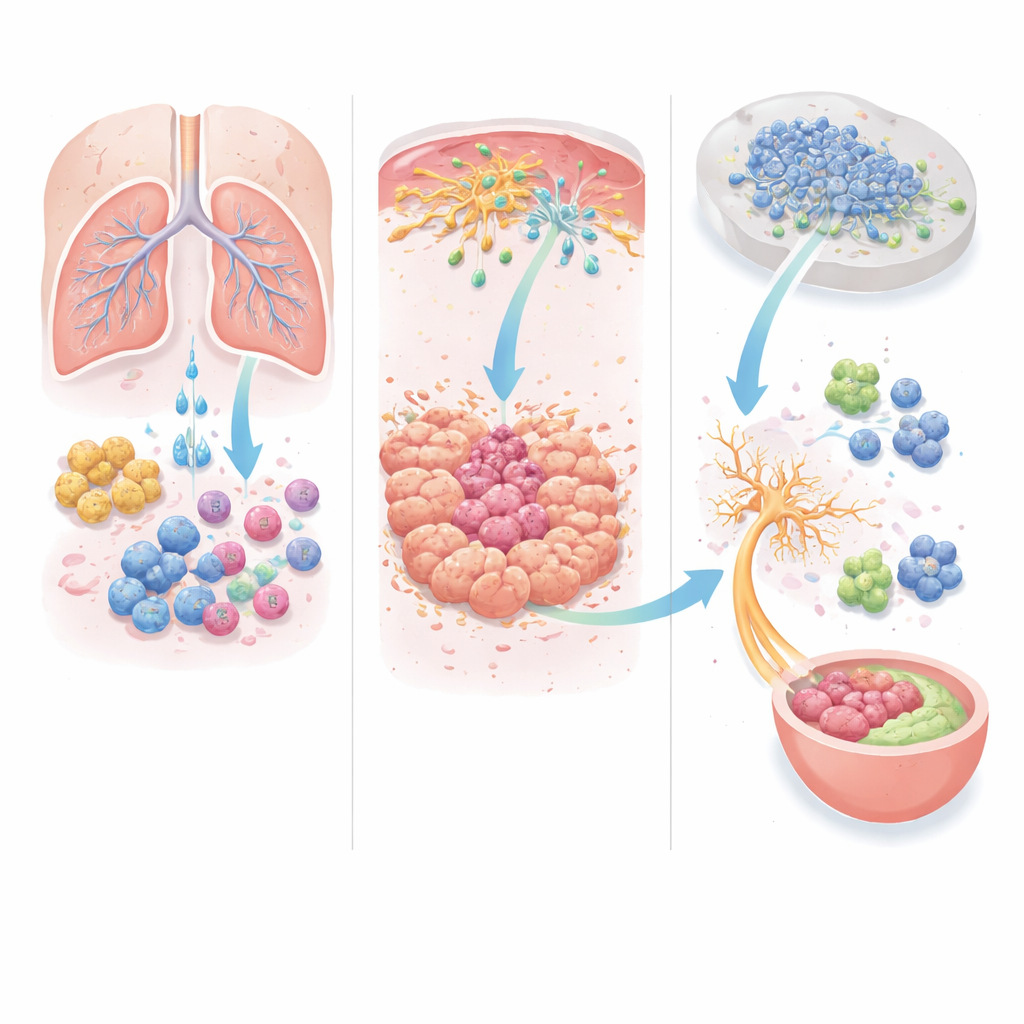
对未来癌症治疗的意义
这项工作表明,巨噬细胞在肺内的空间位置以及它们释放的化学信号,很大程度上决定了它们是助力还是阻碍肿瘤控制。沿气道和血管的驻留巨噬细胞建立了有利于肿瘤清除的免疫富集街区,而位于肿瘤核心及周围的其他巨噬细胞则形成由趋化因子界定的区域,招募抑制性细胞并助长肿瘤生长。研究结果提示,有效的免疫治疗需要比简单地“增强”或“阻断”整体巨噬细胞更精准。未来策略可能旨在保护甚至扩展这些具有保护性的驻留巨噬细胞微环境,同时切断关键通路——例如由CCL2驱动的招募通路和依赖CCR5的迁移——以防止抑制性单核细胞来源细胞在肿瘤环境及邻近淋巴结中占主导地位。
引用: Ghosh, S., Li, X., Rawat, K. et al. Chemokine-defined macrophage niches establish spatial organization of tumor immunity. Nat Immunol 27, 715–724 (2026). https://doi.org/10.1038/s41590-026-02445-2
关键词: 肿瘤微环境, 肺癌免疫, 巨噬细胞微环境, 趋化因子, 癌症免疫治疗