Clear Sky Science · pt
Nichos de macrófagos definidos por quimiocinas estabelecem a organização espacial da imunidade tumoral
Como os bairros dentro dos tumores moldam a batalha imune
Por que alguns tumores permanecem sob controle enquanto outros crescem sem freio, mesmo quando contêm muitas células imunes? Este estudo examina tumores pulmonares em escala muito fina e mostra que nem todas as células imunes são iguais. Em particular, diferentes grupos de macrófagos — células do sistema imune que atuam tanto como limpadoras quanto como coordenadoras — estabelecem “bairros” distintos que podem tanto ajudar o organismo a combater o câncer quanto, silenciosamente, favorecer o crescimento tumoral. Compreender esse mapa interno de zonas imunes benéficas e prejudiciais pode apontar caminhos para terapias contra o câncer mais inteligentes e vacinas mais eficazes.
Duas faces dos macrófagos tumorais
Os macrófagos costumam ser agrupados como um único tipo de célula, mas no pulmão eles se dividem em vários grupos residentes e recrutados. Os autores se concentraram nos macrófagos intersticiais, que vivem no tecido entre os alvéolos e os vasos sanguíneos, e nos macrófagos recrutados que chegam pela corrente sanguínea durante a doença. Usando perfilamento gênico de célula única, mostraram que os macrófagos intersticiais residentes se separam em dois campos principais. Um grupo, encontrado perto das vias aéreas e dos vasos, exibiu um perfil molecular ligado ao suporte imune e produziu sinais conhecidos por atrair linfócitos úteis. O outro grupo, junto com os macrófagos recrutados que ficam no interior dos núcleos tumorais, apresentou programas gênicos mais associados ao crescimento tumoral e à supressão do ataque imune.
Mapeando a paisagem imune no espaço 3D
Para ver onde essas células estão de fato dentro dos tumores, os pesquisadores combinaram seus dados de célula única com transcriptômica espacial — uma abordagem de imagem que mapeia a atividade gênica diretamente em cortes de tecido. Eles descobriram que macrófagos residentes protetores alinham-se nas regiões brônquicas e vasculares e produzem quimiocinas que atraem células T e B, incentivando a formação de pequenos centros imunes organizados chamados estruturas linfoides terciárias. 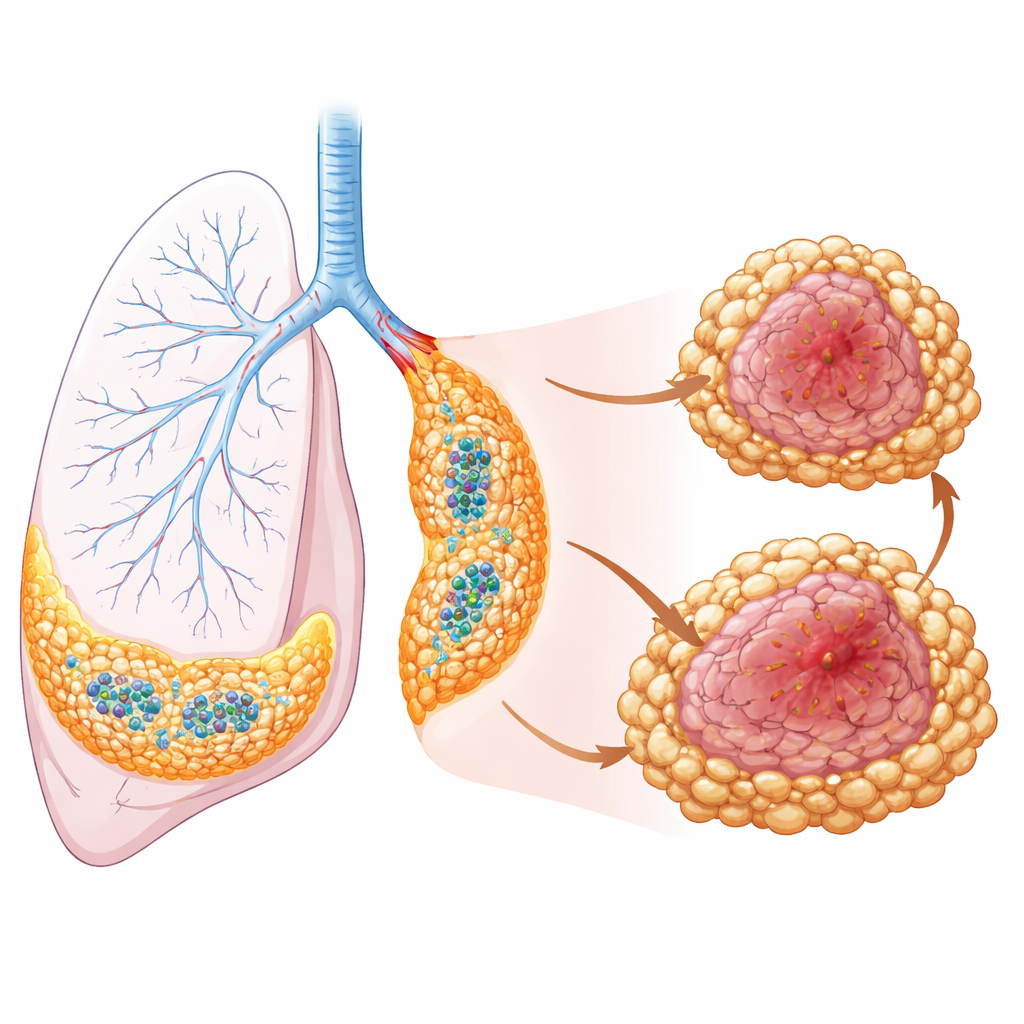
Sinais que alimentam tumores versus sinais que os protegem
Ao remover seletivamente os macrófagos residentes protetores em modelos murinos de melanoma e adenocarcinoma de pulmão, a equipe observou crescimento tumoral mais rápido e desaparecimento das estruturas linfoides terciárias. Os níveis de quimiocinas-chave que atraem linfócitos caíram nos pulmões, e menos células T e B se acumularam perto dos tumores. Por outro lado, a quimiocina CCL2, produzida principalmente por macrófagos intersticiais, mostrou-se crítica para atrair macrófagos recrutados do sangue. Quando os pesquisadores eliminaram a produção de CCL2 apenas de células imunes derivadas da medula óssea, ou mais especificamente de células mieloides de curta duração preservando os macrófagos residentes de longa vida, menos macrófagos recrutados entraram nos pulmões e o crescimento tumoral foi drasticamente reduzido. Esses experimentos demonstraram que a CCL2 derivada de macrófagos atua como uma linha de combustível não redundante para trazer células que suportam o tumor.
Como células em trânsito silenciam respostas vacinais
A história não termina dentro do tumor. Alguns dos macrófagos entrantes se transformam em células dendríticas derivadas de monócitos que carregam material tumoral para linfonodos próximos, onde as respostas imunes são iniciadas. Surpreendentemente, nesse contexto esses viajantes agem mais como freios do que como aceleradores. A equipe descobriu que essas células dependem de um sinal de homing diferente, CCR5, para alcançar os linfonodos. Em camundongos geneticamente modificados de modo que apenas as células derivadas de monócitos não tivessem CCR5, tanto o melanoma quanto o câncer de pulmão cresceram menos. 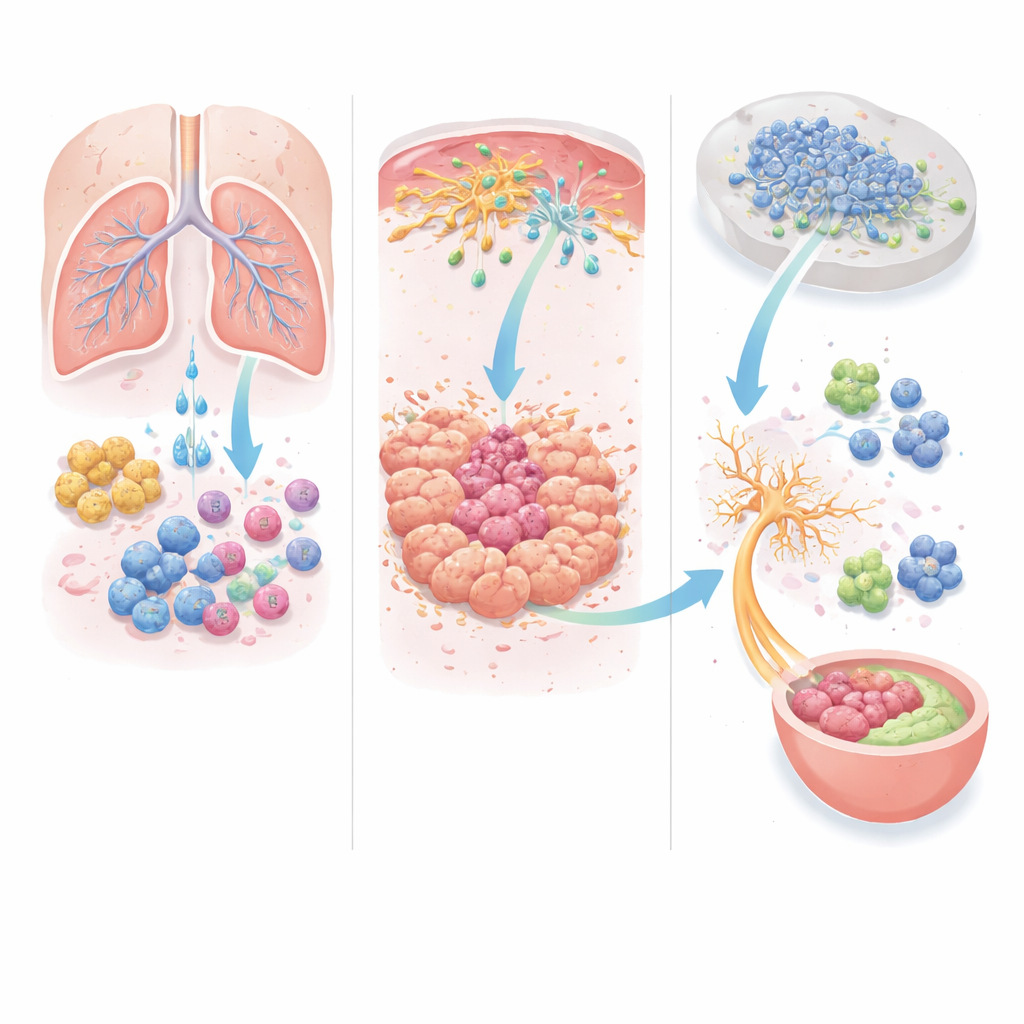
O que isso significa para tratamentos futuros do câncer
Este trabalho mostra que onde os macrófagos vivem dentro do pulmão e quais sinais químicos eles emitem determinam em grande parte se ajudam ou atrapalham o controle tumoral. Macrófagos residentes ao longo das vias aéreas e dos vasos constroem bairros ricos em imunidade que favorecem a rejeição tumoral, enquanto outros macrófagos dentro e ao redor dos núcleos tumorais criam zonas definidas por quimiocinas que recrutam células supressoras e alimentam o crescimento do tumor. As descobertas sugerem que a imunoterapia eficaz precisará ser mais precisa do que simplesmente “estimular” ou “bloquear” os macrófagos como um todo. Em vez disso, estratégias futuras podem visar preservar ou até expandir os nichos de macrófagos residentes protetores, enquanto cortam vias-chave — como o recrutamento dirigido por CCL2 e o tráfego dependente de CCR5 — que permitem que células derivadas de monócitos supressoras dominem o microambiente tumoral e os linfonodos próximos.
Citação: Ghosh, S., Li, X., Rawat, K. et al. Chemokine-defined macrophage niches establish spatial organization of tumor immunity. Nat Immunol 27, 715–724 (2026). https://doi.org/10.1038/s41590-026-02445-2
Palavras-chave: microambiente tumoral, imunidade em câncer de pulmão, nichos de macrófagos, quimiocinas, imunoterapia do câncer