Clear Sky Science · he
נישות מאקרופאגיות המוגדרות על-ידי כימוקינים קובעות את הארגון המרחבי של חיסון הגידול
איך השכונות בתוך הגידול מעצבות את מאבק המערכת החיסונית
מדוע חלק מהגידולים נשארים מבוקרים בעוד אחרים צומחים ללא מעצורים, גם כשהם מלאים בתאי חיסון? המחקר בוחן גידולי ריאות בקנה מידה זעיר ומגלה שלא כל תאי החיסון זהים. במיוחד, קבוצות שונות של מאקרופאגים — תאים חיסוניים שמשמיעים תפקידי ניקיון ותיאום — מקימות "שכונות" מובחנות שיכולות לעזור לגוף להילחם בסרטן או, להיפך, לעודד את שגשוג הגידול. הבנת המפה הפנימית הזו של אזורים חיסוניים מועילים ומזיקים עשויה להוביל לטיפולים חכמים יותר ולחיסונים משופרים.
שניים לפניהם של מאקרופאגים בגידול
בדרך כלל מציירים את המאקרופאגים כסוג תא אחד, אך בריאה הם מתחלקים למספר קבוצות — תושבים ומגיעים מבחוץ. החוקרים התמקדו במאקרופאגים אינטרסטיציאליים, החיים ברקמה שבין השקיות האוויריות לכלי הדם, ובמאקרופאגים שמגויסים מהמחזור הדם בזמן המחלה. בעזרת פרופיל גנים תא-יחיד הראו שהמאקרופאגים התושבים מתחלקים לשני מחנות עיקריים. מחנה אחד, שנמצא בסמוך לסימפונות ולכלי דם, הציג פרופיל מולקולרי הקשור לתמיכה חיסונית ונשא אותות שמושכים לימפוציטים מועילים. המחנה השני, יחד עם המאקרופאגים המגויסים שנמצאים בליבות הגידול, הפגין תוכניות גנטיות הקשורות יותר לקידום גידול ולדיכוי התקפה חיסונית.
מיפוי הנוף החיסוני במרחב תלת־ממדי
כדי לראות היכן התאים יושבים בפועל בתוך הגידולים, החוקרים שילבו את נתוני התא-יחיד עם טרנסקריפטומיקה מרחבית — טכניקת הדמיה שמציגה פעילות גנים באופן ישיר בפרוסות רקמה. הם מצאו שמאקרופאגים תושבים מגוננים מרפדים אזורים ברונכיאליים וכליליים ומייצרים כימוקינים שמושכים תאי T ו-B, ועודדים היווצרות של צבירים חיסוניים מאורגנים וזעירים הנקראים מבנים לימפואידיים שלישוניים. 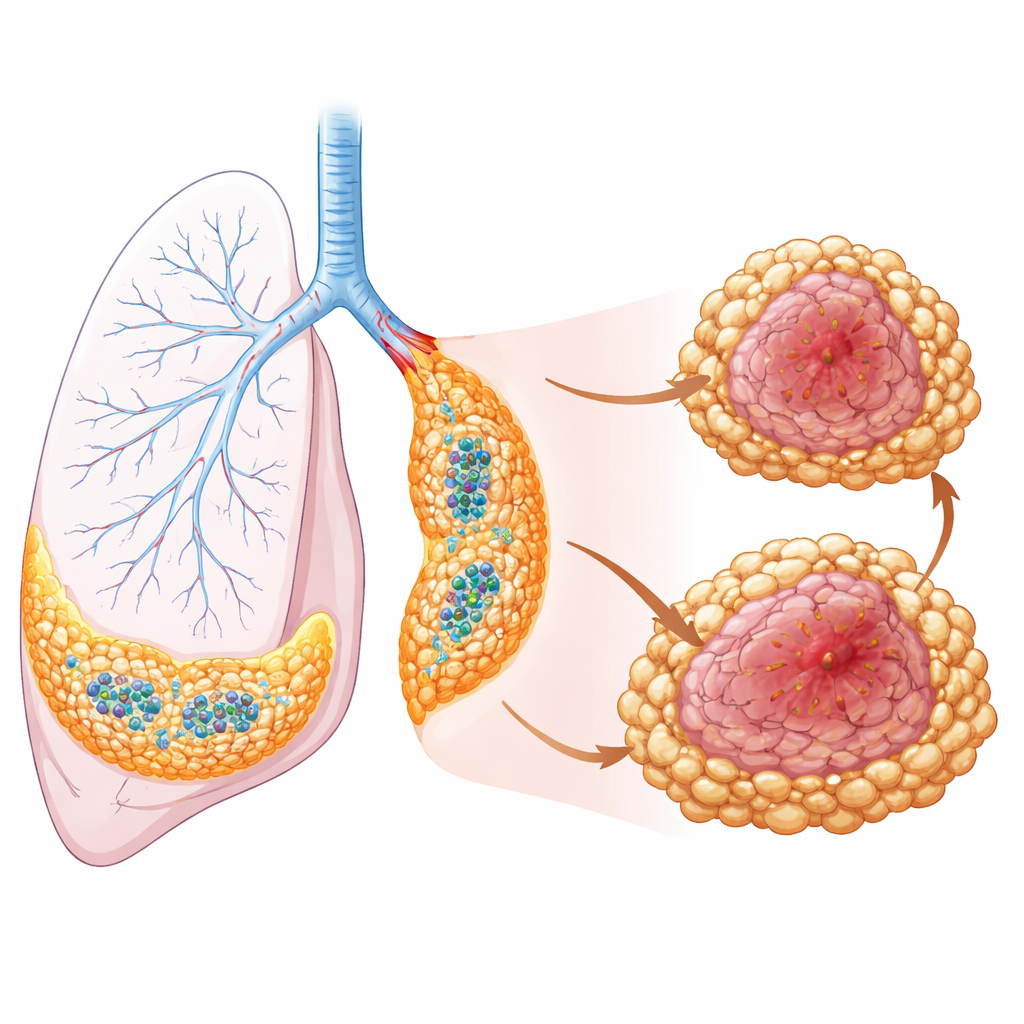
אותות שמזינים גידולים לעומת אותות שמגינים עליהם
כאשר הסירו באופן סלקטיבי את המאקרופאגים התושבים המגינים במודלים של עכברים עם מלנומה ואדנוקרצינומה של הריאה, הצוות ראה שהגידולים צמחו מהר יותר ומבנים לימפואידיים שלישוניים נעלמו. רמות כימוקינים מרכזיים שמושכים לימפוציטים ירדו בריאות, ופחות תאי T ו-B הצטברו בסמוך לגידולים. מצד שני, הכימוקין CCL2, שמיוצר בעיקר על-ידי מאקרופאגים אינטרסטיציאליים, התגלה כחיוני לגיוס מאקרופאגים ממחזור הדם. כאשר החוקרים ביטלו את ייצור ה-CCL2 רק מתאים חסרי מוצא ממח העצם, או במדויק מתאים מיאלואידיים קצרי־חיים תוך שמירה על מאקרופאגים תושבים ארוכי־חיים, פחות מאקרופאגים מגויסים נכנסו לריאות וצמיחת הגידול ירדה מאוד. ניסויים אלה הראו כי ה-CCL2 שמקורו במאקרופאגים מהווה קו אספקה בלתי־מוחל לגיוס תאים התומכים בגידול.
איך תאים נודדים מרגיעים תגובות חיסון לחיסון
הסיפור אינו מסתיים בתוך הגידול. חלק מהמאקרופאגים המגיעים הופכים לתאי דנדריטיים שמקורם במונוציטים ונושאים חומר גידול לצמתים הלימפתיות הסמוכות, שם מתחילות תגובות חיסוניות. באופן מפתיע, בהקשר זה הנוסעים האלה פועלים יותר כבלמים מאשר כמאיצים. הצוות מצא שתאים אלה מסתמכים על אות ייחודי להיגררות, CCR5, כדי להגיע לצמתים הלימפתיות. בעכברים מהונדסים כך שרק התאים שמקורם במונוציטים חסרו CCR5, גם המלנומה וגם סרטן הריאה צמחו פחות. 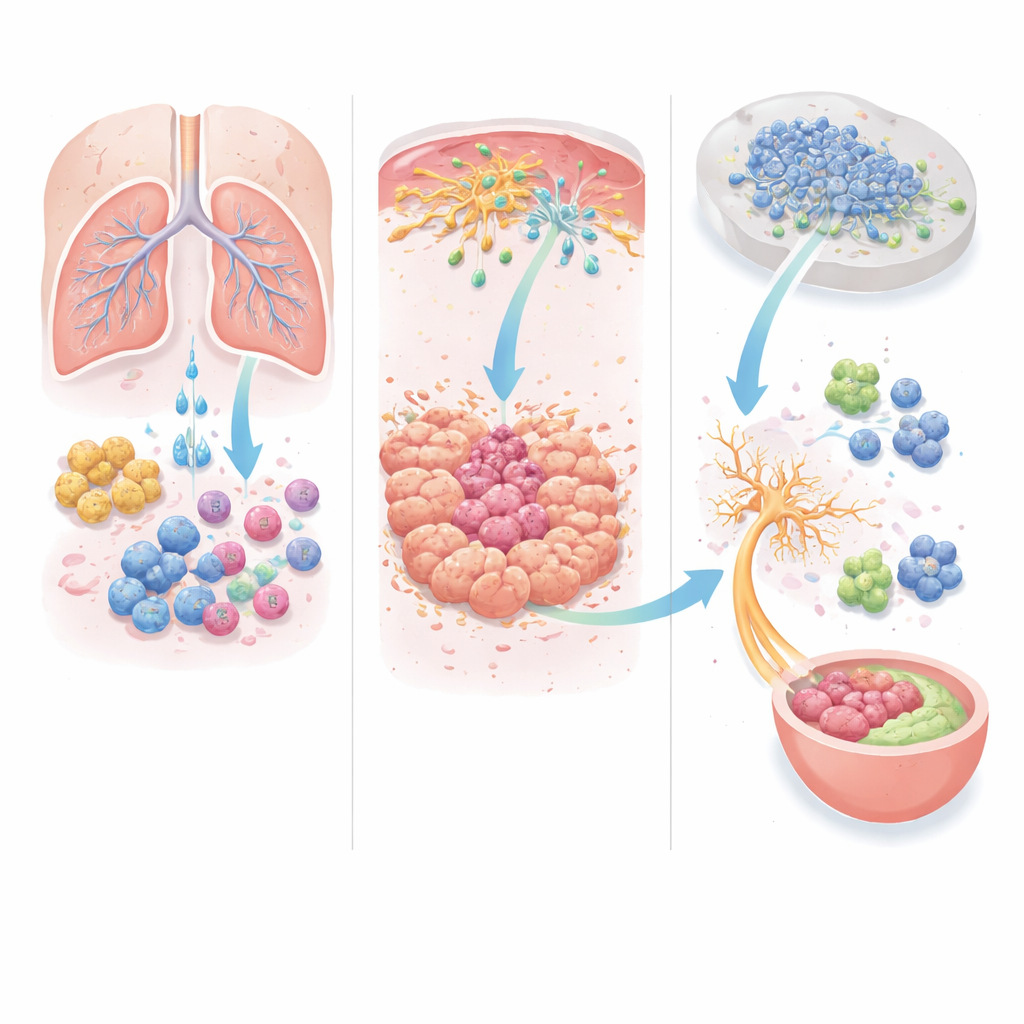
מה המשמעות של זה עבור טיפולים עתידיים בסרטן
העבודה מראה כי מיקום המאקרופאגים בריאה והאותות הכימיקליים שהם פולטים קובעים במידה רבה אם הם מסייעים או פוגעים בשליטה על הגידול. מאקרופאגים תושבים לאורך דרכי הנשימה וכלי הדם בונים שכונות עשירות במערכת חיסון שמטות לכיוון דחיית הגידול, בעוד מאקרופאגים אחרים בתוך ובסביב ליבות הגידול יוצרים אזורים המוגדרים על-ידי כימוקינים שמגייסים תאים מדכאים ומזינים את צמיחת הגידול. הממצאים מרמזים שאימונותרפיה יעילה תצטרך להיות מדויקת יותר מאשר "הגברה" או "חסימה" כוללת של מאקרופאגים. במקום זאת, אסטרטגיות עתידיות עשויות לשאוף לשמר או אפילו להרחיב את נישות המאקרופאגים התושבים המגנות, ולחתוך נתיבי מפתח — כגון גיוס מובל על-ידי CCL2 וזרימת תנועה התלויה ב-CCR5 — שמאפשרים לתאים מדכאים שמקורם במונוציטים להשתלט על סביבת הגידול ועל הצמתים הלימפתיים הסמוכים.
ציטוט: Ghosh, S., Li, X., Rawat, K. et al. Chemokine-defined macrophage niches establish spatial organization of tumor immunity. Nat Immunol 27, 715–724 (2026). https://doi.org/10.1038/s41590-026-02445-2
מילות מפתח: סביבת המיקרו של הגידול, חיסון בסרטן ריאה, נישות מאקרופאגיות, כימוקינים, אימונותרפיה של סרטן