Clear Sky Science · nl
Chemokine-gedefinieerde macrofaag-niches bepalen de ruimtelijke organisatie van tumorimmuniteit
Hoe buurten binnen tumoren de immuunstrijd vormen
Waarom blijven sommige tumoren onder controle terwijl andere ongehinderd groeien, zelfs wanneer ze veel immuuncellen bevatten? Deze studie kijkt op zeer fijne schaal in longtumoren en ontdekt dat niet alle immuuncellen gelijk zijn. Vooral verschillende groepen macrofagen — immuuncellen die zowel opruimers als coördinatoren zijn — creëren distincte “buurten” die het lichaam kunnen helpen kanker te bestrijden of juist stilletjes tumoren laten gedijen. Het in kaart brengen van deze interne kaart van gunstige en ongunstige immuunzones kan wijzen op slimmere kankertherapieën en betere vaccins.
Twee gezichten van tumor-macrofagen
Macrofagen worden vaak samengenomen als één celtype, maar in de long vallen ze uiteen in meerdere residentiële en binnenkomende groepen. De auteurs richtten zich op interstitiële macrofagen, die in het weefsel tussen luchtzakjes en bloedvaten wonen, en op gerekruteerde macrofagen die tijdens ziekte uit de bloedbaan arriveren. Met single-cell genprofilering toonden ze aan dat residentiële interstitiële macrofagen zich opsplitsen in twee hoofdgroepen. De ene groep, te vinden nabij luchtwegen en bloedvaten, vertoonde een moleculair profiel gekoppeld aan immuunondersteuning en droeg signalen die bekend zijn om behulpzame lymfocyten aan te trekken. De andere groep, samen met de binnenkomende gerekruteerde macrofagen in tumorcentra, droeg genprogramma’s die sterker verbonden zijn met tumorgroei en onderdrukking van immuuns-aanvallen.
Het immuunlandschap in 3D in kaart brengen
Om te zien waar deze cellen daadwerkelijk in tumoren zitten, combineerden de onderzoekers hun single-cell-gegevens met ruimtelijke transcripto-omics — een beeldvormende methode die genactiviteit rechtstreeks in weefselsnedes uitzet. Ze vonden dat beschermende residentiële macrofagen bronchiale en vasculaire gebieden bekleden en chemokines produceren die T- en B-cellen aantrekken, wat de vorming bevordert van kleine, georganiseerde immuunknooppunten genaamd tertiaire lymfoïde structuren. 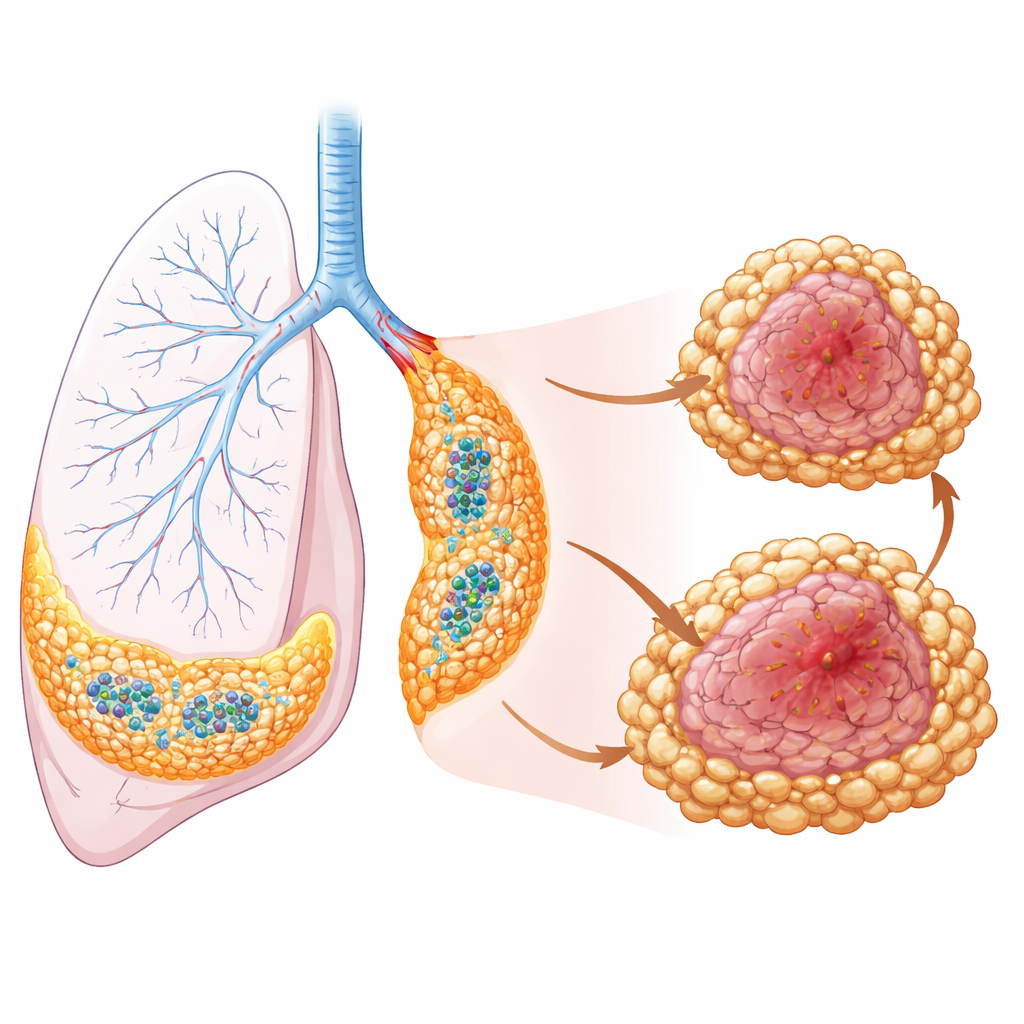
Signalering die tumoren voedt versus signalering die ze bewaakt
Door in muismodellen van melanoom en longadenocarcinoom de beschermende residentiële macrofagen selectief te verwijderen, zagen de onderzoekers dat tumoren sneller groeiden en tertiaire lymfoïde structuren verdwenen. De niveaus van sleutelchemokines die lymfocyten aantrekken, daalden in de longen en minder T- en B-cellen stapelden zich op nabij tumoren. Aan de andere kant bleek de chemokine CCL2, grotendeels geproduceerd door interstitiële macrofagen, cruciaal te zijn voor het aantrekken van gerekruteerde macrofagen uit het bloed. Wanneer de onderzoekers CCL2-productie alleen uitschakelden in beenmerg-afgeleide immuuncellen, of specifieker in kortlevende myeloïde cellen terwijl langlevende residentiële macrofagen behouden bleven, kwamen er minder gerekruteerde macrofagen de longen binnen en nam de tumorgroei sterk af. Deze experimenten toonden aan dat macrofaag-afgeleide CCL2 fungeert als een onmisbare toevoerroute voor het binnenbrengen van tumondersteunende cellen.
Hoe reizende cellen vaccinreacties dempen
Het verhaal eindigt niet binnen de tumor. Sommige van de binnenkomende macrofagen differentiëren tot monocytafgemaakte dendritische cellen die tumormateriaal naar naburige lymfeklieren vervoeren, waar immuunreacties worden geïnitieerd. Verrassend genoeg werken deze reizigers in deze context meer als remmen dan als versnellers. Het team ontdekte dat deze cellen afhankelijk zijn van een ander homingsignaal, CCR5, om lymfeklieren te bereiken. In muizen die zo werden geconstrueerd dat alleen monocytafgemaakte cellen CCR5 misten, groeiden zowel melanoom als longkanker minder. 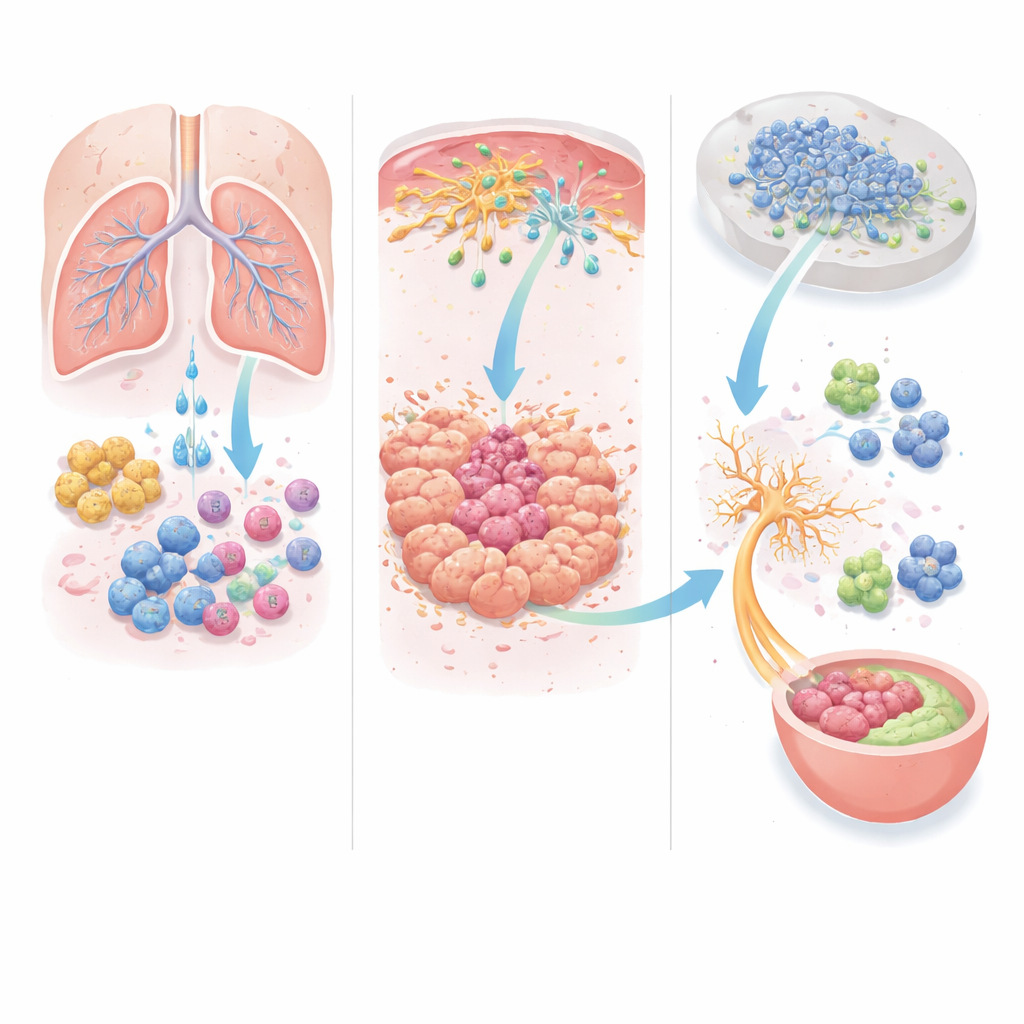
Wat dit betekent voor toekomstige kankerbehandelingen
Dit werk laat zien dat waar macrofagen zich in de long bevinden en welke chemische signalen ze uitstralen grotendeels bepaalt of ze helpen of hinderen bij tumorcontrole. Residentiële macrofagen langs luchtwegen en vaten bouwen immuunrijke buurten die tumorafwijzing bevorderen, terwijl andere macrofagen in en rond tumorcentra chemokine-gedefinieerde zones creëren die onderdrukkende cellen aantrekken en tumorgroei voeden. De bevindingen suggereren dat effectieve immunotherapie preciezer moet zijn dan simpelweg macrofagen in hun geheel te “versterken” of te “blokkeren”. In plaats daarvan kunnen toekomstige strategieën erop gericht zijn beschermende residentiële macrofaag-niches te behouden of zelfs uit te breiden, terwijl kritieke routes — zoals CCL2-gedreven rekrutering en CCR5-afhankelijke trafficking — worden afgesneden die onderdrukkende monocytafgemaakte cellen in staat stellen het tumormilieu en nabije lymfeklieren te domineren.
Bronvermelding: Ghosh, S., Li, X., Rawat, K. et al. Chemokine-defined macrophage niches establish spatial organization of tumor immunity. Nat Immunol 27, 715–724 (2026). https://doi.org/10.1038/s41590-026-02445-2
Trefwoorden: tumormicro-omgeving, longkanker-immuniteit, macrofagen-niches, chemokines, kankerimmunotherapie