Clear Sky Science · pl
Miejsca z makrofagami zdefiniowane przez chemokiny ustalają przestrzenną organizację odporności przeciwnowotworowej
Jak „dzielnice” w obrębie guza kształtują walkę układu odpornościowego
Dlaczego niektóre guzy pozostają pod kontrolą, podczas gdy inne rosną niepowstrzymanie, nawet jeśli zawierają wiele komórek odpornościowych? To badanie przygląda się wnętrzu nowotworów płuca w bardzo drobnym wymiarze i wykazuje, że nie wszystkie komórki odpornościowe są sobie równe. W szczególności różne grupy makrofagów — komórek odpornościowych pełniących funkcję zarówno sprzątaczy, jak i koordynatorów — tworzą odrębne „dzielnice”, które mogą albo wspierać walkę organizmu z rakiem, albo cicho sprzyjać rozwojowi guza. Zrozumienie tej wewnętrznej mapy stref sprzyjających i szkodliwych dla odporności może wskazać drogę do inteligentniejszych terapii przeciwnowotworowych i lepszych szczepionek.
Dwie twarze makrofagów nowotworowych
Makrofagi są często traktowane jako jeden typ komórek, ale w płucach dzielą się na kilka populacji rezydentnych i przybywających. Autorzy skupili się na makrofagach śródmiąższowych, które żyją w tkance między pęcherzykami płucnymi a naczyniami krwionośnymi, oraz na makrofagach rekrutowanych, które napływają z krwi podczas choroby. Przy użyciu profilowania pojedynczych komórek wykazali, że rezydentne makrofagi śródmiąższowe dzielą się na dwa główne obozy. Jeden obóz, zlokalizowany przy oskrzelach i naczyniach, wykazywał profil molekularny związany ze wsparciem odporności i wydzielał sygnały znane z przyciągania pomocnych limfocytów. Drugi obóz, wraz z napływającymi makrofagami rekrutowanymi w centrach guzów, prezentował programy genowe bardziej powiązane z wspieraniem wzrostu guza i tłumieniem ataku immunologicznego.
Mapowanie krajobrazu odporności w przestrzeni 3D
Aby zobaczyć, gdzie te komórki naprawdę się znajdują w guzach, badacze połączyli dane z pojedynczych komórek ze spatial transcriptomics — metodą obrazowania, która mapuje aktywność genów bezpośrednio w plastrach tkanki. Odkryli, że ochronne rezydentne makrofagi wyściełają obszary oskrzelowe i naczyniowe i produkują chemokiny przyciągające komórki T i B, sprzyjając tworzeniu niewielkich, zorganizowanych węzłów odpornościowych zwanych trzeciorzędowymi strukturami limfoidalnymi. 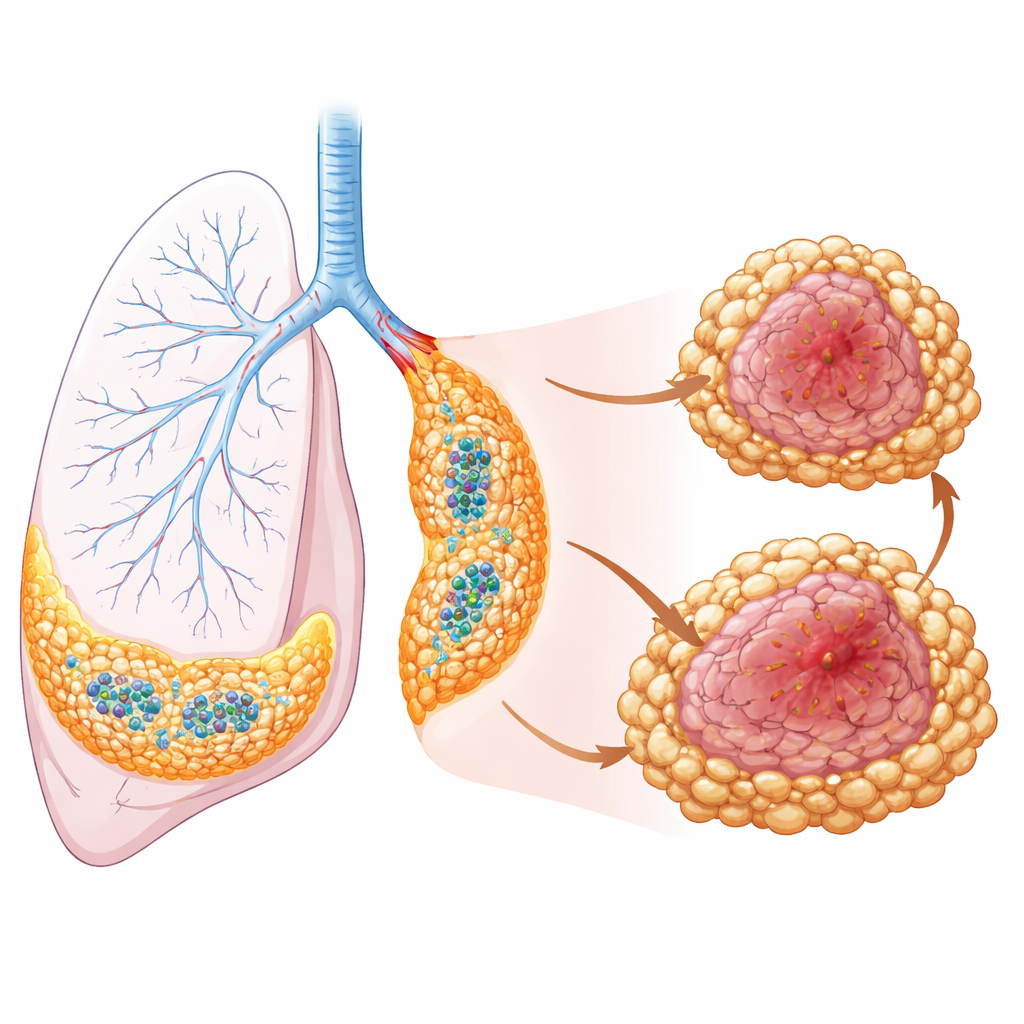
Sygnały karmiące guzy versus sygnały je chroniące
Usuwając selektywnie ochronne rezydentne makrofagi w modelach mysich czerniaka i gruczolakoraka płuca, zespół zaobserwował przyspieszenie wzrostu guzów i zanik trzeciorzędowych struktur limfoidalnych. Poziomy kluczowych chemokin przyciągających limfocyty spadły w płucach, a wokół guzów zgromadziło się mniej komórek T i B. Z drugiej strony chemokina CCL2, produkowana głównie przez makrofagi śródmiąższowe, okazała się kluczowa w przyciąganiu makrofagów rekrutowanych z krwi. Gdy badacze wyeliminowali produkcję CCL2 tylko w komórkach pochodzących ze szpiku kostnego, a precyzyjniej w krótkotrwałych komórkach mieloidalnych przy zachowaniu długowiecznych makrofagów rezydentnych, do płuc weszło mniej makrofagów rekrutowanych, a wzrost guza został wyraźnie zahamowany. Te eksperymenty wykazały, że CCL2 pochodzące od makrofagów działa jako niezastąpione „źródło zasilania” przyciągające komórki wspierające guz.
Jak wędrujące komórki tłumią odpowiedzi na szczepionki
Opowieść nie kończy się w samym guzie. Niektóre z napływających makrofagów przekształcają się w dendrytyczne komórki pochodzenia monocytarnego, które transportują materiał nowotworowy do pobliskich węzłów chłonnych, gdzie inicjowane są odpowiedzi odpornościowe. Zaskakująco, w tym kontekście wędrowcy ci działają bardziej jak hamulec niż przyspieszacz. Zespół odkrył, że te komórki polegają na innym sygnale kierunkowym, CCR5, by dotrzeć do węzłów chłonnych. U myszy zmodyfikowanych tak, że tylko komórki pochodzące z monocytów nie miały CCR5, zarówno czerniak, jak i rak płuca rosły słabiej. 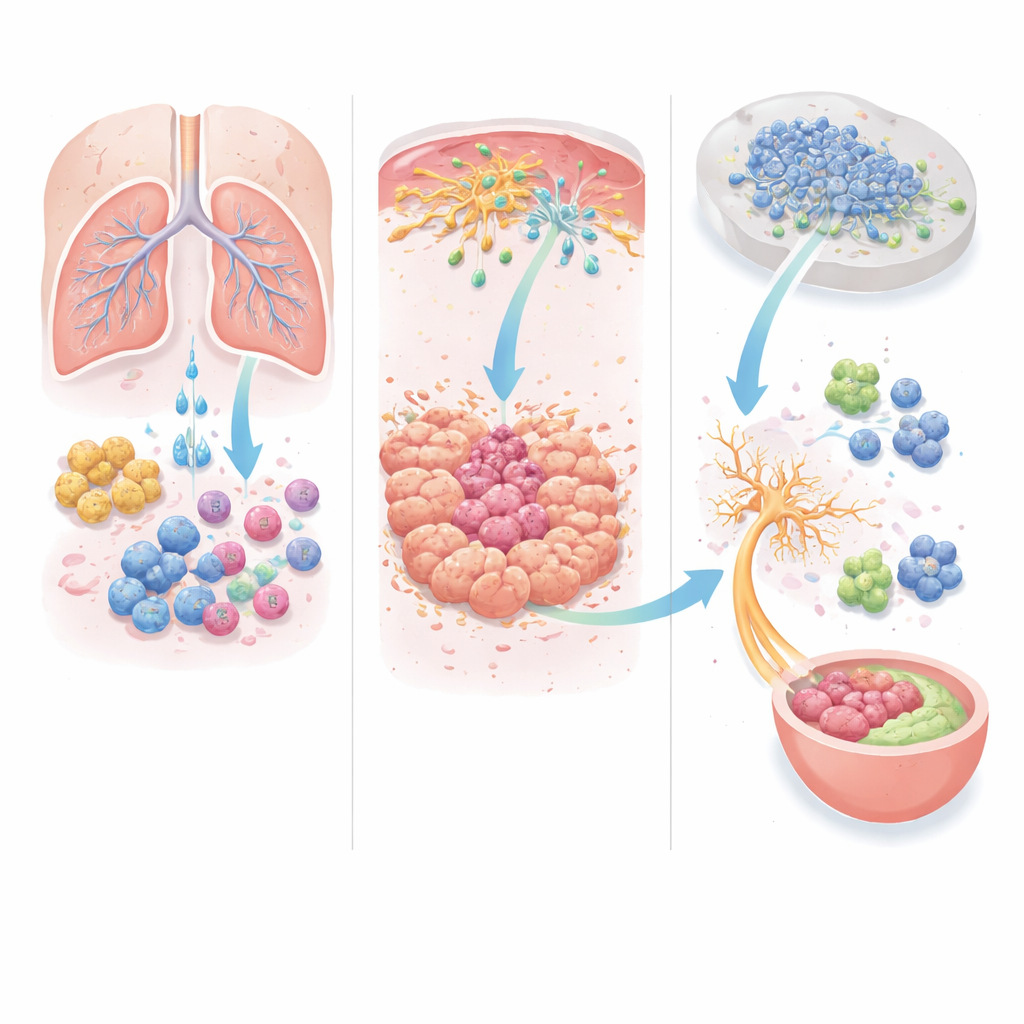
Co to znaczy dla przyszłych terapii przeciwnowotworowych
Ta praca pokazuje, że to, gdzie makrofagi znajdują się w obrębie płuca i jakie sygnały chemiczne wysyłają, w dużej mierze determinuje, czy pomagają, czy przeszkadzają w kontroli guza. Rezydentne makrofagi wzdłuż dróg oddechowych i naczyń budują bogate w odporność „dzielnice”, sprzyjające odrzuceniu guza, podczas gdy inne makrofagi w i wokół rdzeni guzów tworzą strefy zdefiniowane przez chemokiny, które rekrutują komórki supresyjne i napędzają wzrost nowotworu. Wyniki sugerują, że skuteczna immunoterapia będzie musiała być bardziej precyzyjna niż proste „wzmacnianie” lub „blokowanie” makrofagów jako całości. Zamiast tego przyszłe strategie mogą dążyć do zachowania lub nawet rozszerzenia ochronnych nisz rezydentnych makrofagów, jednocześnie odcinając kluczowe szlaki — takie jak rekrutacja napędzana przez CCL2 i transport zależny od CCR5 — które pozwalają dominować supresyjnym komórkom pochodzenia monocytarnego w środowisku guza i w pobliskich węzłach chłonnych.
Cytowanie: Ghosh, S., Li, X., Rawat, K. et al. Chemokine-defined macrophage niches establish spatial organization of tumor immunity. Nat Immunol 27, 715–724 (2026). https://doi.org/10.1038/s41590-026-02445-2
Słowa kluczowe: mikrośrodowisko guza, odporność na raka płuca, niche makrofagów, chemokiny, immunoterapia nowotworów