Clear Sky Science · zh
Tau蛋白磷酸化削弱保护性tau包膜的功能
为何细小的细胞“套管”对大脑健康至关重要
在每个神经细胞内部,称为微管的细长空心棒状结构像铁轨一样,运输维持细胞生命的货物。这些“轨道”被一种名为tau的蛋白覆盖,形成围绕它们的保护性套管。在阿尔茨海默病及相关脑病中,tau发生大量修饰并凝集成缠结,同时微管崩解。本文填补了这一难题中的一块缺失拼图:显示对tau的一种常见化学修饰——磷酸化,直接削弱了这些保护性套管,使细胞内部的轨道更易受损。
细胞内“轨道”上的保护外套
微管是赋予神经细胞形态并提供重要运输通道的长蛋白管。在健康状态下,tau分子并非单独漂浮;它们可以在微管表面紧密聚集,形成作者所称的致密、连续层状“包膜”。这些包膜起到绝缘套的作用:它们减缓或阻挡某些其他蛋白,包括可将微管切断的“剪刀”类分子酶(切割酶)。先前的研究表明,当tau仅松散附着并单独移动时,微管很容易成为这些剪刀的目标;而当tau形成有凝聚力的包膜时,轨道则受到强有力的保护。 
化学“标签”如何破坏外套
研究团队探问当tau被磷酸化时会发生什么,磷酸化是一个正常的调控过程,但在退化性大脑中被大幅放大。利用纯化蛋白和高分辨率显微镜,他们比较了去磷酸化的tau(带有很少化学标签)与携带大量磷酸基团的tau。在极低浓度下,去磷酸化tau能自发沿微管组装成大而连续的包膜,而磷酸化tau多以单个、可移动分子存在。即便在两种形式都处于较高水平并可形成包膜时,磷酸化形式覆盖微管表面的程度较低,其包膜更薄且更易出现“间隙”,显示tau分子之间的凝聚力减弱。
实时观察套管如何崩解
为探测稳定性,研究者先用较少修饰的tau构建包膜,然后加入一种与脑相关的酶Cdk5,该酶会向tau添加磷酸基团。他们观察到包膜从边缘后退,甚至裂成碎片,像剥落的外套。进一步分析显示,磷酸化不仅削弱了tau对微管的附着力,还减少了tau分子之间的相互粘结,这两者都是形成稳固套管所必需的。在活细胞中,他们使用荧光技术监测微管上的tau。正常tau表现为周转慢、几近固定的层状存在,与包膜一致。无法形成包膜的tau突变体,或暴露于Cdk5作用下的tau,交换速度明显更快,表明其附着更松散、更脆弱,这与体外结果相符。 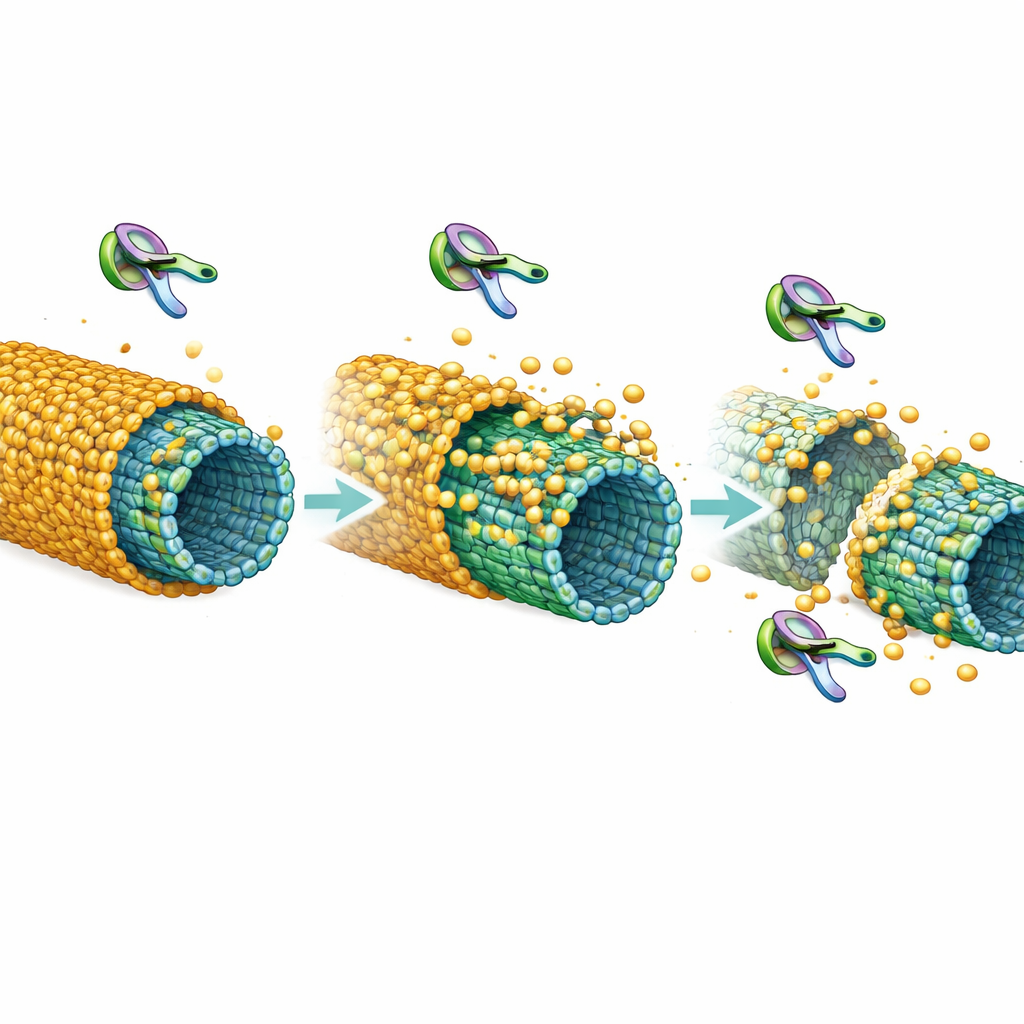
从脆弱套管到断裂的轨道
关键问题是这些变化是否影响微管的存续。作者转而研究一种强效切割酶katanin。在裸露或松散包被的微管上,katanin会迅速将管状结构切断。当微管被结实的tau包膜包裹时,它们大体保持完整,证实了包膜的保护作用。然而,当包膜由磷酸化tau构成时,保护明显减弱:包膜覆盖区内出现更多切口,且微管尽管表面tau密度看似相似,却解体得更快。在培养细胞中,单独过度表达katanin会导致微管急剧丧失,但同时共表达全长tau可挽救微管格架。共表达不能形成包膜的tau,或通过Cdk5驱动tau的额外磷酸化,则在很大程度上丧失了这种保护,使微管被侵蚀。
这对阿尔茨海默病等疾病意味着什么
总体而言,研究表明大量磷酸化的tau不仅仅将其从微管上轻推下来:它破坏了tau包膜的形成、稳定性和屏蔽能力。随着tau越来越多被磷酸化,包膜解体,tau释放到细胞内可能形成聚集体,暴露的微管则成为切割酶的易受损目标。这一组合可以逐步剥夺轴突和树突内部的轨道,破坏运输和结构,远在大型缠结出现之前就已产生影响。对普通读者而言,结论是:与阿尔茨海默病相关的化学变化削弱了通常保护神经细胞“高速公路”的微观‘套管’,有助于解释大脑连线如何在分子层面开始松散。
引用: Siahaan, V., Weissova, R., Karhanova, A. et al. Tau phosphorylation impedes functionality of protective tau envelopes. Nat Chem Biol 22, 759–769 (2026). https://doi.org/10.1038/s41589-025-02122-9
关键词: tau蛋白, 微管, 磷酸化, 阿尔茨海默病, 神经退行性疾病