Clear Sky Science · nl
Fosforylering van tau belemmert de functionaliteit van beschermende tau‑omhulsels
Waarom kleine cellulaire “mouwen” van belang zijn voor de hersengezondheid
In elke zenuwcel fungeren lange holle staven, microtubuli genoemd, als spoorlijnen die lading vervoeren en de cel in leven houden. Deze spoorlijnen zijn bedekt met een eiwit genaamd tau, dat een beschermende mouw om hen heen vormt. Bij de ziekte van Alzheimer en aanverwante hersenaandoeningen wordt tau sterk gemodificeerd en klontert het samen tot verwarde ophopingen, terwijl microtubuli uiteen vallen. Dit artikel vult een ontbrekend stukje in die puzzel aan: het toont aan dat een veelvoorkomende chemische verandering van tau, fosforylering genaamd, rechtstreeks deze beschermende mouwen verzwakt en de interne spoorlijnen van de cel kwetsbaar achterlaat voor schade.
Beschermende jassen op de interne rails van de cel
Microtubuli zijn lange proteïnebuizen die zenuwcellen hun vorm geven en snelwegen bieden voor essentieel transport. Onder gezonde omstandigheden zweven tau‑moleculen niet zomaar vrij rond; ze kunnen zich dicht op het oppervlak van microtubuli verzamelen en daarmee dichte, continue lagen vormen die de auteurs “omhulsels” noemen. Deze omhulsels werken als isolerende mouwen: ze vertragen of blokkeren bepaalde andere eiwitten, waaronder moleculaire scharen die bekendstaan als severing‑enzymen en die microtubuli in stukken kunnen knippen. Eerder werk liet zien dat wanneer tau slechts losjes vastzit en individueel beweegt, microtubuli gemakkelijke doelwitten zijn voor deze scharen. Wanneer tau cohesieve omhulsels vormt, worden de sporen sterk beschermd. 
Hoe chemische “labels” de jas doen scheuren
Het team vroeg zich af wat er gebeurt wanneer tau gefosforyleerd is, een normale regulerende stap die in degenererende hersenen sterk wordt opgevoerd. Met gezuiverde eiwitten en microscopie met hoge resolutie vergeleken ze gedephosphoryleerd tau (met weinig chemische labels) met tau waaraan veel fosfaatgroepen waren toegevoegd. Bij zeer lage concentraties assembleerde gedephosphoryleerd tau gemakkelijk tot grote, continue omhulsels langs microtubuli, terwijl gefosforyleerd tau meestal als losse, mobiele moleculen bleef bestaan. Zelfs wanneer beide vormen in hogere concentraties aanwezig waren en omhulsels konden vormen, bedekte de gefosforyleerde variant minder van het microtubulusoppervlak en waren de omhulsels dunner en gevoeliger voor “kieren”, wat wijst op verminderde cohesie tussen tau‑moleculen.
De mouwen in realtime zien instorten
Om de stabiliteit te onderzoeken, bouwden de onderzoekers omhulsels uit relatief ongemodificeerd tau en voegden vervolgens een hersengerelateerd enzym toe, Cdk5, dat fosfaatgroepen aan tau plakt. Ze zagen de omhulsels terugtrekken vanaf de randen en zelfs in stukken splitsen, als een afbladderende jas. Verdere analyse toonde aan dat fosforylering niet alleen de hechting van tau aan microtubuli verzwakt, maar ook vermindert hoe sterk tau‑moleculen aan elkaar kleven — beide zijn nodig voor een stevige mouw. In levende cellen gebruikten ze fluorescentietechnieken om tau op microtubuli te volgen. Normaal tau gedroeg zich als een laag met een langzaam turnover, bijna vastgeplakt, consistent met een omhulsel. Tau‑mutanten die geen omhulsels kunnen vormen, of tau blootgesteld aan Cdk5, wisselden veel sneller uit, wat wijst op een lossere, fragielere binding die overeenkomt met de in‑vitro resultaten. 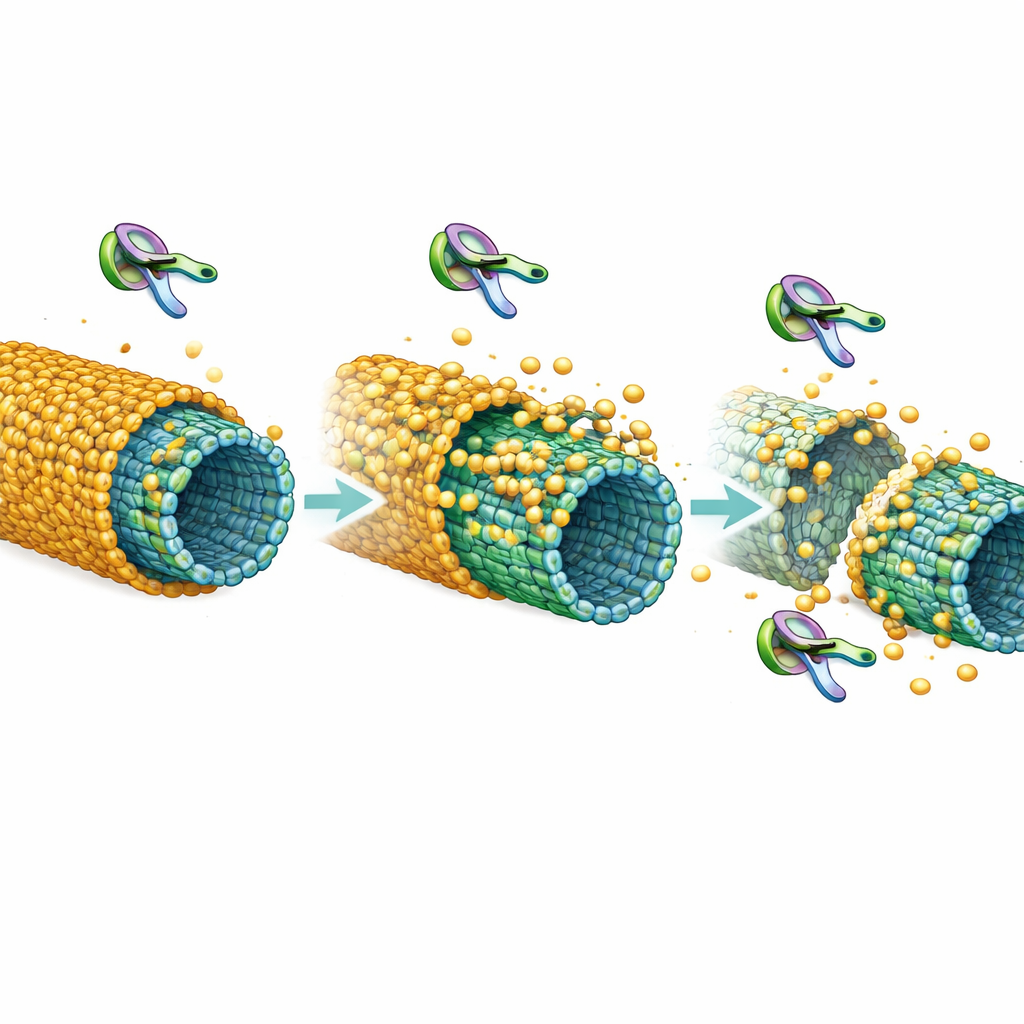
Van fragiele mouwen naar gebroken sporen
De cruciale vraag was of deze veranderingen van belang zijn voor het voortbestaan van microtubuli. De auteurs richtten zich op katanin, een krachtig severing‑enzym. Op blote of los bedekte microtubuli sneed katanin de buizen snel doormidden. Wanneer microtubuli waren omwikkeld met robuuste tau‑omhulsels, bleven ze grotendeels intact, wat de beschermende rol van de jas bevestigde. Echter, wanneer omhulsels waren opgebouwd uit gefosforyleerd tau, was de bescherming merkbaar zwakker: er ontstonden meer knippen binnen de bedekte gebieden en microtubuli vielen sneller uiteen, zelfs wanneer de tau‑dichtheid er vergelijkbaar uitzag. In gecultiveerde cellen leidde overexpressie van katanin alleen tot een scherp verlies van microtubuli, maar co‑expressie van volledig tau herstelde het lattice. Co‑expressie van tau die geen omhulsels kan vormen, of het extra fosforyleren van tau via Cdk5, verwijderde deze bescherming grotendeels en liet microtubuli wegvagen.
Wat dit betekent voor ziekten zoals Alzheimer
Samengevat laat de studie zien dat zware fosforylering van tau meer doet dan het lichtjes van microtubuli duwen: het verstoort de vorming, stabiliteit en beschermende kracht van tau‑omhulsels. Naarmate tau meer gefosforyleerd raakt, vallen omhulsels uiteen, komt tau vrij in de cel waar het kan aggregëren, en worden de blootgestelde microtubuli makkelijke doelwitten voor severing‑enzymen. Deze combinatie kan geleidelijk axonen en dendrieten ontdoen van hun interne spoorlijnen, waardoor transport en structuur worden ondermijnd lang voordat grote kluwens verschijnen. Voor de niet‑specialist is de boodschap dat Alzheimer‑gerelateerde chemische wijzigingen aan tau de microscopische “mouwen” verzwakken die normaal de snelwegen van zenuwcellen beschermen, en zo helpen verklaren hoe de bedrading van de hersenen op moleculair niveau begint te rafelen.
Bronvermelding: Siahaan, V., Weissova, R., Karhanova, A. et al. Tau phosphorylation impedes functionality of protective tau envelopes. Nat Chem Biol 22, 759–769 (2026). https://doi.org/10.1038/s41589-025-02122-9
Trefwoorden: tau‑eiwit, microtubuli, fosforylering, Ziekte van Alzheimer, neurodegeneratie