Clear Sky Science · de
Tau-Phosphorylierung beeinträchtigt die Funktion schützender Tau-Hüllen
Warum winzige zelluläre „Ärmel“ für die Gehirngesundheit wichtig sind
Innerhalb jeder Nervenzelle fungieren lange, hohle Röhren, die Mikrotubuli genannt werden, wie Eisenbahnschienen und transportieren Fracht, die die Zelle am Leben erhält. Diese Schienen sind von einem Protein namens Tau überzogen, das eine schützende Hülle um sie bildet. Bei Alzheimer und verwandten Hirnerkrankungen wird Tau stark verändert und verklumpt zu Fibrillen, während Mikrotubuli zerfallen. Diese Arbeit enthüllt ein fehlendes Stück des Puzzles: Sie zeigt, dass eine verbreitete chemische Veränderung von Tau, die Phosphorylierung, diese schützenden Hüllen direkt schwächt und die inneren Schienen der Zelle verwundbar für Schäden macht.
Schutzmäntel auf den inneren Schienen der Zelle
Mikrotubuli sind lange Proteinröhren, die Nervenzellen ihre Form geben und als Autobahnen für lebenswichtigen Transport dienen. Unter gesunden Bedingungen schwimmen Tau-Moleküle nicht einfach frei umher; sie können sich dicht an der Oberfläche der Mikrotubuli anlagern und dichte, durchgehende Schichten bilden, die die Autoren als „Hüllen“ bezeichnen. Diese Hüllen wirken wie isolierende Ärmel: Sie verlangsamen oder blockieren bestimmte andere Proteine, darunter molekulare Scheren, sogenannte Severing-Enzyme, die Mikrotubuli zerschneiden können. Frühere Arbeiten zeigten, dass Mikrotubuli, wenn Tau nur locker gebunden und einzeln beweglich ist, leichte Ziele für diese Scheren sind. Bildet Tau kohäsive Hüllen, sind die Schienen stark geschützt. 
Wie chemische „Markierungen“ den Mantel zerstören
Das Team fragte, was passiert, wenn Tau phosphoryliert wird, ein normaler Regulationsprozess, der in degenerierenden Gehirnen stark übersteigert ist. Mit gereinigten Proteinen und hochauflösender Mikroskopie verglichen sie dephosphoryliertes Tau (mit wenigen chemischen Markierungen) mit Tau, das viele Phosphatgruppen trägt. Bei sehr niedrigen Konzentrationen bildete dephosphoryliertes Tau leicht große, durchgehende Hüllen entlang der Mikrotubuli, während phosphoryliertes Tau größtenteils als einzelne, mobile Moleküle blieb. Selbst wenn beide Formen in höheren Mengen vorhanden waren und Hüllen bilden konnten, bedeckte die phosphorylierte Variante weniger der Mikrotubulusoberfläche, und ihre Hüllen waren dünner und anfälliger für Lücken, was eine verringerte Kohäsion zwischen den Tau-Molekülen zeigte.
Die Hüllen in Echtzeit beim Zerfall beobachten
Um die Stabilität zu prüfen, bauten die Forscher Hüllen aus relativ unverändertem Tau und fügten dann ein gehirnrelevantes Enzym, Cdk5, hinzu, das Phosphatgruppen an Tau anhängt. Sie beobachteten, wie die Hüllen von ihren Rändern zurückwichen und sogar in Stücke aufspalteten, wie ein sich abziehender Mantel. Weitergehende Analysen zeigten, dass Phosphorylierung nicht nur den Halt von Tau an Mikrotubuli schwächt, sondern auch verringert, wie stark Tau-Moleküle aneinander haften — beides erforderlich für einen stabilen Ärmel. In lebenden Zellen verwendeten sie Fluoreszenztechniken, um Tau an Mikrotubuli zu überwachen. Normales Tau verhielt sich wie eine Schicht mit langsamem Austausch, fast festgeklebt, was zu einer Hülle passt. Tau-Mutanten, die keine Hüllen bilden können, oder Tau, das Cdk5 ausgesetzt war, tauschten deutlich schneller aus, was auf eine lockerere, fragilere Bindung hinweist, die den In-vitro-Ergebnissen entspricht. 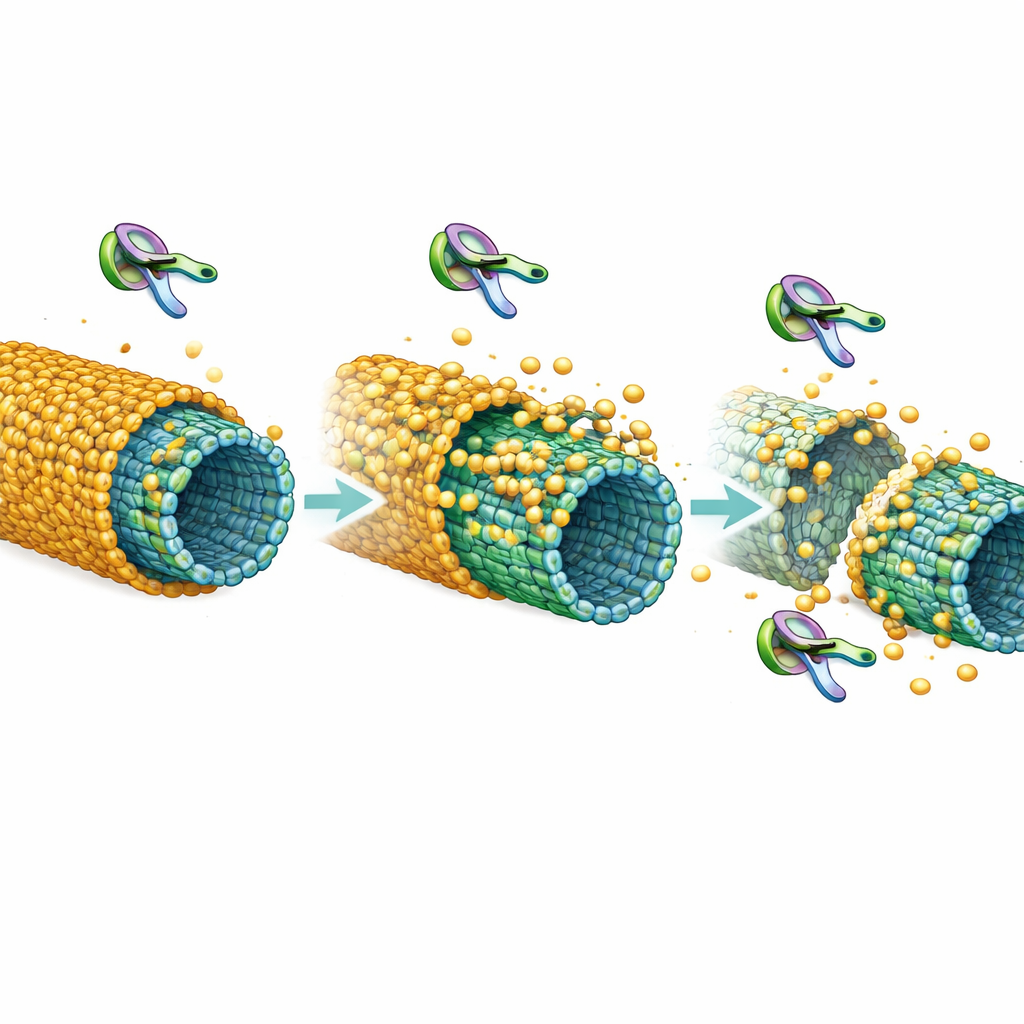
Von fragilen Ärmeln zu gebrochenen Schienen
Die entscheidende Frage war, ob diese Veränderungen für das Überleben der Mikrotubuli relevant sind. Die Autoren wandten sich an Katanin, ein kräftiges Severing-Enzym. Auf unbedeckten oder locker beschichteten Mikrotubuli schnitt Katanin die Röhren schnell in Stücke. Waren die Mikrotubuli jedoch in robuste Tau-Hüllen eingewickelt, blieben sie weitgehend intakt, was die schützende Rolle des Mantels bestätigte. Wurden die Hüllen jedoch aus phosphoryliertem Tau gebildet, war der Schutz spürbar schwächer: Mehr Schnitte erschienen innerhalb der bedeckten Bereiche, und die Mikrotubuli zerfielen schneller, obwohl die Tau-Dichte ähnlich aussah. In kultivierten Zellen führte die Überproduktion von Katanin allein zu einem starken Verlust von Mikrotubuli, aber die Koexpression von Voll-Längen-Tau rettete das Gitter. Koexpression von Tau, das keine Hüllen bilden kann, oder das verstärkte Phosphorylieren von Tau durch Cdk5 beseitigte diesen Schutz weitgehend und ließ die Mikrotubuli erodieren.
Was das für Krankheiten wie Alzheimer bedeutet
Insgesamt zeigt die Studie, dass starke Phosphorylierung von Tau mehr bewirkt, als es nur von Mikrotubuli zu stoßen: Sie stört die Bildung, Stabilität und Schutzwirkung der Tau-Hüllen. Mit zunehmender Phosphorylierung zerfallen die Hüllen, Tau wird in die Zelle freigesetzt, wo es aggregieren kann, und die freigelegten Mikrotubuli werden zu leichten Zielen für Severing-Enzyme. Diese Kombination kann Axone und Dendriten schrittweise ihrer inneren Schienen entkleiden, den Transport und die Struktur untergraben, lange bevor große Fibrillen sichtbar werden. Für Laien lautet die Botschaft, dass Alzheimer-assoziierte chemische Veränderungen an Tau die mikroskopischen „Ärmel“ schwächen, die normalerweise die Verkehrsadern der Nervenzellen schützen, und damit helfen zu erklären, wie die Verkabelung des Gehirns auf molekularer Ebene zu bröckeln beginnt.
Zitation: Siahaan, V., Weissova, R., Karhanova, A. et al. Tau phosphorylation impedes functionality of protective tau envelopes. Nat Chem Biol 22, 759–769 (2026). https://doi.org/10.1038/s41589-025-02122-9
Schlüsselwörter: Tau-Protein, Mikrotubuli, Phosphorylierung, Alzheimer-Krankheit, Neurodegeneration