Clear Sky Science · fr
La phosphorylation de la protéine tau compromet la fonctionnalité des « manchons » protecteurs
Pourquoi de minuscules « manchons » cellulaires comptent pour la santé du cerveau
À l’intérieur de chaque neurone, de longues tiges creuses appelées microtubules servent de rails, transportant le matériel indispensable à la survie de la cellule. Ces rails sont recouverts par une protéine appelée tau, qui forme autour d’eux un manchon protecteur. Dans la maladie d’Alzheimer et d’autres troubles cérébraux apparentés, la tau subit de lourdes modifications et s’agrège en enchevêtrements, tandis que les microtubules se désagrègent. Cet article révèle une pièce manquante du puzzle : il montre qu’une modification chimique fréquente de la tau, la phosphorylation, affaiblit directement ces manchons protecteurs et laisse les rails internes de la cellule vulnérables aux dommages.
Des revêtements protecteurs sur les rails intérieurs de la cellule
Les microtubules sont de longs tubes protéiques qui donnent leur forme aux neurones et offrent des autoroutes pour le transport vital. Dans des conditions saines, les molécules de tau ne flottent pas simplement de façon isolée ; elles peuvent se regrouper étroitement à la surface des microtubules pour former des couches denses et continues que les auteurs appellent « manchons ». Ces manchons jouent un rôle d’isolant : ils ralentissent ou bloquent certaines autres protéines, notamment des ciseaux moléculaires appelés enzymes de sectionnement qui peuvent couper les microtubules en morceaux. Des travaux antérieurs avaient montré que lorsque la tau est faiblement attachée et mobile, les microtubules sont des cibles faciles pour ces ciseaux. Quand la tau forme des manchons cohésifs, les rails sont fortement protégés. 
Comment des « étiquettes » chimiques fragilisent le manteau
Les chercheurs se sont demandé ce qui se passe lorsque la tau est phosphorylée, un processus de régulation normal qui est fortement exagéré dans les cerveaux en dégénérescence. En utilisant des protéines purifiées et de la microscopie à haute résolution, ils ont comparé la tau déphosphorylée (peu d’étiquettes chimiques) à la tau portant de nombreux groupes phosphate. À de très faibles concentrations, la tau déphosphorylée s’assemblait facilement en grands manchons continus le long des microtubules, tandis que la tau phosphorylée restait majoritairement sous forme de molécules individuelles et mobiles. Même lorsque les deux formes étaient présentes à des niveaux plus élevés et pouvaient former des manchons, la version phosphorylée couvrait une moindre surface des microtubules et ses manchons étaient plus fins et plus « parsemés de trous », montrant une cohésion réduite entre les molécules de tau.
Observer la désintégration des manchons en temps réel
Pour sonder la stabilité, les chercheurs ont construit des manchons à partir de tau relativement non modifiée puis ont ajouté une enzyme cérébrale, Cdk5, qui ajoute des groupes phosphate à la tau. Ils ont observé les manchons se retirer à partir de leurs bords et même se fendre en morceaux, comme un manteau qui pèle. Des analyses supplémentaires ont montré que la phosphorylation affaiblit non seulement l’adhérence de la tau aux microtubules, mais réduit aussi la force d’attraction entre molécules de tau, deux éléments nécessaires à un manchon solide. Dans des cellules vivantes, ils ont utilisé des techniques de fluorescence pour suivre la tau sur les microtubules. La tau normale se comportait comme une couche à renouvellement lent, presque collée, compatible avec l’existence d’un manchon. Les mutants de tau incapables de former des manchons, ou la tau exposée à la Cdk5, échangeaient beaucoup plus rapidement, indiquant une fixation plus lâche et plus fragile en accord avec les résultats in vitro. 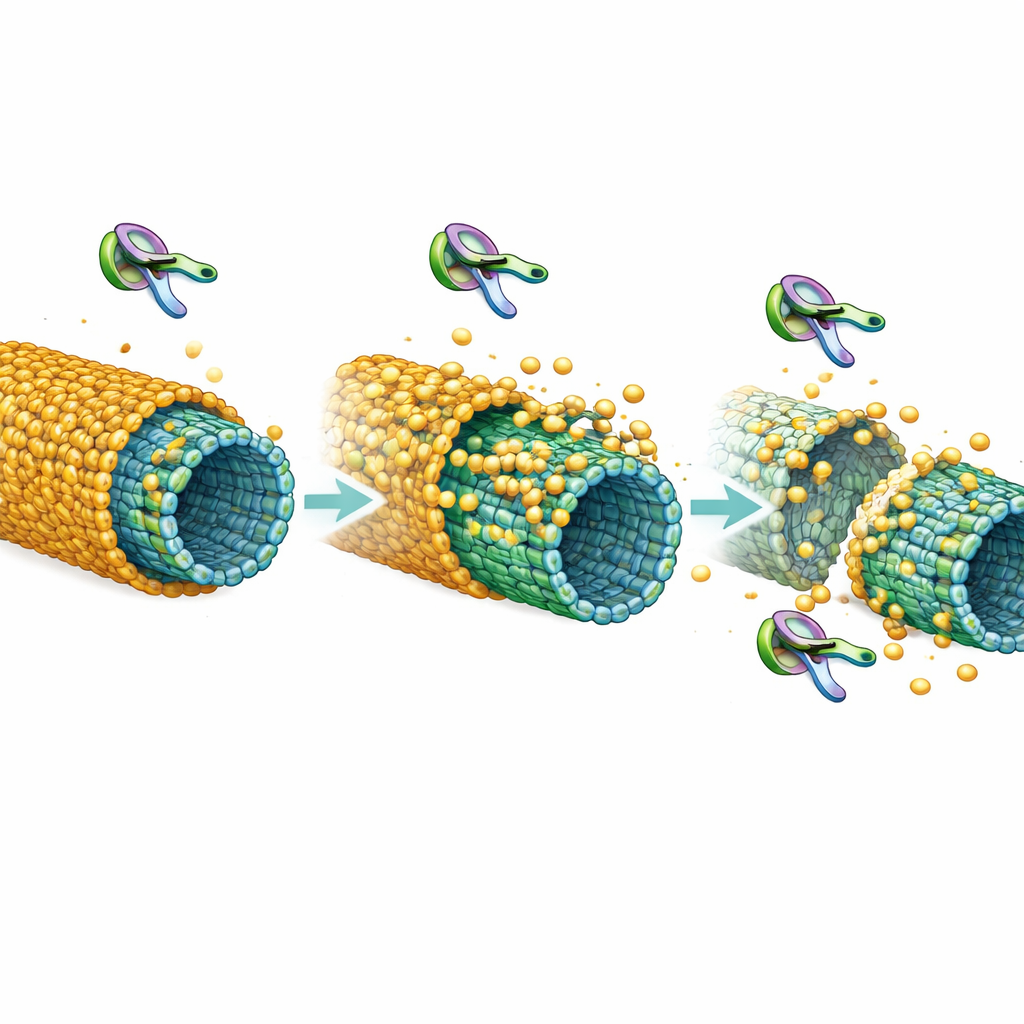
De manchons fragiles à rails brisés
La question cruciale était de savoir si ces changements affectent la survie des microtubules. Les auteurs se sont intéressés à la katanine, une puissante enzyme de sectionnement. Sur des microtubules nus ou faiblement recouverts, la katanine découpait rapidement les tubes. Lorsque les microtubules étaient enveloppés de manchons tau robustes, ils restaient pour la plupart intacts, confirmant le rôle protecteur du revêtement. Cependant, lorsque les manchons étaient constitués de tau phosphorylée, la protection était visiblement affaiblie : davantage de coupures apparaissaient dans les régions recouvertes, et les microtubules se désarmaient plus vite, même si la densité de tau semblait similaire. Dans des cultures cellulaires, la surexpression de la katanine seule entraînait une perte marquée de microtubules, mais la co‑expression de tau pleine longueur sauvait le réseau. Co‑exprimer une tau incapable de former des manchons, ou induire une phosphorylation accrue de la tau via Cdk5, supprimait largement cette protection et permettait l’érosion des microtubules.
Ce que cela signifie pour des maladies comme Alzheimer
Dans l’ensemble, l’étude montre que la phosphorylation massive de la tau fait plus que la déloger des microtubules : elle perturbe la formation, la stabilité et le pouvoir protecteur des manchons de tau. À mesure que la tau devient plus phosphorylée, les manchons se désassemblent, la tau est libérée dans la cellule où elle peut s’agréger, et les microtubules exposés deviennent des cibles faciles pour les enzymes de sectionnement. Cette combinaison peut peu à peu dépouiller les axones et les dendrites de leurs rails internes, compromettant le transport et la structure bien avant l’apparition de gros enchevêtrements. Pour un lecteur non spécialiste, le message est que les modifications chimiques de la tau liées à Alzheimer affaiblissent les « manchons » microscopiques qui protègent normalement les autoroutes des neurones, ce qui aide à expliquer comment le câblage du cerveau commence à se déliter au niveau moléculaire.
Citation: Siahaan, V., Weissova, R., Karhanova, A. et al. Tau phosphorylation impedes functionality of protective tau envelopes. Nat Chem Biol 22, 759–769 (2026). https://doi.org/10.1038/s41589-025-02122-9
Mots-clés: protéine tau, microtubules, phosphorylation, maladie d’Alzheimer, neurodégénérescence