Clear Sky Science · tr
Tau fosforilasyonu koruyucu tau kılıflarının işlevini engelliyor
Hücre içindeki küçük “kılıflar” neden beyin sağlığı için önemli
Her sinir hücresinin içinde, yol boyunca yük taşıyan ve hücrenin canlı kalmasını sağlayan uzun boş çubuklar olan mikrotübüller, tren rayları gibi davranır. Bu raylar, etraflarına koruyucu bir kılıf oluşturan tau adlı bir proteinle kaplıdır. Alzheimer hastalığında ve ilişkili beyin bozukluklarında tau yoğun biçimde değişime uğrar ve yumaklar oluşturarak birikirken mikrotübüller parçalanır. Bu çalışma bu bulmacanın eksik bir parçasını ortaya koyuyor: tau üzerindeki yaygın bir kimyasal değişiklik olan fosforilasyonun, bu koruyucu kılıfları doğrudan zayıflattığını ve hücrenin içsel raylarını hasara karşı savunmasız bıraktığını gösteriyor.
Hücrenin iç raylarına tutulan koruyucu örtüler
Mikrotübüller, sinir hücrelerine şekil veren ve hayati taşımacılık için otoyollar sağlayan uzun protein tüpleridir. Sağlıklı koşullarda, tau molekülleri sadece serbestçe yüzmez; mikrotübüllerin yüzeyinde sıkıca toplanarak yazarların “kılıf” dediği yoğun, sürekli katmanlar oluşturabilirler. Bu kılıflar yalıtkan birer kılıf gibi davranır: bazı diğer proteinleri, mikrotübülleri parçalayan makas benzeri kesme enzimleri dahil olmak üzere, yavaşlatır veya engeller. Önceki çalışmalar, tau gevşek bağlı ve tek tek hareket ederken mikrotübüllerin bu makaslar için kolay hedefler olduğunu göstermişti. Tau kohezif kılıflar oluşturduğunda ise raylar güçlü biçimde korunur. 
Kimyasal “etiketler” kılıfı nasıl bozar
Araştırma ekibi, tau fosforilendiğinde ne olduğunu sordu; bu normal bir düzenleyici süreç olup dejeneratif beyinlerde aşırıya kaçar. Saflaştırılmış proteinler ve yüksek çözünürlüklü mikroskopi kullanarak, az fosforile olmuş (az kimyasal etikete sahip) tau ile çok sayıda fosfat grubu taşıyan tauyu karşılaştırdılar. Çok düşük konsantrasyonlarda, de-fosforile tau mikrotübüller boyunca kolaylıkla büyük, sürekli kılıflar oluştururken, fosforile tau çoğunlukla bireysel, hareketli moleküller halinde kaldı. Her iki form daha yüksek düzeylerde bulunup kılıf oluşturabilse bile, fosforile versiyon mikrotübül yüzeyini daha az örttü ve kılıfları daha ince ve daha “boşluk eğilimli”ydi; bu da tau molekülleri arasındaki kohezyonun azaldığını gösteriyordu.
Kılıfların gerçek zamanlı çöküşünü izlemek
Stabiliteyi incelemek için araştırmacılar göreli olarak az değiştirilmiş tau ile kılıflar inşa etti ve ardından tauya fosfat ekleyen beyinle ilişkili bir enzim olan Cdk5’i eklediler. Kılıfların kenarlarından geri çekildiğini ve hatta bir soyulan kılıf gibi parçalara ayrıldığını gözlemlediler. Daha ileri analizler fosforilasyonun yalnızca tau’nun mikrotübüllere tutunmasını zayıflatmakla kalmadığını, aynı zamanda tau moleküllerinin birbirine yapışma gücünü de azalttığını gösterdi; sağlam bir kılıf için her ikisi de gereklidir. Canlı hücrelerde, mikrotübüller üzerindeki tau’yu izlemek için floresans teknikleri kullandılar. Normal tau yavaş değişen, neredeyse yapışmış bir katman gibi davrandı; bu, bir kılıfla uyumluydu. Kılıf oluşturamayan tau mutantları veya Cdk5’e maruz kalan tau çok daha hızlı değişim gösterdi; bu, in vitro bulgularla uyumlu olarak daha gevşek, daha kırılgan bir bağlanmayı işaret ediyordu. 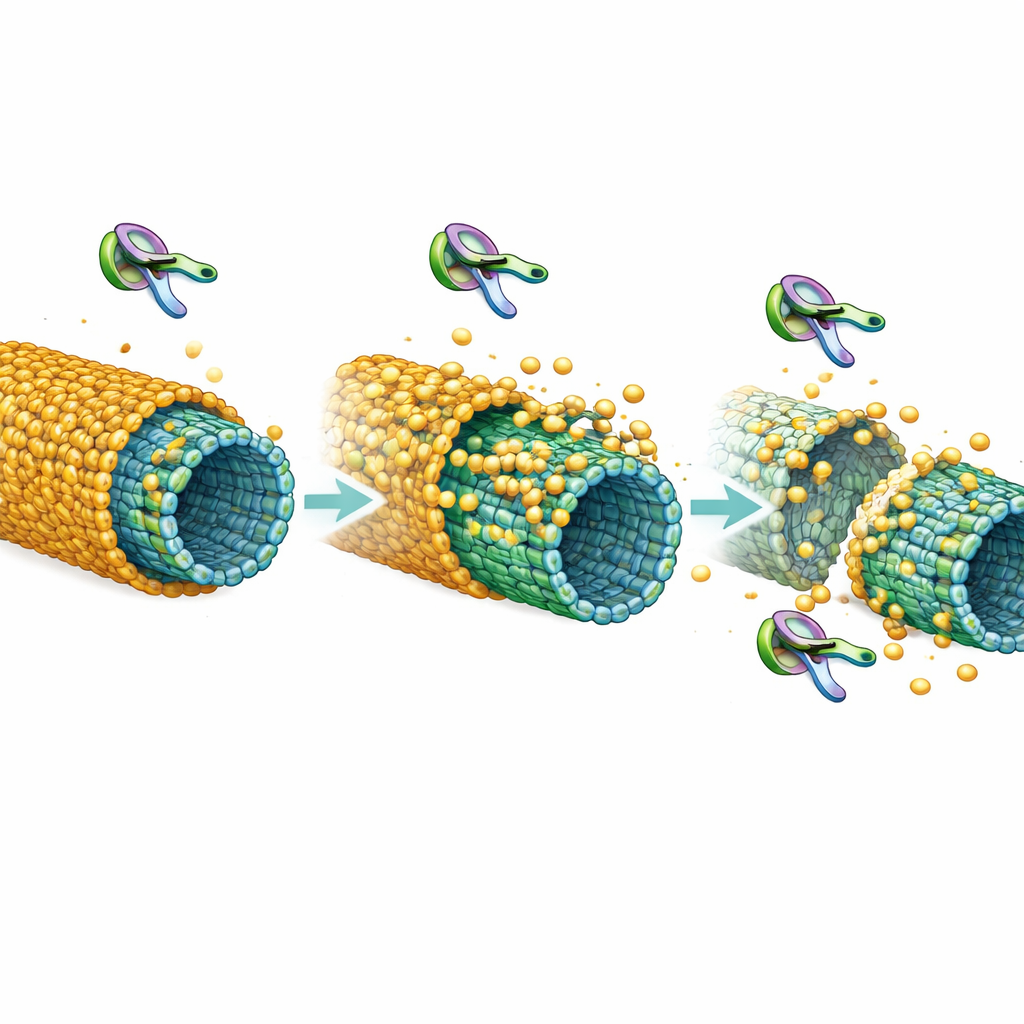
Kırılgan kılıflardan parçalanmış raylara
Önemli soru, bu değişikliklerin mikrotübül hayatta kalması için önemi olup olmadığıydı. Yazarlar güçlü bir kesme enzimi olan katanine yöneldiler. Çıplak veya gevşek kaplı mikrotübüller üzerinde katanin tüpleri hızla parçaladı. Mikrotübüller sağlam tau kılıflarıyla sarıldığında büyük ölçüde bütün kaldılar; bu da kılıfın koruyucu rolünü doğruladı. Ancak kılıflar fosforile tau’dan yapıldığında koruma belirgin şekilde zayıftı: kaplı bölgelerde daha fazla kesik ortaya çıktı ve mikrotübüller tau yoğunluğu benzer görünse bile daha hızlı çözündü. Kültürdeki hücrelerde yalnızca katanini aşırı üretmek mikrotübüllerin hızla kaybına yol açarken, tam uzunlukta tau ile eş zamanlı ifade örgüyü kurtardı. Kılıf oluşturamayan tau ile eş zamanlı ifade veya Cdk5 aracılığıyla tau’nun aşırı fosforilasyonu bu korumayı büyük ölçüde ortadan kaldırdı ve mikrotübüllerin erozyonuna izin verdi.
Alzheimer gibi hastalıklar için anlamı
Genel olarak çalışma, tau’nun yoğun fosforilasyonunun onu mikrotübüllerden hafifçe uzaklaştırmaktan daha fazlasını yaptığını; tau kılıflarının oluşumunu, stabilitesini ve koruyucu gücünü bozduğunu gösteriyor. Tau daha fazla fosforilendikçe kılıflar çözülür, tau hücre içine salınır ve burada agregasyon oluşturabilir; açığa çıkan mikrotübüller ise kesme enzimleri için kolay hedef haline gelir. Bu kombinasyon akson ve dendritleri içsel raylarından yavaşça soyabilir, büyük yumaklar ortaya çıkmadan çok önce taşıma ve yapıyı zayıflatabilir. Bir düz okuyucu için çıkarılacak mesaj şudur: Alzheimer ile ilişkili tau’daki kimyasal değişiklikler, sinir hücresi otoyollarını normalde koruyan mikroskobik “kılıfları” zayıflatır ve beynin bağlantılarının moleküler düzeyde nasıl çözülmeye başladığını açıklamaya yardımcı olur.
Atıf: Siahaan, V., Weissova, R., Karhanova, A. et al. Tau phosphorylation impedes functionality of protective tau envelopes. Nat Chem Biol 22, 759–769 (2026). https://doi.org/10.1038/s41589-025-02122-9
Anahtar kelimeler: tau proteini, mikrotübüller, fosforilasyon, Alzheimer hastalığı, nörodejenerasyon