Clear Sky Science · sv
Tau-fosforylering försvagar skyddande tau-sleeves
Varför små cell‑”ärmar” spelar roll för hjärnhälsa
Inuti varje nervcell fungerar långa, ihåliga stavar kallade mikrotubuli som räls, och transporterar gods som håller cellen vid liv. Dessa rälsar är täckta av ett protein som heter tau, vilket bildar ett skyddande hölje runt dem. Vid Alzheimers sjukdom och besläktade hjärnstörningar förändras tau kraftigt och klumpar ihop sig till trassel, samtidigt som mikrotubuli faller sönder. Denna artikel avslöjar en saknad pusselbit: den visar att en vanlig kemisk förändring av tau, kallad fosforylering, direkt försvagar dessa skyddande höljen och lämnar cellens inre rälsar sårbara för skador.
Skyddande mantel på cellens inre räls
Mikrotubuli är långa proteintuber som ger nervceller form och fungerar som motorvägar för livsviktig transport. Under friska förhållanden flyter inte tau-molekyler bara fritt; de kan samlas tätt på mikrotubulernas yta och bilda täta, kontinuerliga lager som författarna kallar ”envelopes” (höljen). Dessa höljen fungerar som isolerande ärmar: de bromsar eller blockerar vissa andra proteiner, inklusive molekylära saxar kända som severing‑enzymer som kan klippa mikrotubuli i bitar. Tidigare arbete visade att när tau sitter löst och rör sig individuellt är mikrotubuli enkla mål för dessa saxar. När tau bildar sammanhängande höljen skyddas rälsen kraftigt. 
Hur kemiska ”etiketter” bryter manteln
Forskarna frågade vad som händer när tau fosforyleras, en normal regleringsprocess som är kraftigt överdriven i degenererande hjärnor. Genom att använda renade proteiner och högupplöst mikroskopi jämförde de defosforylerad tau (med få kemiska etiketter) med tau som bar många fosfatgrupper. Vid mycket låga koncentrationer monterade defosforylerad tau lätt ihop till stora, kontinuerliga höljen längs mikrotubuli, medan fosforylerad tau mest förblev som individuella, rörliga molekyler. Även när båda formerna fanns i högre nivåer och kunde bilda höljen, täckte den fosforylerade versionen mindre av mikrotubuliytan och dess höljen var tunnare och mer ”glappiga”, vilket visade minskad sammanhållning mellan tau‑molekylerna.
Att se ärmarna falla sönder i realtid
För att undersöka stabiliteten byggde forskarna höljen av relativt omodifierad tau och tillsatte sedan ett hjärnrelaterat enzym, Cdk5, som lägger till fosfatgrupper på tau. De såg hur höljen drog sig tillbaka från kanterna och till och med sprack i bitar, som en skalande mantel. Vidare analys visade att fosforylering inte bara försvagar taus grepp om mikrotubuli utan också minskar hur starkt tau‑molekyler fäster vid varandra, båda nödvändiga för en solid mantel. I levande celler använde de fluorescensmetoder för att övervaka tau på mikrotubuli. Normal tau uppträdde som ett skikt med långsam omsättning, nästan som fastlimmat, i linje med ett hölje. Tau‑mutanter som inte kan bilda höljen, eller tau exponerat för Cdk5, bytte plats mycket snabbare, vilket indikerar en lösare, mer skör bindning som stämmer med in vitro‑resultaten. 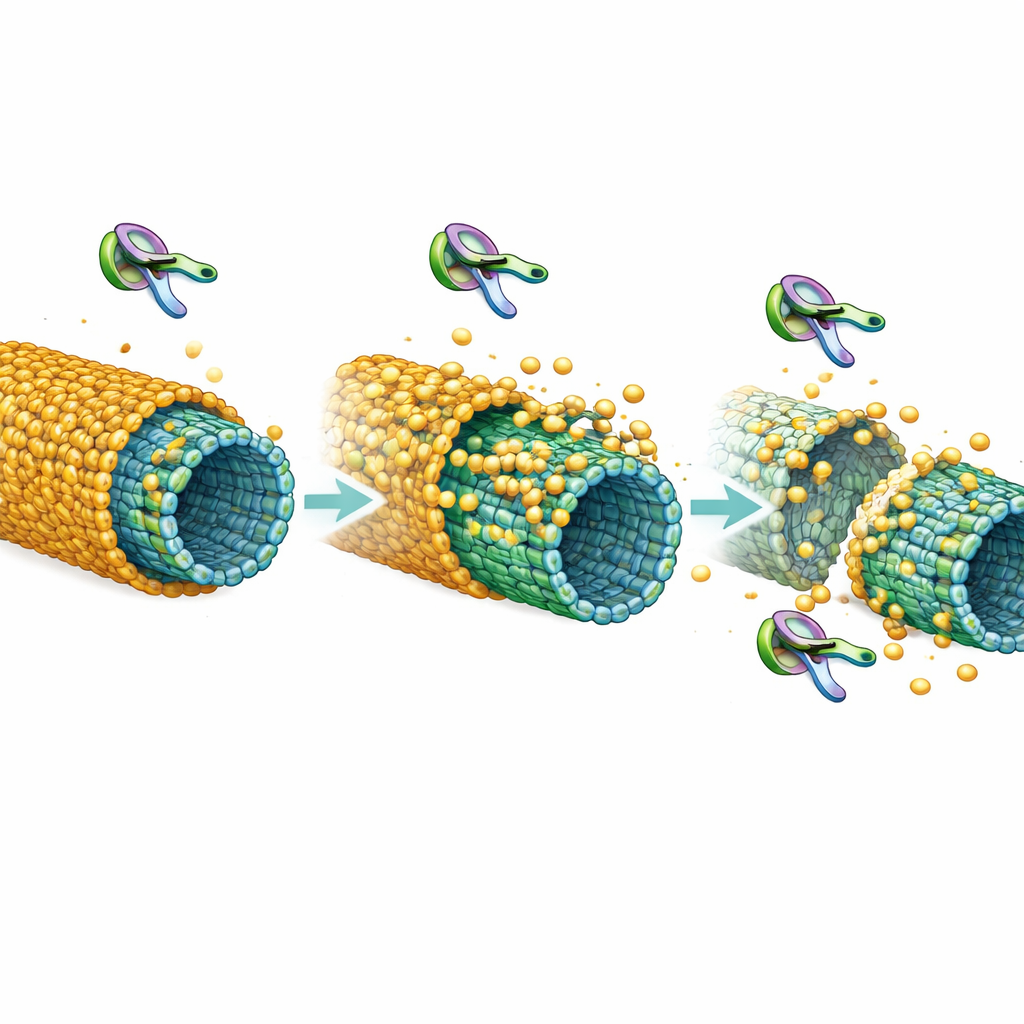
Från sköra ärmar till brutna rälsar
Den avgörande frågan var om dessa förändringar spelar roll för mikrotubulis överlevnad. Författarna vände sig till katanin, ett kraftfullt severing‑enzym. På nakna eller löst täckta mikrotubuli kapade katanin snabbt rören. När mikrotubuli var omslutna av robusta tau‑höljen förblev de till stor del intakta, vilket bekräftade mantelns skyddande roll. Men när höljen var gjorda av fosforylerad tau var skyddet märkbart svagare: fler snitt dök upp inom de täckta regionerna, och mikrotubuli demonterades snabbare trots att tau‑densiteten såg liknande ut. I odlade celler ledde överproduktion av katanin ensam till en kraftig förlust av mikrotubuli, men samtidig uttryck av fullängds‑tau räddade skelettet. Samuttryck av tau som inte kan bilda höljen, eller ökad fosforylering av tau via Cdk5, tog i hög grad bort detta skydd och tillät mikrotubuli att erodera.
Vad detta betyder för sjukdomar som Alzheimers
Sammantaget visar studien att kraftig fosforylering av tau gör mer än att knuffa det bort från mikrotubuli: det stör bildandet, stabiliteten och skyddsförmågan hos tau‑höljen. När tau blir mer fosforylerat löses höljen upp, tau frigörs i cellen där det kan aggregera, och de exponerade mikrotubuli blir enkla mål för severing‑enzymer. Denna kombination kan gradvis beröva axoner och dendriter på deras inre rälsar, undergräva transport och struktur långt innan stora trassel uppstår. För en allmän läsare är budskapet att Alzheimers‑kopplade kemiska förändringar av tau försvagar de mikroskopiska ”ärmar” som normalt skyddar nervcellernas motorvägar, vilket hjälper till att förklara hur hjärnans ledningar börjar fransa ur på molekylär nivå.
Citering: Siahaan, V., Weissova, R., Karhanova, A. et al. Tau phosphorylation impedes functionality of protective tau envelopes. Nat Chem Biol 22, 759–769 (2026). https://doi.org/10.1038/s41589-025-02122-9
Nyckelord: tau-protein, mikrotubuli, fosforylering, Alzheimers sjukdom, neurodegeneration