Clear Sky Science · zh
在小鼠与人类中检验边缘系统α‑突触核蛋白病变与髓鞘标志物之间的反向关联
这为何与脑健康有关
帕金森病和相关的“路易体”疾病以运动障碍著称,但在症状出现之前,这些疾病也涉及大脑连线的细微改变。本研究提出了一个看似简单的问题:某些易受损的大脑区域是否因其神经纤维髓鞘包裹较差——即缺乏有利于快速信号传导的脂质包层——而在这些疾病中更易受累?通过将人类脑组织样本与小鼠实验相结合,研究者检验了髓鞘减少是否真的会导致帕金森样疾病中有害蛋白聚集体的增加。
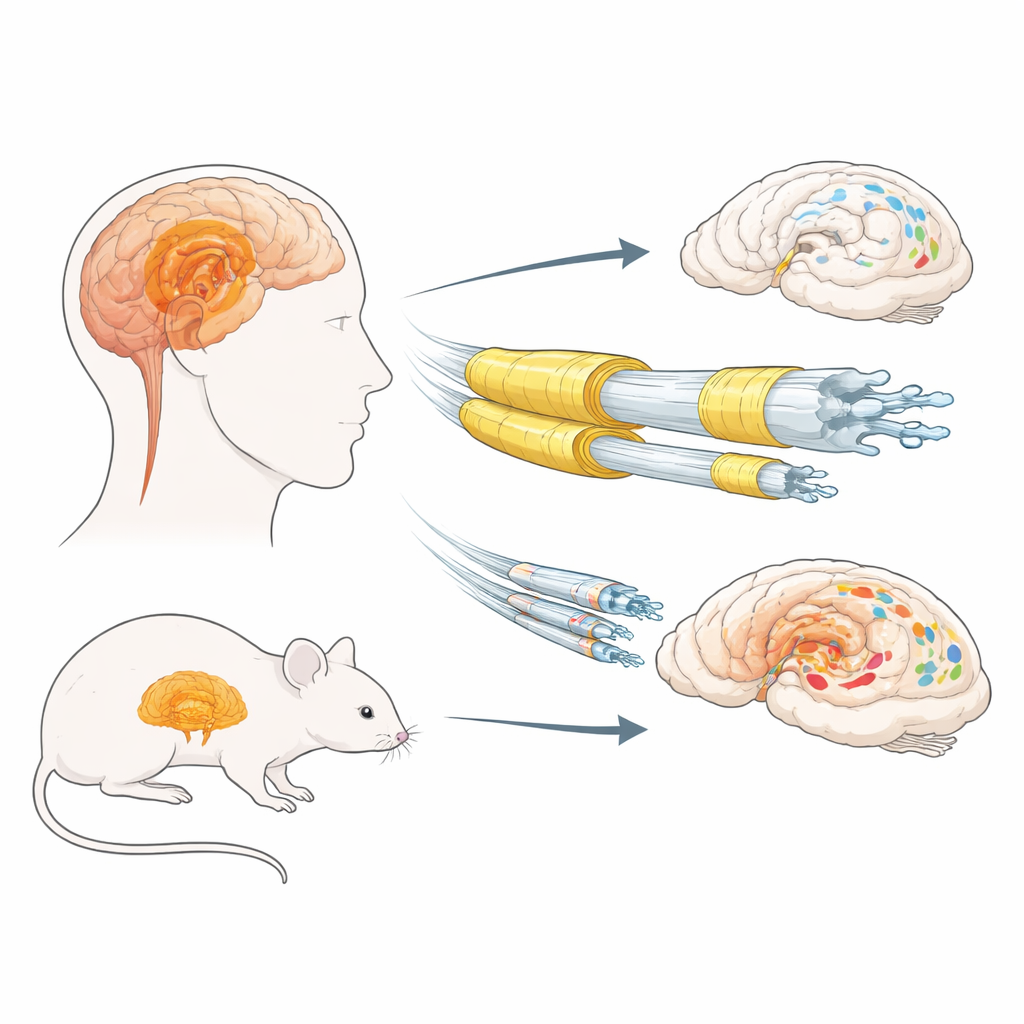
大脑的绝缘层与蛋白聚集
在路易体疾病中,一种正常的大脑蛋白α‑突触核蛋白可能发生错误折叠并在神经细胞内积聚,形成称为路易体和路易神经突的斑块。早期研究提示,长而细、髓鞘较差的神经纤维可能尤其脆弱。髓鞘由支持细胞——少突胶质细胞生成,并含有若干关键结构蛋白,包括髓鞘碱性蛋白(MBP)和蛋白脂质蛋白(PLP)。作者首先检查了来自嗅球和杏仁核的尸检组织——这些是与嗅觉和情绪相关的边缘系统区域——来自有无路易体疾病的男性与女性。他们测量了若干髓鞘标志物,并将其与不溶性、被高度修饰(过度磷酸化)的α‑突触核蛋白水平进行了比较。
人类边缘组织中的性别相关模式
人类数据揭示了一个显著的性别特异性模式。在患有路易体疾病的男性杏仁核中,不溶性、过度磷酸化的α‑突触核蛋白含量较高与一种特定PLP形式(20千道尔顿异构体)水平较低相关,并且有迹象表明其他与髓鞘相关的基因也有所下降。这种反向关系在女性中未见。结果提示,至少在男性中,杏仁核中更严重的路易样病理倾向于伴随较弱的髓鞘特征。然而,这些是来自终末期组织的相关性观察:无法判断髓鞘丧失是促使α‑突触核蛋白病理加重,还是病理逐渐损伤了髓鞘。
在小鼠中检验髓鞘作用
为超越相关性,研究团队转向可实验性扰动髓鞘的小鼠模型。他们向小鼠大脑的嗅觉‑边缘区域注入了预形成纤维(preformed fibrils)型的α‑突触核蛋白——这些微小种子能触发类路易样聚集体。部分小鼠饲喂铜络合物cuprizone,这种化合物会破坏髓鞘并导致动物体重下降;另一些小鼠携带“颤抖者”(shiverer)遗传突变,使MBP的产生减半。设想很简单:若髓鞘欠佳确实使神经元更易受损,则这些操纵应显著放大α‑突触核蛋白聚集体的扩散、神经细胞损伤和行为问题。
髓鞘损伤仅带来有限的推动
结果比预期更温和。cuprizone明确降低了关键髓鞘蛋白并改变了雄性小鼠的白质结构,证实绝缘层受损。然而,尽管纤维注射可靠地在灰质区域产生了类路易包涵体,cuprizone仅在一个位点(丝氨酸‑129)略微增加了过度磷酸化的不溶性α‑突触核蛋白的比例。总体不溶性α‑突触核蛋白的总量、神经元健康的测量指标以及一系列记忆、探索和嗅觉测试并未因髓鞘损伤而显著恶化。同样,携带颤抖者突变的小鼠——尽管髓鞘更薄——与正常同窝小鼠相比,除蛋白聚集体平均尺寸略有增大外,并未显示边缘系统α‑突触核蛋白病理或行为缺陷的明确、系统性增加。
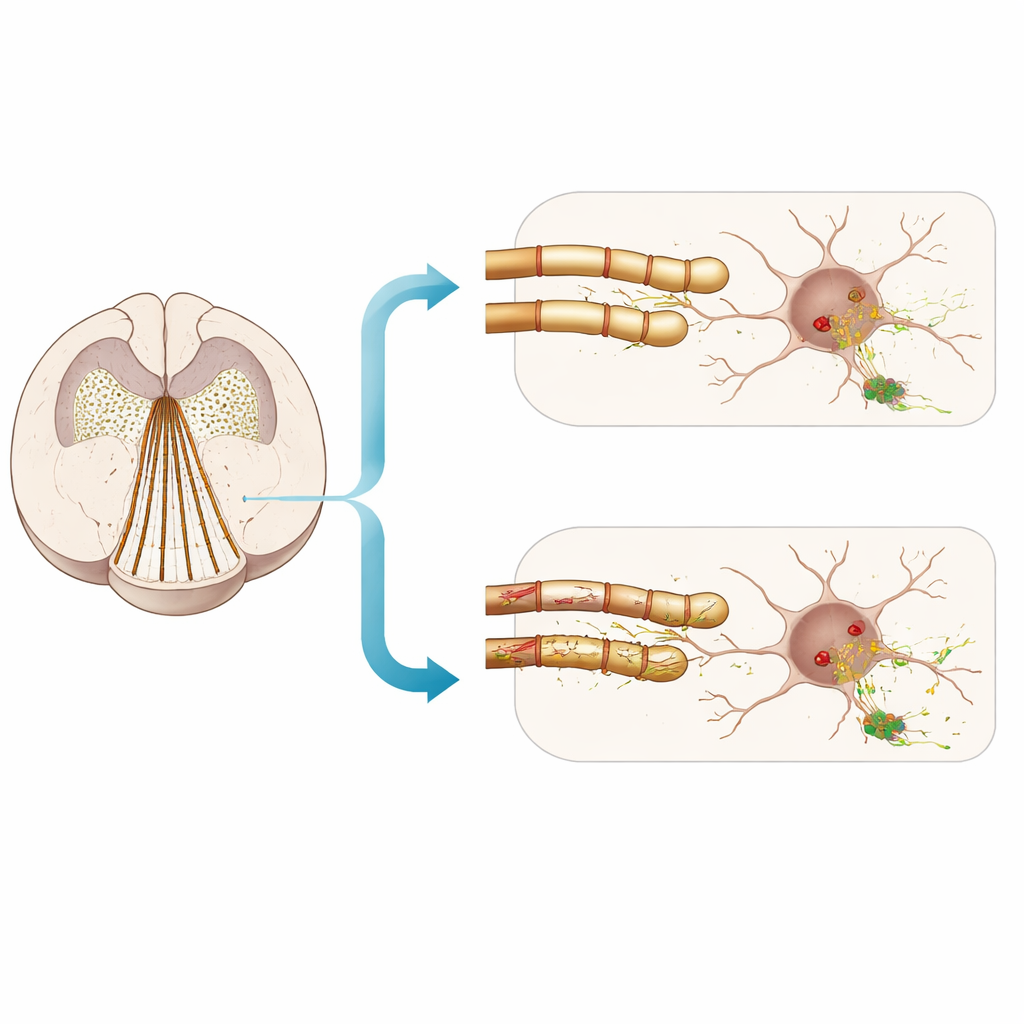
对理解风险的意义
综合来看,这项工作支持一种更为细致的观点。在患有路易体疾病的男性与纤维种子诱导的小鼠中,较弱的髓鞘标志常与更重的α‑突触核蛋白负荷并存,尤以边缘区域为甚。但当研究者有意损伤髓鞘时,只观察到早期病理的轻微、不一致加剧,且在所研究的时间范围内没有强有力的证据显示额外的神经元丧失或显著的行为衰退。对普通读者而言,结论是:髓鞘健康是病理形成的一部分,但并非全部——仅仅剥夺神经纤维的绝缘并不能自动复制帕金森相关疾病中观察到的选择性易损性。其他易受累通路的特征——例如极细的轴突、密集的突触分支和高能量需求——可能与髓鞘状况相互作用,共同决定有害蛋白聚集何时何地出现。
引用: Clark, R.N., Landes, R.E., Abbas, M. et al. Testing an inverse link between limbic alpha-synucleinopathy and myelin markers in mice and humans. npj Parkinsons Dis. 12, 77 (2026). https://doi.org/10.1038/s41531-026-01278-y
关键词: 帕金森病, 路易体相关疾病, 髓鞘, α‑突触核蛋白, 边缘系统