Clear Sky Science · pl
Testowanie odwrotnego związku między limbiczną alfa-synukleinopatią a markerami mieliny u myszy i ludzi
Dlaczego to ma znaczenie dla zdrowia mózgu
Choroba Parkinsona i pokrewne schorzenia „z ciałami Lewy’ego” kojarzą się głównie z problemami ruchowymi, ale obejmują także subtelne zmiany w okablowaniu mózgu na długo przed pojawieniem się objawów. Badanie stawia pozornie proste pytanie: czy niektóre szczególnie wrażliwe regiony mózgu są mocniej dotknięte w tych chorobach dlatego, że ich włókna nerwowe są słabo izolowane przez mielinę — tłuszczową osłonkę ułatwiającą szybkie przewodzenie sygnałów? Łącząc próbki ludzkiego mózgu z eksperymentami na myszach, autorzy sprawdzają, czy mniejsza ilość mieliny rzeczywiście powoduje większe nagromadzenie szkodliwych skupisk białkowych obserwowanych w stanach przypominających Parkinsona.
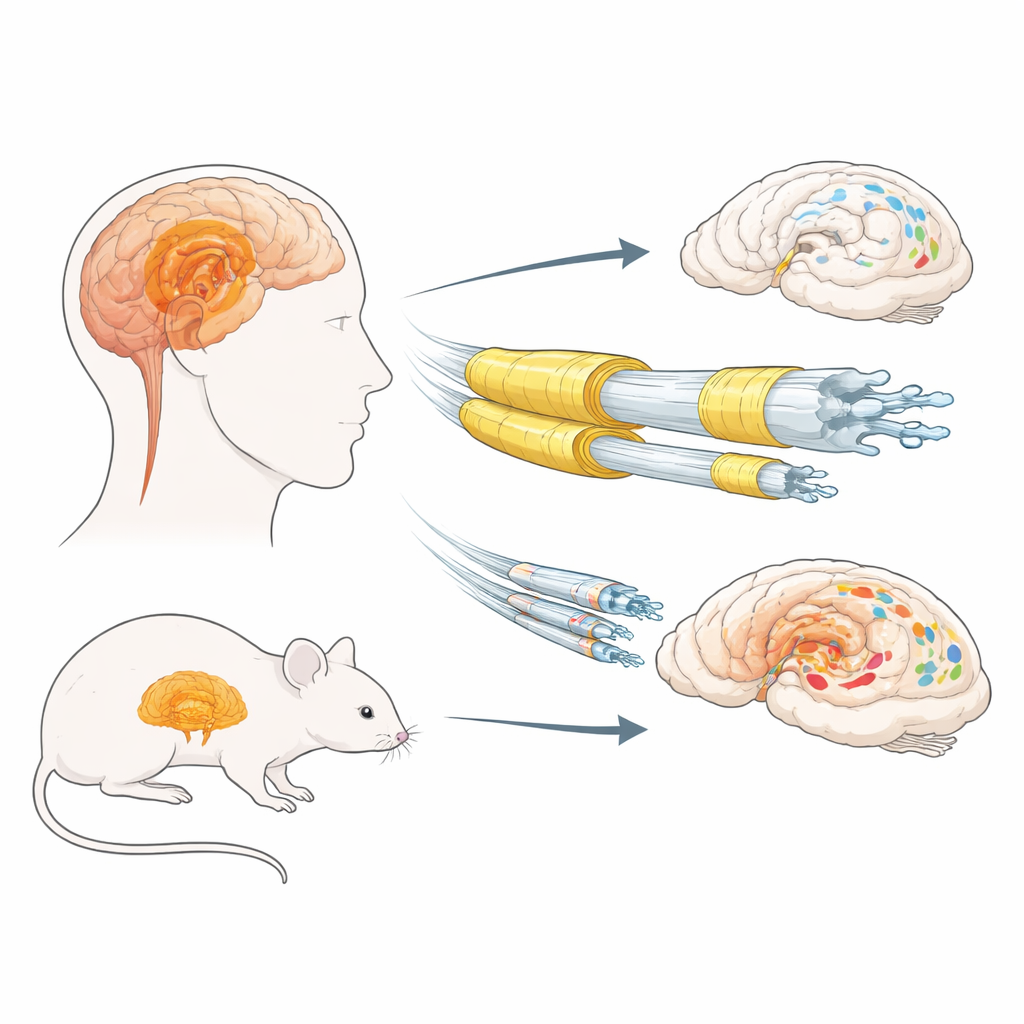
Izolacja mózgu i skupiska białkowe
W chorobach z ciałami Lewy’ego normalne białko mózgowe o nazwie alfa‑synukleina może nieprawidłowo się fałdować i gromadzić w komórkach nerwowych, tworząc grudki zwane ciałami Lewy’ego i wtrętami Lewy’ego. Wcześniejsze prace sugerowały, że długie, cienkie włókna o słabej mielinizacji mogą być szczególnie narażone. Mielinę wytwarzają komórki podporowe zwane oligodendrocytami i zawiera ona kluczowe białka strukturalne, w tym białko zasadowe mieliny (MBP) i proteolipid proteinę (PLP). Autorzy najpierw zbadali tkanki pośmiertne z opuszki węchowej i ciała migdałowatego — regionów limbicznych ważnych dla węchu i emocji — pochodzące od mężczyzn i kobiet z chorobą z ciałami Lewy’ego i bez niej. Mierzyli kilka markerów mieliny i porównywali je z poziomami nierozpuszczalnej, silnie zmodyfikowanej (hiperfosforylowanej) alfa‑synukleiny.
Wzorzec związany z płcią w tkance limbicznej ludzi
Dane ludzkie ujawniły uderzający, specyficzny dla płci wzorzec. W ciele migdałowatym mężczyzn z chorobą z ciałami Lewy’ego wyższe ilości nierozpuszczalnej, hiperfosforylowanej alfa‑synukleiny wiązały się z niższymi poziomami określonej formy PLP (izoformy 20 kilodaltonów), a pojawiały się także sygnały, że inne geny związane z mieliną były nieco obniżone. Ten odwrotny związek nie występował u kobiet. Wyniki sugerują, że przynajmniej u mężczyzn poważniejsza patologia typu Lewy’ego w ciele migdałowatym często towarzyszy słabszym markom mieliny. Są to jednak korelacje z tkanek ze stadium końcowego: nie mówią nam, czy utrata mieliny pogarsza patologię alfa‑synukleiny, czy też zmiany patologiczne stopniowo uszkadzają mielinę.
Wystawienie mieliny na próbę u myszy
Aby wyjść poza korelacje, zespół zwrócił się do modeli mysich pozwalających eksperymentalnie zaburzać mielinizację. Wstrzyknęli do rejonów węchowo‑limbiczych mózgu myszy wstępnie utworzone fibryle alfa‑synukleiny — maleńkie zarodniki, które wywołują agregaty podobne do Lewy’ego. Część myszy karmiono kuprizonem, związkiem wiążącym miedź, który zaburza mielinę i powoduje utratę masy ciała; inne miały genetyczną mutację „shiverer”, redukującą o połowę produkcję MBP. Idea była prosta: jeśli słaba mielina rzeczywiście zwiększa wrażliwość neuronów, te manipulacje powinny znacząco nasilić rozprzestrzenianie się grudek alfa‑synukleiny, uszkodzenia komórek nerwowych i zaburzenia behawioralne.
Uszkodzenie mieliny daje jedynie umiarkowany efekt
Rezultaty okazały się bardziej stonowane niż oczekiwano. Kuprizon wyraźnie zmniejszył kluczowe białka mieliny i zmienił strukturę istoty białej u samców myszy, potwierdzając, że izolacja została naruszona. Jednak podczas gdy wstrzyknięcia fibryli niezawodnie wywoływały wtręty podobne do Lewy’ego w obszarach istoty szarej, kuprizon jedynie nieznacznie zwiększył odsetek nierozpuszczalnej alfa‑synukleiny hiperfosforylowanej w jednym miejscu (seryna‑129). Całkowite ilości nierozpuszczalnej alfa‑synukleiny, wskaźniki zdrowia neuronów oraz szereg testów pamięci, eksploracji i węchu nie pogorszyły się znacząco po uszkodzeniu mieliny. Podobnie myszy z mutacją shiverer — pomimo cieńszej mieliny — nie wykazały wyraźnego, systematycznego wzrostu patologii limbicznej alfa‑synukleiny ani deficytów behawioralnych w porównaniu z normatywnymi rodzeństwem, poza niewielkim wzrostem średniego rozmiaru agregatów białkowych.
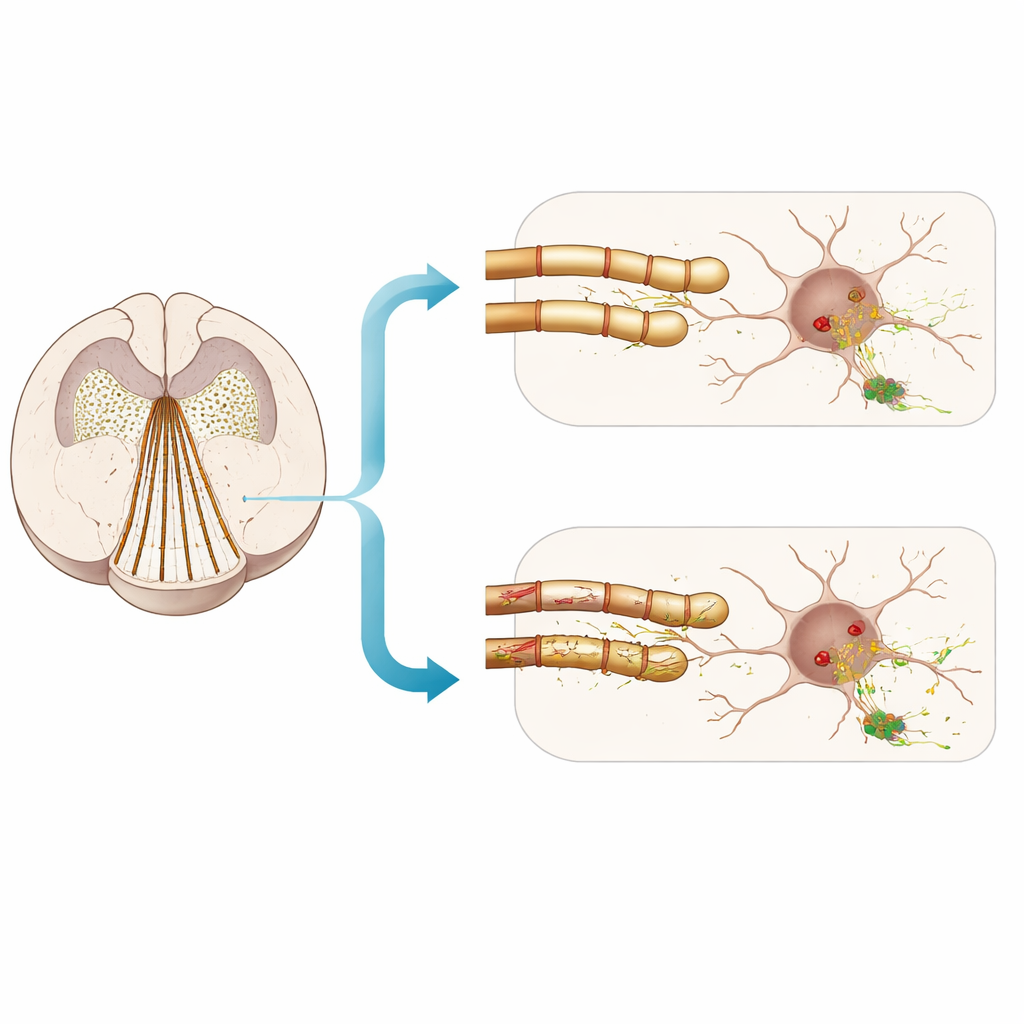
Co to oznacza dla rozumienia ryzyka
Podsumowując, praca wspiera zniuansowany pogląd. Zarówno u mężczyzn z chorobą z ciałami Lewy’ego, jak i u myszy zaszczepionych fibrylami, słabsze markery mieliny często towarzyszą większym obciążeniom alfa‑synukleiną, szczególnie w obszarach limbicznych. Jednak gdy badacze celowo uszkodzili mielinę, zaobserwowali jedynie umiarkowane, niespójne nasilanie wczesnej patologii i brak mocnych dowodów na dodatek utraty komórek nerwowych czy znaczącego pogorszenia zachowania w badanych przedziałach czasowych. Dla czytelnika niezaawansowanego w temacie wniosek jest taki, że stan mieliny jest istotną częścią układanki, ale nie wyjaśnia wszystkiego: samo pozbawienie izolacji włókien nerwowych nie odtwarza automatycznie wybiórczej wrażliwości obserwowanej w schorzeniach związanych z Parkinsonem. Inne cechy narażonych szlaków — takie jak bardzo cienkie aksony, gęste rozgałęzienie synaps i wysokie zapotrzebowanie energetyczne — mogą wchodzić w interakcje ze stanem mieliny, kształtując miejsce i czas pojawiania się szkodliwych skupisk białkowych.
Cytowanie: Clark, R.N., Landes, R.E., Abbas, M. et al. Testing an inverse link between limbic alpha-synucleinopathy and myelin markers in mice and humans. npj Parkinsons Dis. 12, 77 (2026). https://doi.org/10.1038/s41531-026-01278-y
Słowa kluczowe: choroba Parkinsona, choroby z ciałami Lewy’ego, mielina, alfa-synukleina, układ limbiczny