Clear Sky Science · es
Poniendo a prueba un vínculo inverso entre la alfa-sinucleinopatía límbica y marcadores de la mielina en ratones y humanos
Por qué esto importa para la salud cerebral
La enfermedad de Parkinson y los trastornos relacionados con los “cuerpos de Lewy” son conocidos por sus problemas de movimiento, pero también implican cambios sutiles en la conectividad cerebral mucho antes de que aparezcan los síntomas. Este estudio plantea una pregunta aparentemente simple: ¿ciertas regiones cerebrales vulnerables se ven muy afectadas en estas enfermedades porque sus fibras nerviosas están pobremente aisladas por la mielina, el recubrimiento graso que facilita la transmisión rápida de señales? Combinando muestras cerebrales humanas con experimentos en ratones, los investigadores comprueban si tener menos mielina realmente provoca más de los agregados proteicos dañinos observados en condiciones similares al Parkinson.
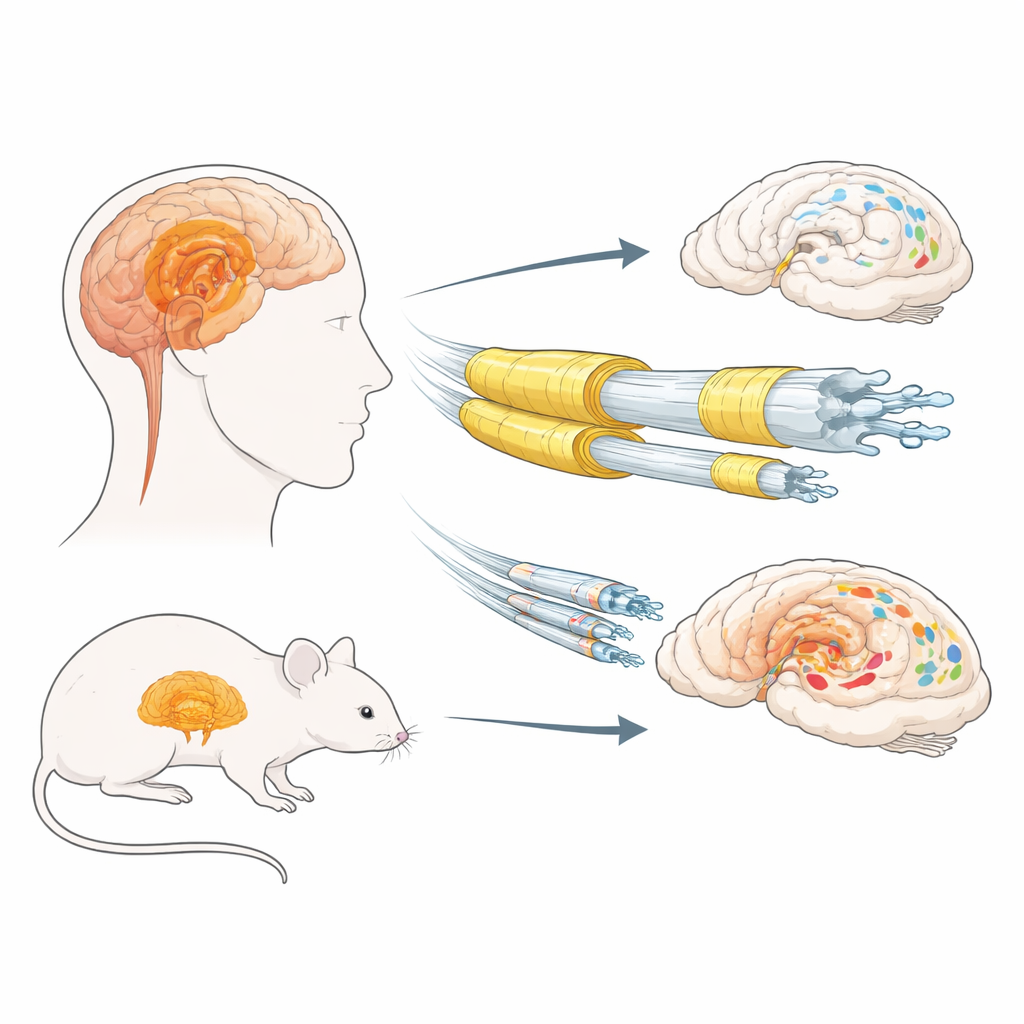
El aislamiento cerebral y los agregados proteicos
En los trastornos por cuerpos de Lewy, una proteína cerebral normal llamada alfa‑sinucleína puede plegarse mal y acumularse dentro de las neuronas, formando agregados denominados cuerpos y neuritas de Lewy. Trabajos previos sugerían que las fibras nerviosas largas, delgadas y pobremente mielinizadas podrían ser especialmente vulnerables. La mielina la producen células de soporte llamadas oligodendrocitos y contiene proteínas estructurales clave, entre ellas la proteína basica de la mielina (MBP) y la proteína proteolípida (PLP). Los autores examinaron primero tejido postmortem del bulbo olfatorio y la amígdala —regiones límbicas importantes para el olfato y la emoción— de hombres y mujeres con y sin enfermedad por cuerpos de Lewy. Midieron varios marcadores de mielina y los compararon con los niveles de alfa‑sinucleína insoluble, altamente modificada (hiperfosforilada).
Un patrón ligado al sexo en tejido límbico humano
Los datos humanos revelaron un patrón llamativo y específico por sexo. En la amígdala de hombres con enfermedad por cuerpos de Lewy, mayores cantidades de alfa‑sinucleína insoluble e hiperfosforilada se asociaron con niveles más bajos de una forma particular de PLP (el isoforma de 20 kilodaltons), y hubo indicios de que otros genes relacionados con la mielina también estaban algo reducidos. Esta relación inversa no se observó en mujeres. Los hallazgos sugieren que, al menos en hombres, una patología tipo Lewy más intensa en la amígdala suele acompañar firmas de mielina más débiles. Sin embargo, se trata de correlaciones en tejido en estadio terminal: no permiten saber si la pérdida de mielina empeora la patología de la alfa‑sinucleína, o si la propia patología va dañando progresivamente la mielina.
Poner la mielina a prueba en ratones
Para avanzar más allá de la correlación, el equipo recurrió a modelos de ratón que permiten alterar experimentalmente la mielina. Inyectaron fibrillas preformadas de alfa‑sinucleína —pequeñas semillas que desencadenan agregados tipo Lewy— en regiones olfato‑límbicas del cerebro del ratón. Algunos animales recibieron cuprizona en la dieta, un compuesto quelante del cobre que altera la mielina y provoca pérdida de peso; otros portaban una mutación genética “shiverer” que reduce a la mitad la producción de MBP. La idea era simple: si la pobre mielina realmente hace a las neuronas más vulnerables, estas manipulaciones deberían amplificar de forma notable la propagación de los agregados de alfa‑sinucleína, el daño neuronal y los problemas conductuales.
El daño a la mielina apenas acelera el proceso
Los resultados fueron más moderados de lo esperado. La cuprizona redujo claramente proteínas clave de la mielina y alteró la estructura de la materia blanca en ratones machos, confirmando que el aislamiento se vio comprometido. No obstante, aunque las inyecciones de fibrillas produjeron de forma fiable inclusiones tipo Lewy en regiones de materia gris, la cuprizona solo aumentó ligeramente la fracción de alfa‑sinucleína insoluble que estaba hiperfosforilada en un sitio (serina‑129). Las cantidades totales de alfa‑sinucleína insoluble, las medidas de salud neuronal y una batería de pruebas de memoria, exploración y olfato no empeoraron de manera consistente por el insulto a la mielina. De forma similar, los ratones con la mutación shiverer —a pesar de tener mielina más fina— no mostraron incrementos claros y sistemáticos en la patología límbica de la alfa‑sinucleína ni en déficits conductuales en comparación con sus camadas normales, aparte de un pequeño aumento en el tamaño medio de los agregados proteicos.
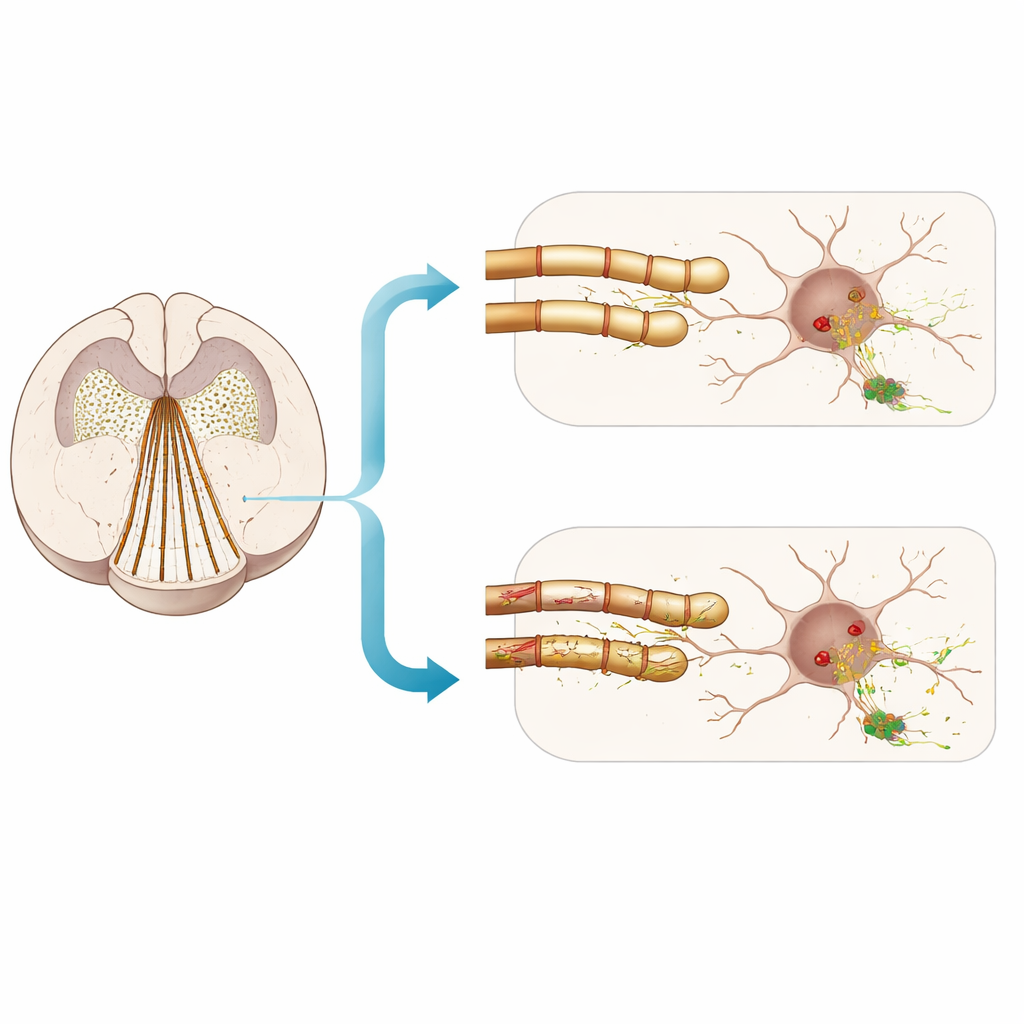
Qué significa esto para entender el riesgo
En conjunto, el trabajo respalda una visión matizada. Tanto en hombres con enfermedad por cuerpos de Lewy como en ratones sembrados con fibrillas, marcadores de mielina más débiles suelen acompañar cargas mayores de alfa‑sinucleína, especialmente en zonas límbicas. Pero cuando los investigadores dañaron deliberadamente la mielina, observaron solo una agravación modesta e inconsistente de la patología temprana y no hallaron pruebas sólidas de pérdida neuronal añadida ni de un deterioro conductual importante en los intervalos temporales estudiados. Para un lector general, la conclusión es que la salud de la mielina forma parte de la historia, pero no la explica por completo: simplemente quitar el aislamiento a las fibras nerviosas no reproduce de forma automática la vulnerabilidad selectiva observada en las condiciones relacionadas con el Parkinson. Otras características de las vías en riesgo —como axones muy finos, un denso ramificado de sinapsis y altas demandas energéticas— pueden interactuar con el estado de la mielina para determinar dónde y cuándo emergen los agregados proteicos dañinos.
Cita: Clark, R.N., Landes, R.E., Abbas, M. et al. Testing an inverse link between limbic alpha-synucleinopathy and myelin markers in mice and humans. npj Parkinsons Dis. 12, 77 (2026). https://doi.org/10.1038/s41531-026-01278-y
Palabras clave: Enfermedad de Parkinson, Trastornos por cuerpos de Lewy, mielina, alfa-sinucleína, sistema límbico