Clear Sky Science · nl
Het testen van een omgekeerde relatie tussen limbische alpha‑synucleinopathie en myelinekenmerken bij muizen en mensen
Waarom dit van belang is voor hersengezondheid
De ziekte van Parkinson en verwante “Lewy‑lichaam” aandoeningen staan vooral bekend om bewegingsproblemen, maar ze gaan ook gepaard met subtiele veranderingen in de hersenbedrading, lang voordat symptomen zichtbaar worden. Deze studie stelt een schijnbaar eenvoudige vraag: worden bepaalde kwetsbare hersengebieden in deze ziekten hard getroffen omdat hun zenuwvezels slecht geïsoleerd zijn door myeline, de vette bekleding die signalen helpt versnellen? Door menselijke hersenmonsters te combineren met muisexperimenten testen de onderzoekers of minder myeline daadwerkelijk meer van de schadelijke eiwitklonters veroorzaakt die bij Parkinson‑achtige aandoeningen worden gezien.
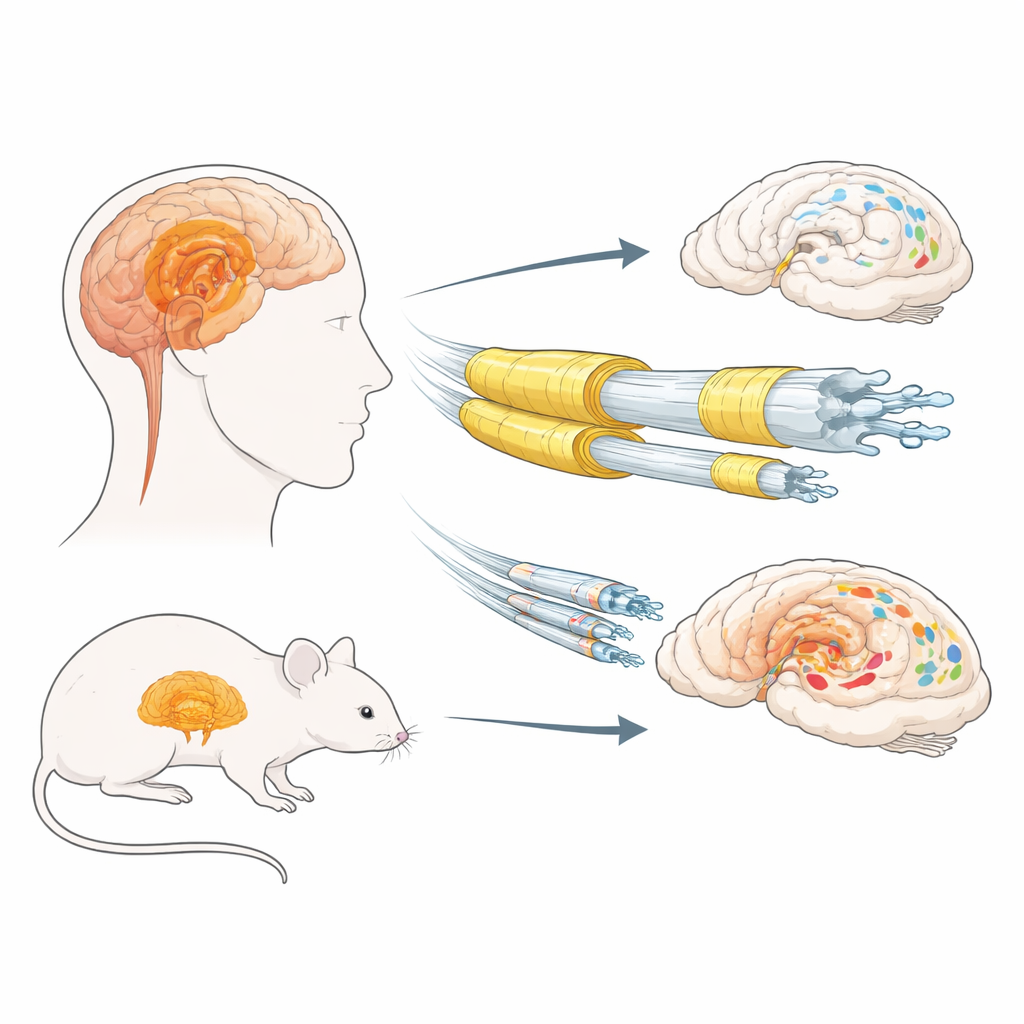
De isolatie van de hersenen en eiwitklonters
Bij Lewy‑lichaam aandoeningen kan een normaal herseneiwit, alpha‑synucleïne, fout vouwen en zich ophopen in zenuwcellen, waarbij klonters ontstaan die Lewy‑lichamen en Lewy‑neurieten worden genoemd. Eerder werk wees erop dat lange, dunne, slecht gemyleiniseerde zenuwvezels mogelijk extra kwetsbaar zijn. Myeline wordt gevormd door ondersteunende cellen, oligodendrocyten, en bevat belangrijke structurele eiwitten, waaronder myelinebasicproteïne (MBP) en proteolipide‑proteïne (PLP). De auteurs onderzochten eerst postmortaal weefsel van de reukbol en amygdala — limbische gebieden die belangrijk zijn voor geur en emotie — van mannen en vrouwen met en zonder Lewy‑lichaam ziekte. Ze maten verschillende myeline‑markers en vergeleken die met niveaus van onoplosbare, sterk gemodificeerde (hypergefosforyleerde) alpha‑synucleïne.
Een aan geslacht gekoppeld patroon in menselijk limbisch weefsel
De menselijke gegevens toonden een opvallend geslachtsspecifiek patroon. In de amygdala van mannen met Lewy‑lichaam ziekte waren hogere hoeveelheden onoplosbare, hypergefosforyleerde alpha‑synucleïne gekoppeld aan lagere niveaus van een specifieke PLP‑vorm (het 20 kilodalton isoform), en er waren aanwijzingen dat ook andere myelinegerelateerde genen enigszins verlaagd waren. Deze omgekeerde relatie werd niet gezien bij vrouwen. De bevindingen suggereren dat, althans bij mannen, ernstigere Lewy‑achtige pathologie in de amygdala vaak samengaat met zwakkere myelinesignaturen. Dit zijn echter correlaties uit eind‑stadium weefsel: ze kunnen niet aantonen of myelineverlies de alpha‑synucleïnepathologie verergert, of dat de pathologie geleidelijk myeline beschadigt.
Myeline op de proef stellen bij muizen
Om verder te komen dan correlatie wendde het team zich tot muismodellen die experimentele verstoring van myeline mogelijk maken. Ze injecteerden vooraf gevormde fibrillen van alpha‑synucleïne — kleine zaailingen die Lewy‑achtige aggregaten opwekken — in reuk‑limbische gebieden van de muizenhersenen. Sommige muizen kregen cuprizone, een koperbindende verbinding die myeline verstoort en gewichtsverlies veroorzaakt; andere muizen droegen een genetische “shiverer” mutatie die de productie van MBP halveert. Het idee was eenvoudig: als slechte myeline neuronen echt kwetsbaarder maakt, zouden deze manipulaties de verspreiding van alpha‑synucleïneklonten, zenuwcelbeschadiging en gedragsproblemen drastisch moeten versterken.
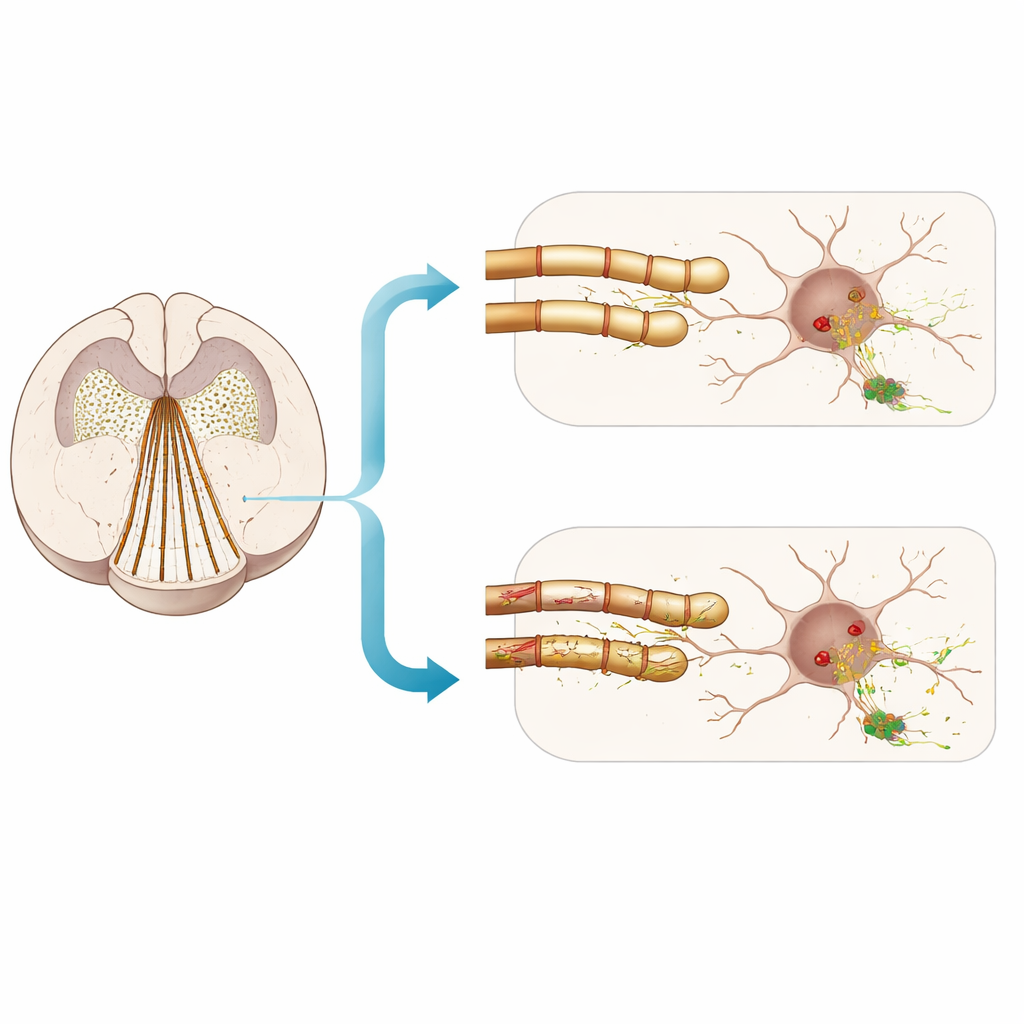
Myelinebeschadiging geeft slechts een bescheiden duwtje
De resultaten waren minder uitgesproken dan verwacht. Cuprizone verminderde duidelijk belangrijke myelineeiwitten en veranderde de witte‑stofstructuur bij mannelijke muizen, wat bevestigt dat de isolatie werd aangetast. Toch, terwijl fibrilinjecties betrouwbaar Lewy‑achtige inclusies in grijze‑stofgebieden produceerden, verhoogde cuprizone slechts licht het aandeel onoplosbare alpha‑synucleïne dat op één plaats (serine‑129) hypergefosforyleerd was. De totale hoeveelheden onoplosbare alpha‑synucleïne, maten van neuronale gezondheid en een reeks geheugen‑, verkennings‑ en geurtesten werden niet sterk verslechterd door de myelinebeschadiging. Evenzo vertoonden muizen met de shiverer‑mutatie — ondanks dunnere myeline — geen duidelijke, systematische toename in limbische alpha‑synucleïnepathologie of in gedragsdeficits vergeleken met normale nestgenoten, afgezien van een kleine toename in de gemiddelde grootte van eiwitaggregaten.
Wat dit betekent voor het begrip van risico
Gezamenlijk ondersteunen de bevindingen een genuanceerd beeld. Zowel bij mannen met Lewy‑lichaam ziekte als in fibril‑geïnjecteerde muizen gaan zwakkere myeline‑markers vaak samen met zwaardere alpha‑synucleïnelasten, vooral in limbische gebieden. Maar wanneer de onderzoekers myeline opzettelijk beschadigden, zagen ze slechts een bescheiden, inconsistent verergering van vroege pathologie en geen sterk bewijs voor extra zenuwcelverlies of grote gedragsachteruitgang binnen de onderzochte tijdsbestekken. Voor de algemene lezer is de conclusie dat myelinegezondheid deel uitmaakt van het verhaal, maar niet het hele verhaal: het simpelweg wegnemen van isolatie van zenuwvezels reproduceert niet automatisch de selectieve kwetsbaarheid die bij Parkinson‑verwante aandoeningen wordt gezien. Andere kenmerken van risicopaden — zoals zeer fijne axonen, dichte vertakking van synapsen en hoge energiebehoefte — kunnen in wisselwerking met de myelinestatus bepalen waar en wanneer schadelijke eiwitklonters ontstaan.
Bronvermelding: Clark, R.N., Landes, R.E., Abbas, M. et al. Testing an inverse link between limbic alpha-synucleinopathy and myelin markers in mice and humans. npj Parkinsons Dis. 12, 77 (2026). https://doi.org/10.1038/s41531-026-01278-y
Trefwoorden: Ziekte van Parkinson, Lewy‑lichaam aandoeningen, myeline, alpha‑synucleïne, limbisch systeem