Clear Sky Science · tr
Fareklerde ve insanlarda limbik alfa-sinükleinopati ile miyelin belirteçleri arasındaki ters ilişkiyi test etme
Beyin sağlığı için neden önemli
Parkinson hastalığı ve ilişkili "Lewy cisimciği" bozuklukları hareketle ilgili sorunlarla bilinir, ancak belirti ortaya çıkmadan uzun süre önce beyin bağlantılarında ince değişiklikler de içerir. Bu çalışma aldatıcı derecede basit bir soruyu soruyor: belirli hassas beyin bölgeleri bu hastalıklardan, sinyal iletimini hızlandıran yağlı kaplama olan miyelin tarafından kötü yalıtılmış olmaları nedeniyle mi ağır biçimde etkileniyor? İnsan beyin örneklerini fare deneyleriyle birleştirerek araştırmacılar, daha az miyelin olmasının gerçekten Parkinson benzeri durumlarda görülen zararlı protein kümelerinin artmasına yol açıp açmadığını test ediyor.
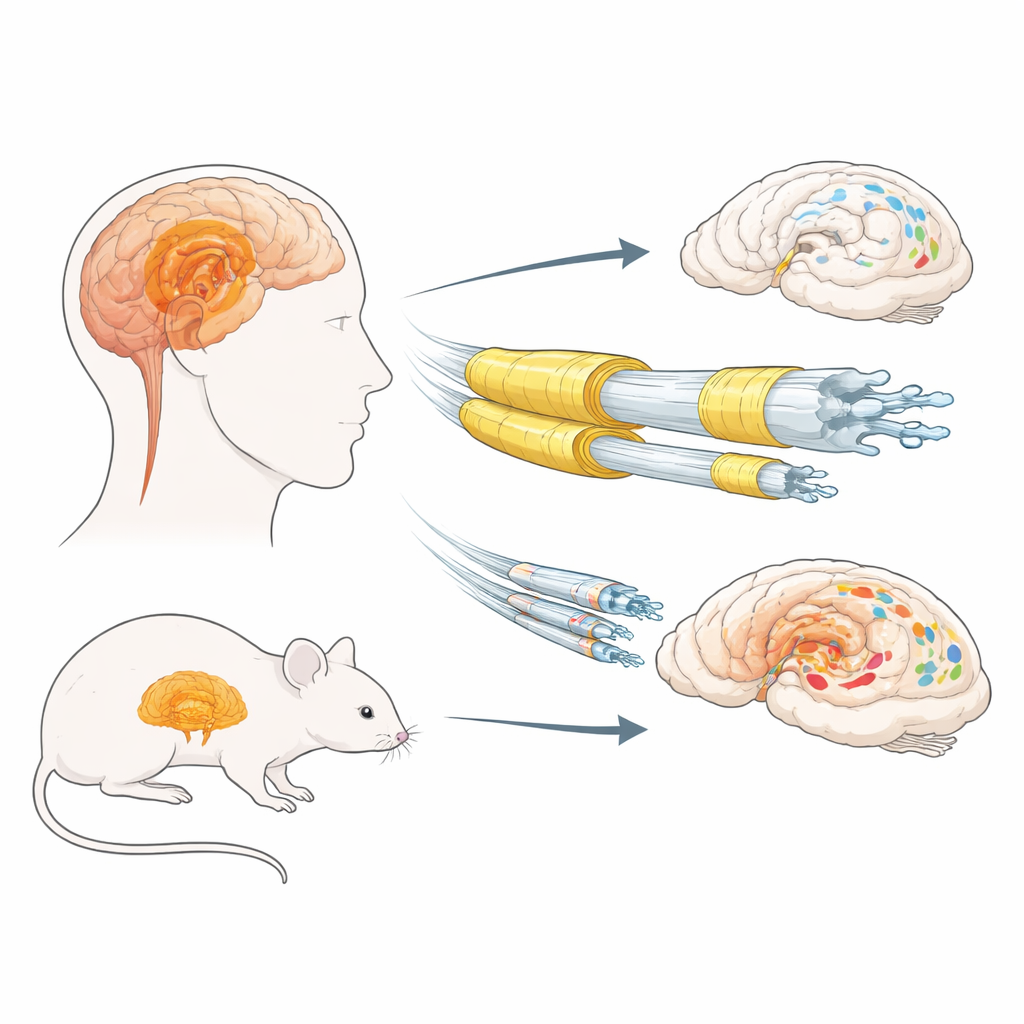
Beynin yalıtımı ve protein kümeleri
Lewy cisimciği bozukluklarında alfa‑sinüklein adı verilen normal bir beyin proteini hatalı katlanabilir ve sinir hücreleri içinde birikerek Lewy cisimcikleri ve Lewy neuritleri adı verilen kümeler oluşturabilir. Önceki çalışmalar, uzun, ince ve kötü miyelinlenmiş sinir liflerinin özellikle risk altında olabileceğini öne sürmüştü. Miyelin oligodendrosit adı verilen destek hücreleri tarafından üretilir ve miyelin temel protein (MBP) ile proteolipiddendir (PLP) gibi önemli yapısal proteinleri içerir. Yazarlar önce koku ve duygu için önemli limbik bölgeler olan olfaktör biberon (olfactory bulb) ve amigdaladan lewy cisimciği olan ve olmayan erkek ve kadınlardan alınmış otopsi dokularını incelediler. Birkaç miyelin belirtecini ölçtüler ve bunları çözünmez, yüksek oranda modifiye olmuş (hiperfosforile) alfa‑sinüklein düzeyleriyle karşılaştırdılar.
İnsan limbik dokusunda cinsiyete bağlı desen
İnsan verileri çarpıcı, cinsiyete özgü bir desen ortaya koydu. Lewy cisimciği hastalığı olan erkeklerin amigdalasında, çözünmez, hiperfosforile alfa‑sinüklein miktarının yüksek olması belirli bir PLP formunun (20 kilodalton izoformu) daha düşük seviyeleriyle bağlantılıydı ve diğer miyelinle ilişkili genlerin de biraz azalmış olabileceğine dair ipuçları vardı. Bu ters ilişki kadınlarda görülmedi. Bulgular, en azından erkeklerde amigdalada daha kötü Lewy tipi patolojinin daha zayıf miyelin imzalarıyla birlikte olma eğiliminde olduğunu öne sürüyor. Ancak bunlar son evre dokudan elde edilen korelasyonlar: miyelin kaybının alfa‑sinüklein patolojisini kötüleştirip kötüleştirmediğini ya da patolojinin zamanla miyeline zarar verip vermediğini söyleyemezler.
Farelerde miyelini teste tabi tutmak
Korelasyonun ötesine geçmek için ekip miyelinin deneysel olarak bozulmasına izin veren fare modellerine döndü. Araştırmacılar alfa‑sinüklein önceden oluşturulmuş fibrillerini — Lewy benzeri agregatleri tetikleyen küçük tohumlar — fare beyninin olfaktör‑limbik bölgelerine enjekte ettiler. Bazı farelere miyelini bozup hayvanlarda kilo kaybına neden olan bakır bağlayıcı bir bileşik olan kuprizon (cuprizone) verildi; diğerleri MBP üretimini yarıya indiren genetik "shiverer" mutasyonunu taşıyordu. Fikir basitti: eğer kötü miyelin gerçekten nöronları daha savunmasız kılıyorsa, bu müdahaleler alfa‑sinüklein kümelerinin yayılımını, sinir hücresi hasarını ve davranışsal sorunları dramatik şekilde artırmalıydı.
Miyelin hasarı yalnızca ılımlı bir etki verdi
Sonuçlar beklenenden daha ılımlıydı. Kuprizon erkek farelerde belirgin şekilde ana miyelin proteinlerini azalttı ve beyaz madde yapısını değiştirdi; bu, yalıtımın bozulduğunu doğruladı. Ancak fibril enjeksiyonları gri madde bölgelerinde güvenilir şekilde Lewy‑benzeri inklüzyonlar üretirken, kuprizon yalnızca çözünmez alfa‑sinükleinin bir yerinde (serin‑129) hiperfosforile olan fraksiyonunu biraz artırdı. Çözünmez alfa‑sinükleinin toplam miktarı, nöronal sağlık ölçümleri ve çeşitli hafıza, keşif ve koku testleri miyelin hasarıyla belirgin şekilde kötüleşmedi. Benzer şekilde, daha ince miyeline sahip olmalarına rağmen shiverer mutasyonlu fareler, normal kardeşlerine kıyasla limbik alfa‑sinüklein patolojisinde ya da davranışsal bozukluklarda açık, sistematik artış göstermedi; tek istisna protein agregatlarının ortalama boyutunda küçük bir artıştır.
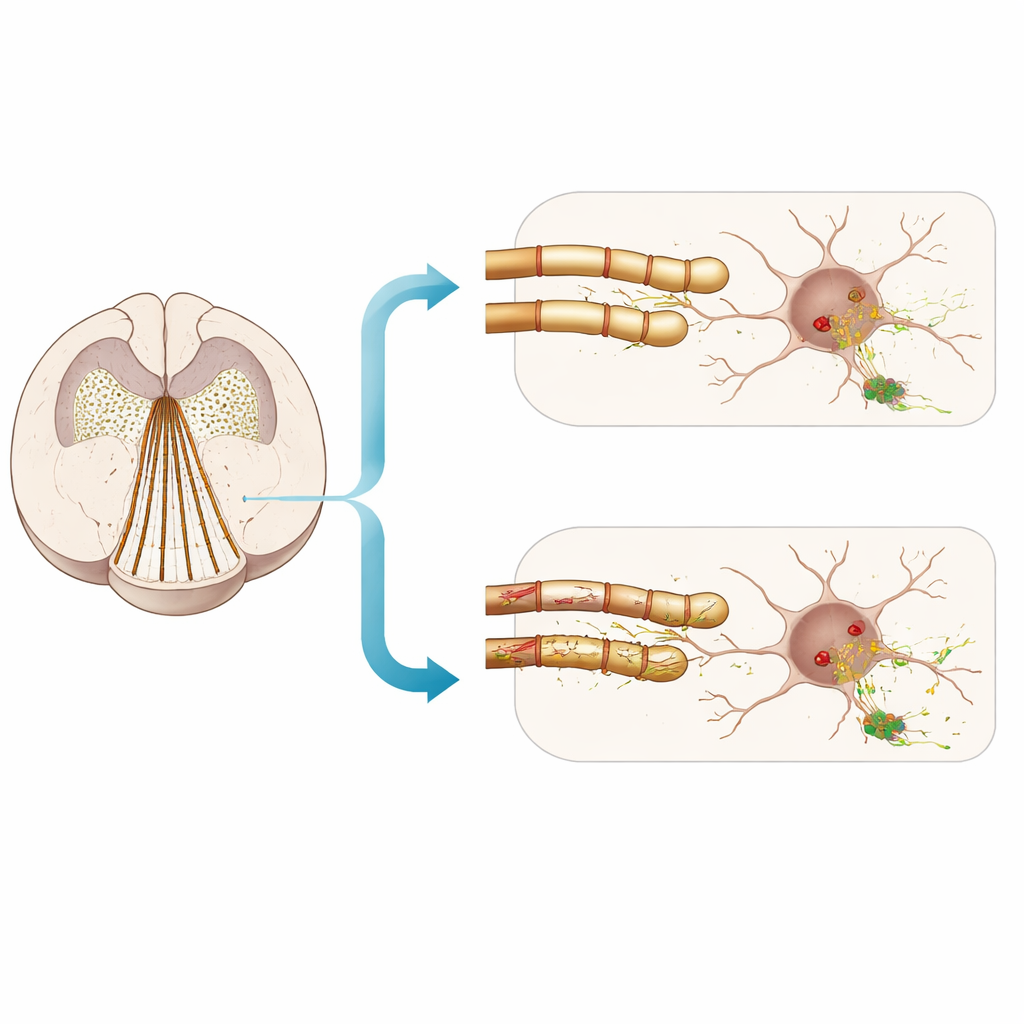
Riskin anlaşılması için bunun anlamı
Bir arada ele alındığında, çalışma nüanslı bir görüşü destekliyor. Hem Lewy cisimciği hastalığı olan erkeklerde hem de fibril‑tohumlanmış farelerde, özellikle limbik alanlarda, daha zayıf miyelin belirteçleri genellikle daha ağır alfa‑sinüklein yükleriyle birlikte görülüyor. Ancak araştırmacılar miyelini kasıtlı olarak zarar verdiğinde, erken patolojinin yalnızca ılımlı ve tutarsız biçimde kötüleşmesini gördüler ve çalışılan zaman dilimlerinde belirgin bir sinir hücresi kaybı ya da büyük davranış düşüşü kanıtı elde edemediler. Genel okuyucu için çıkarım şudur: miyelin sağlığı hikâyenin bir parçası, ama tümü değil — sinir liflerinden yalıtımı basitçe kaldırmak, otomatik olarak Parkinson ilişkili durumlarda görülen seçici duyarlılığı yeniden üretmiyor. Çok ince aksonlar, yoğun dallanan sinapslar ve yüksek enerji gereksinimleri gibi risk altındaki yolakların diğer özellikleri miyelin durumu ile etkileşime girerek zararlı protein kümelerinin nerede ve ne zaman ortaya çıkacağını şekillendirebilir.
Atıf: Clark, R.N., Landes, R.E., Abbas, M. et al. Testing an inverse link between limbic alpha-synucleinopathy and myelin markers in mice and humans. npj Parkinsons Dis. 12, 77 (2026). https://doi.org/10.1038/s41531-026-01278-y
Anahtar kelimeler: Parkinson hastalığı, Lewy cisimciği bozuklukları, miyelin, alfa-sinüklein, limbik sistem