Clear Sky Science · ru
Тестирование обратной связи между лимбальной альфа-синуклеинопатией и маркерами миелина у мышей и людей
Почему это важно для здоровья мозга
Болезнь Паркинсона и связанные с ней «тельца Леви» обычно ассоциируются с проблемами движений, но они также сопровождаются тонкими изменениями проводящих путей мозга задолго до появления явных симптомов. В этом исследовании задают на первый взгляд простой вопрос: поражаются ли определённые уязвимые области мозга в этих заболеваниях потому, что их нервные волокна слабо изолированы миелином — жирной оболочкой, которая ускоряет проведение сигналов? Объединив анализы человеческой ткани и эксперименты на мышах, авторы проверяют, вызывает ли меньшее количество миелина действительно больше скоплений вредного белка, характерных для состояний, похожих на болезнь Паркинсона.
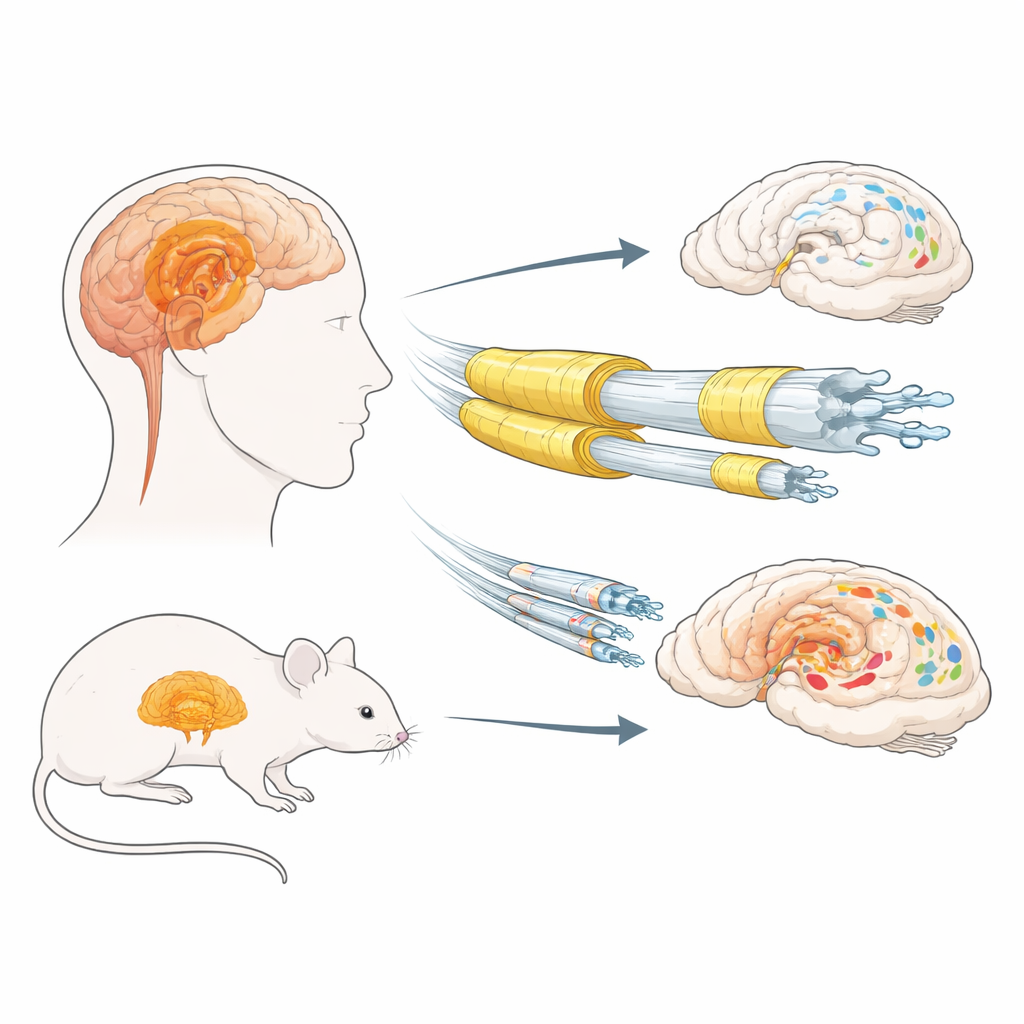
Изоляция мозга и белковые скопления
При заболеваниях с тельцами Леви нормальный белок мозга альфа‑синуклеин может неправильно сворачиваться и накапливаться внутри нейронов, формируя включения, называемые тельцами Леви и дендритными/аксональными включениями. Предыдущие работы предполагали, что длинные тонкие слабо миелинизированные волокна особенно уязвимы. Миелин вырабатывают вспомогательные клетки — олигодендроциты, и он содержит ключевые структурные белки, такие как миелиновый базовый белок (MBP) и протеолипидный белок (PLP). Авторы сначала исследовали посмертные образцы обонятельной луковицы и миндалины — лимбических областей, важных для обоняния и эмоций — у мужчин и женщин с болезнью с тельцами Леви и без неё. Они измеряли несколько маркеров миелина и сравнивали их с уровнями нерастворимого, сильно модифицированного (гиперфосфорилированного) альфа‑синуклеина.
Половой паттерн в лимбальной ткани человека
Данные у людей выявили поразительную, зависящую от пола закономерность. В миндалине у мужчин с болезнью с тельцами Леви большее количество нерастворимого, гиперфосфорилированного альфа‑синуклеина было связано с более низким уровнем определённой формы PLP (изоформа ~20 килодальтон), а также отмечались намёки на снижение экспрессии других генов, связанных с миелином. Такая обратная связь не наблюдалась у женщин. Эти результаты указывают, что по крайней мере у мужчин ухудшение патологии типа Леви в миндалине часто сопровождается слабее выраженными «миелиновыми подписями». Однако это корреляции в тканях терминальной стадии: они не могут сказать, вызывает ли потеря миелина усиление патологии альфа‑синуклеина или сама патология постепенно повреждает миелин.
Проверка роли миелина на мышах
Чтобы выйти за рамки корреляции, команда обратилась к моделям на мышах, где миелин можно экспериментально нарушать. Они вводили предварительно сформированные фибриллы альфа‑синуклеина — крошечные семена, вызывающие агрегирование, похожее на тельца Леви — в обонятельно‑лимбические области мозга мышей. Части животных кормили купризоном, соединением, связывающим медь, которое нарушает миелин и приводит к потере веса; другие несли генетическую мутацию «shiverer», которая сокращает продукцию MBP наполовину. Идея была проста: если плохой миелин действительно делает нейроны более уязвимыми, то такие вмешательства должны значительно усилить распространение агрегатов альфа‑синуклеина, повреждение нейронов и поведенческие нарушения.
Повреждение миелина даёт лишь умеренный эффект
Результаты оказались более сдержанными, чем ожидалось. Купризон ясно снижал ключевые миелиновые белки и изменял структуру белого вещества у самцов мышей, подтверждая нарушение изоляции. Тем не менее, хотя инъекции фибрилл стабильно вызывали включения, похожие на тельца Леви, в сером веществе, купризон лишь незначительно увеличивал долю нерастворимого альфа‑синуклеина, гиперфосфорилированного в одном сайте (серин‑129). Общие количества нерастворимого альфа‑синуклеина, показатели здоровья нейронов и ряд тестов на память, исследование и обоняние существенно не ухудшались после повреждения миелина. Аналогично, мыши с мутацией shiverer — несмотря на более тонкий миелин — не демонстрировали чётких систематических увеличений лимбальной патологии альфа‑синуклеина или поведенческих дефицитов по сравнению с нормальными крысятами из того же помёта, за исключением небольшого увеличения среднего размера белковых агрегатов.
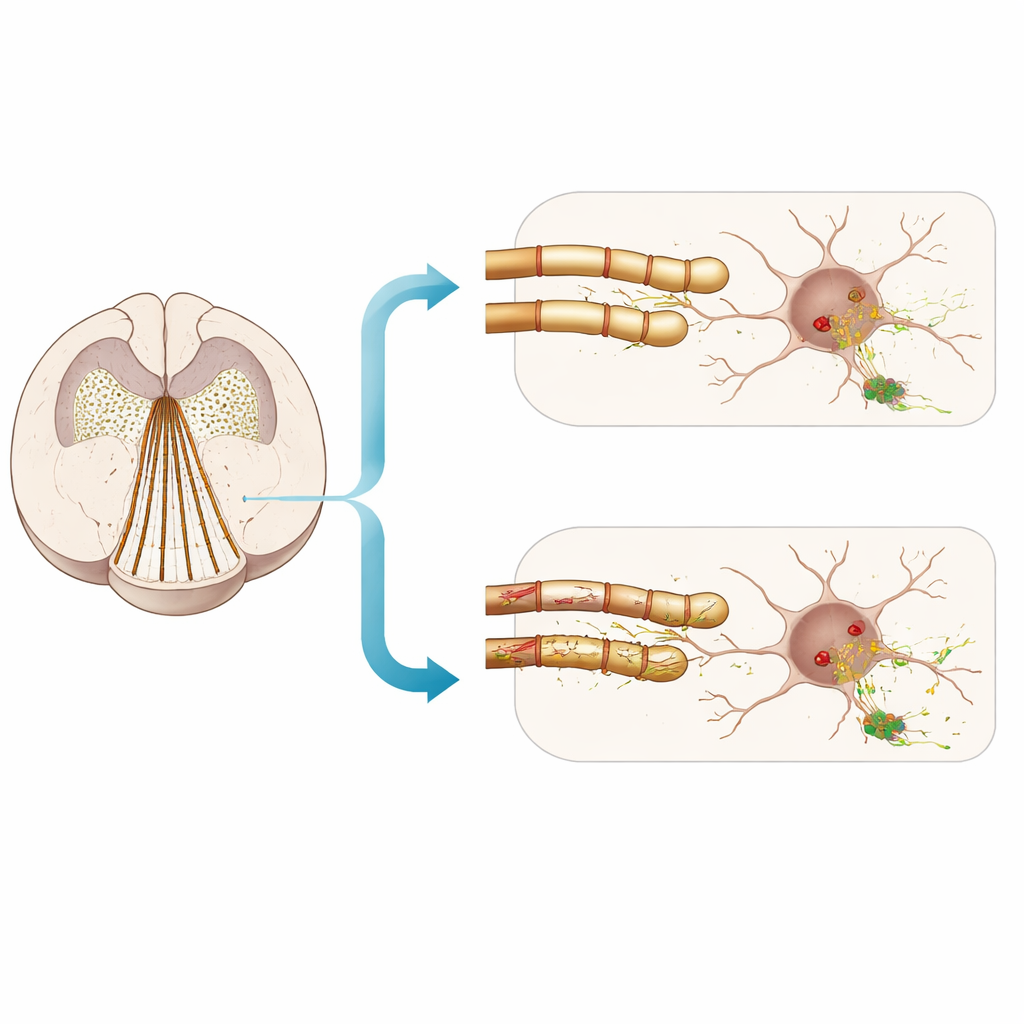
Что это значит для понимания факторов риска
В совокупности работа поддерживает нюансированный взгляд. И у мужчин с болезнью с тельцами Леви, и у мышей с посевом фибрилл более слабые миелиновые маркеры часто сопровождают большие нагрузки альфа‑синуклеина, особенно в лимбических областях. Но когда исследователи намеренно повреждали миелин, они наблюдали лишь умеренное, непоследовательное усиление ранней патологии и не получили убедительных данных о дополнительной потере нейронов или значительном поведенческом упадке в изучаемые сроки. Для широкого читателя вывод таков: состояние миелина — это часть истории, но не вся история: простое удаление изоляции с нервных волокон не воспроизводит самостоятельно избирательную уязвимость, наблюдаемую при состояниях, связанных с болезнью Паркинсона. Другие особенности уязвимых путей — например чрезвычайно тонкие аксоны, плотное ветвление синапсов и высокие энергетические требования — могут взаимодействовать со статусом миелина, определяя, где и когда возникают вредные белковые скопления.
Цитирование: Clark, R.N., Landes, R.E., Abbas, M. et al. Testing an inverse link between limbic alpha-synucleinopathy and myelin markers in mice and humans. npj Parkinsons Dis. 12, 77 (2026). https://doi.org/10.1038/s41531-026-01278-y
Ключевые слова: Болезнь Паркинсона, Болезни с тельцами Леви, миелин, альфа-синуклеин, лимбическая система