Clear Sky Science · zh
TBK1 限制 IRGQ 调控的自噬
细胞如何决定保留什么、丢弃什么
在每个细胞内部,一个繁忙的回收系统不断分拣磨损部件和错误折叠的蛋白,防止它们引发问题。本研究揭示了一个小的蛋白枢纽如何启动针对特定货物的细胞清理,以及另一种酶如何将该枢纽切换到关闭状态。理解这一开关有助于阐明细胞如何微调废物处理,对衰老、癌症、感染和免疫反应等领域具有重要意义。
细胞内的定向清理队
细胞并非随机降解其内容物。它们通过一种称为自噬的过程,将选定物质包裹在微小膜囊中并送入酸性隔室进行分解。专门的受体蛋白帮助挑选要打包的货物,并协助招募核心清理机器。近期鉴定出的蛋白 IRGQ 就是此类受体之一,能识别细胞表面某些版本的免疫展示分子。在这项工作中,作者表明 IRGQ 不只是一个标记货物的蛋白;它还组织自噬体形成的早期步骤。
连接货物与机器的蛋白枢纽
IRGQ 与一类称为 ATG8 的小适配蛋白家族相互作用,这些蛋白装饰着正在形成的自噬体膜,对构建这些回收囊至关重要。研究团队发现 IRGQ 带有两个独立的对接位点,可与不同的 ATG8 成员结合。其中一个位点对单一 ATG8 蛋白 GABARAPL2 显示出显著偏好。通过结构预测、蛋白质拉下实验和显微镜观察,研究者证明 IRGQ 与 GABARAPL2 一起形成一个枢纽,招募负责将 ATG8 蛋白附着到膜上的关键酶。当该枢纽存在时,细胞的 ATG8 附着增加,针对特定货物的自噬活性也增强,证实 IRGQ 积极促进选择性清理的起始,而不仅仅是为待降解材料打标签。
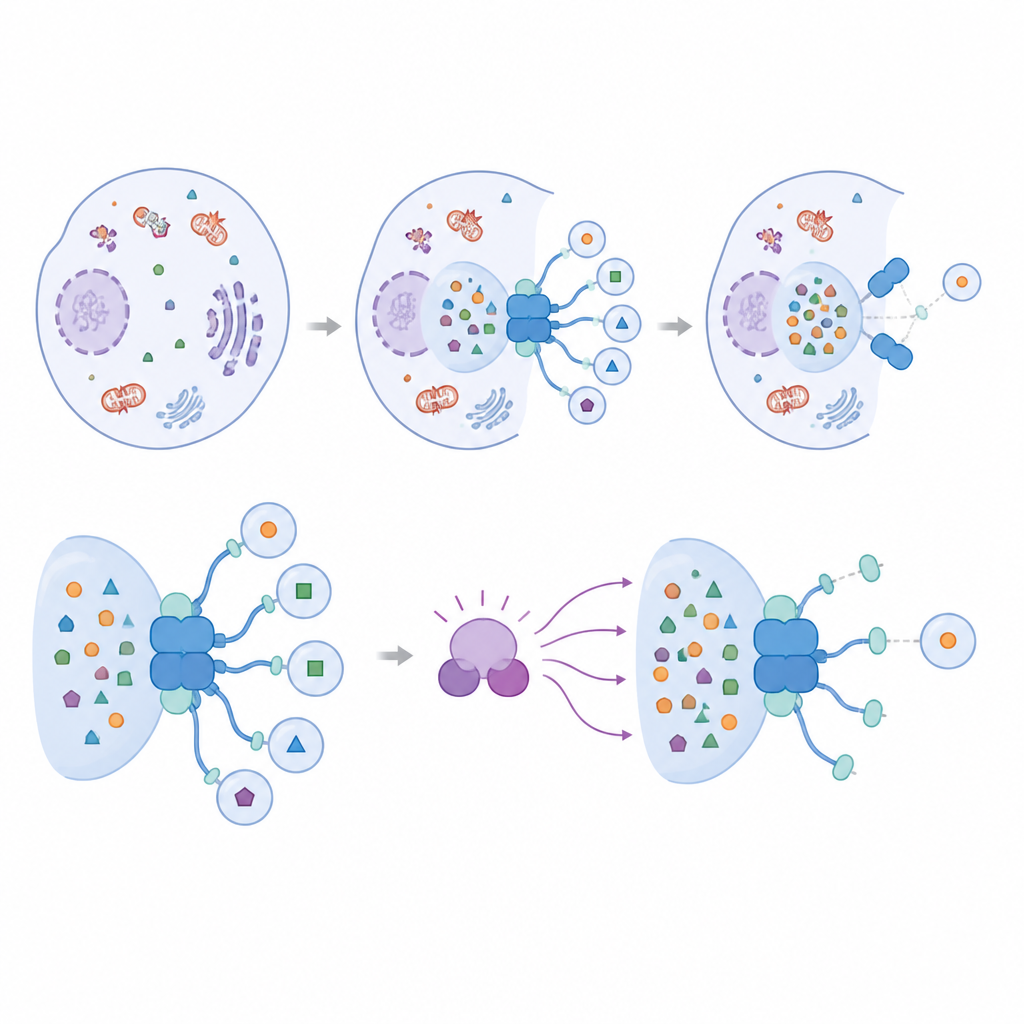
清理枢纽上的分子刹车
研究接着探讨这一强大起始枢纽如何被调控。焦点转向已知影响多种选择性自噬形式的酶 TBK1。作者显示 TBK1 直接在靠近 GABARAPL2 与 IRGQ 接触点的单个氨基酸上修饰 GABARAPL2。当该位点被改变以模拟永久修饰状态时,IRGQ 与 GABARAPL2 之间的结合明显减弱,复合体解体。高级建模和基于细胞的实验证实,这一变化并未广泛破坏 GABARAPL2 与其他结合伙伴的相互作用能力,而是特异性地使其与 IRGQ 及相关起始机器的连接不稳定。
对货物的选择性影响,而非全局回收
拆散 IRGQ–GABARAPL2 枢纽带来了出人意料的局部影响。细胞在饥饿时的散装自噬——即细胞的全局回收反应——在 GABARAPL2 的该修饰位点被改变时仍大体保持不变。然而,GABARAPL2 本身及 IRGQ 所携带货物(一部分主要组织相容性复合体 I 类分子)的运输明显受损。在携带磷酸模拟型 GABARAPL2 的细胞中,这些免疫分子在细胞表面积累,而未能到达溶酶体进行降解,近似于缺失 IRGQ 时的情况。相反,抑制 TBK1 活性会使更多这类货物被送往溶酶体,表明 TBK1 通常作用于抑制这一特定的自噬清除途径。
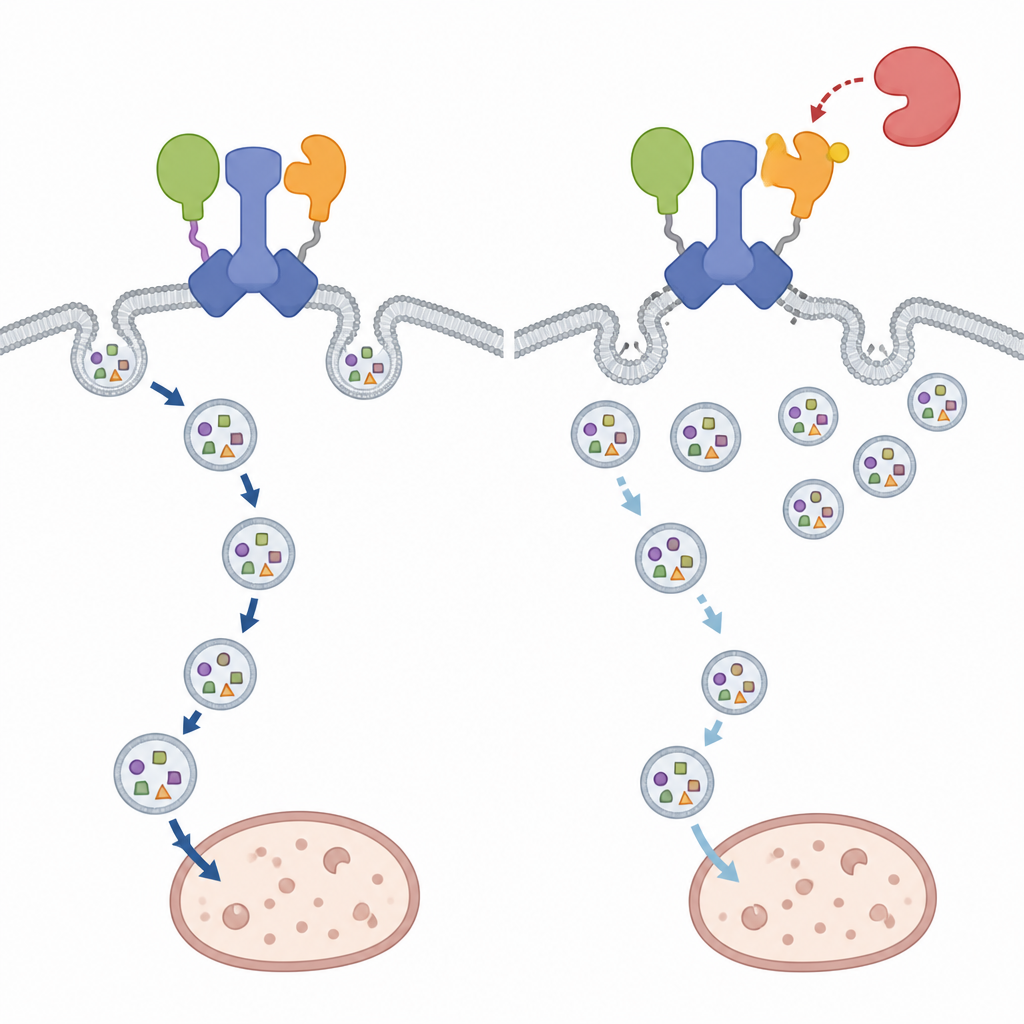
依赖情境的细胞回收停止信号
综合来看,研究发现 IRGQ 是将被选货物与自噬体形成早期步骤相连的核心组织者,而 TBK1 则是对这一路径施加情境依赖性刹车的因子。通过在恰当时刻修饰 GABARAPL2,TBK1 能够关闭 IRGQ 枢纽,而不会关闭细胞的全局回收系统。对非专业读者而言,这意味着细胞拥有一个精细调控的开关,能够打开或关闭特定的清理通路,从而在不同情境下影响免疫信号的展示及受损组分的清除方式。
引用: Gestal-Mato, U., Lascaux, P., Poveda-Cuevas, S.A. et al. TBK1 restricts IRGQ-mediated autophagy. Nat Commun 17, 4335 (2026). https://doi.org/10.1038/s41467-026-73005-3
关键词: 选择性自噬, IRGQ, TBK1, GABARAPL2, MHC I 类分子质量控制