Clear Sky Science · de
TBK1 schränkt IRGQ-vermittelte Autophagie ein
Wie Zellen entscheiden, was behalten und was weggeworfen wird
In jeder Zelle sortiert ein aktives Recycling‑System fortlaufend verschlissene Teile und fehlgefaltete Proteine aus, bevor sie Schaden anrichten. Diese Studie enthüllt, wie ein kleines Protein‑Zentrum die Reinigung für bestimmte Fracht startet und wie ein anderes Enzym dieses Zentrum in den Aus‑Zustand versetzen kann. Das Verständnis dieses Schalters erklärt, wie Zellen die Abfallbeseitigung feinabstimmen — mit Folgen für Altern, Krebs, Infektionen und Immunantworten.
Ein gezieltes Aufräumteam innerhalb der Zelle
Zellen verdauen ihre Inhalte nicht zufällig. Sie nutzen einen Prozess namens Autophagie, um ausgewähltes Material in winzige Membransäckchen einzupacken und in saure Kompartimente zur Zerlegung zu liefern. Spezialisierte Rezeptorproteine helfen zu bestimmen, welche Fracht verpackt wird, und rekrutieren die Kernmaschinerie der Reinigung. Das Protein IRGQ wurde kürzlich als ein solcher Rezeptor identifiziert, der bestimmte Varianten von Immun‑Darstellungs‑Molekülen an der Zelloberfläche erkennt. In dieser Arbeit zeigen die Autorinnen und Autoren, dass IRGQ mehr ist als ein bloßer Markierer der Fracht: Es organisiert auch die frühen Schritte der Bildung von Autophagosomen.
Ein Protein‑Zentrum, das Fracht und Maschinerie verbindet
IRGQ interagiert mit einer Familie kleiner Adapterproteine, bekannt als ATG8s, die die entstehende Autophagosomen‑Membran schmücken und für den Aufbau dieser Recycling‑Säcke unverzichtbar sind. Das Team fand heraus, dass IRGQ zwei separate Andockstellen trägt, die verschiedene ATG8‑Mitglieder binden können. Eine dieser Stellen zeigt eine auffällige Präferenz für ein einzelnes ATG8‑Protein namens GABARAPL2. Mithilfe von Strukturvorhersagen, Protein‑Pulldown‑Assays und Mikroskopie demonstrieren die Forschenden, dass IRGQ und GABARAPL2 gemeinsam ein Zentrum bilden, das Schlüsselenzyme heranführt, die ATG8‑Proteine an Membranen anheften. Ist dieses Zentrum vorhanden, zeigen Zellen erhöhte ATG8‑Anheftung und mehr autophagische Aktivität für spezifische Frachten, was bestätigt, dass IRGQ aktiv die Initiation selektiver Reinigung fördert und nicht nur Material zum Abtransport markiert.
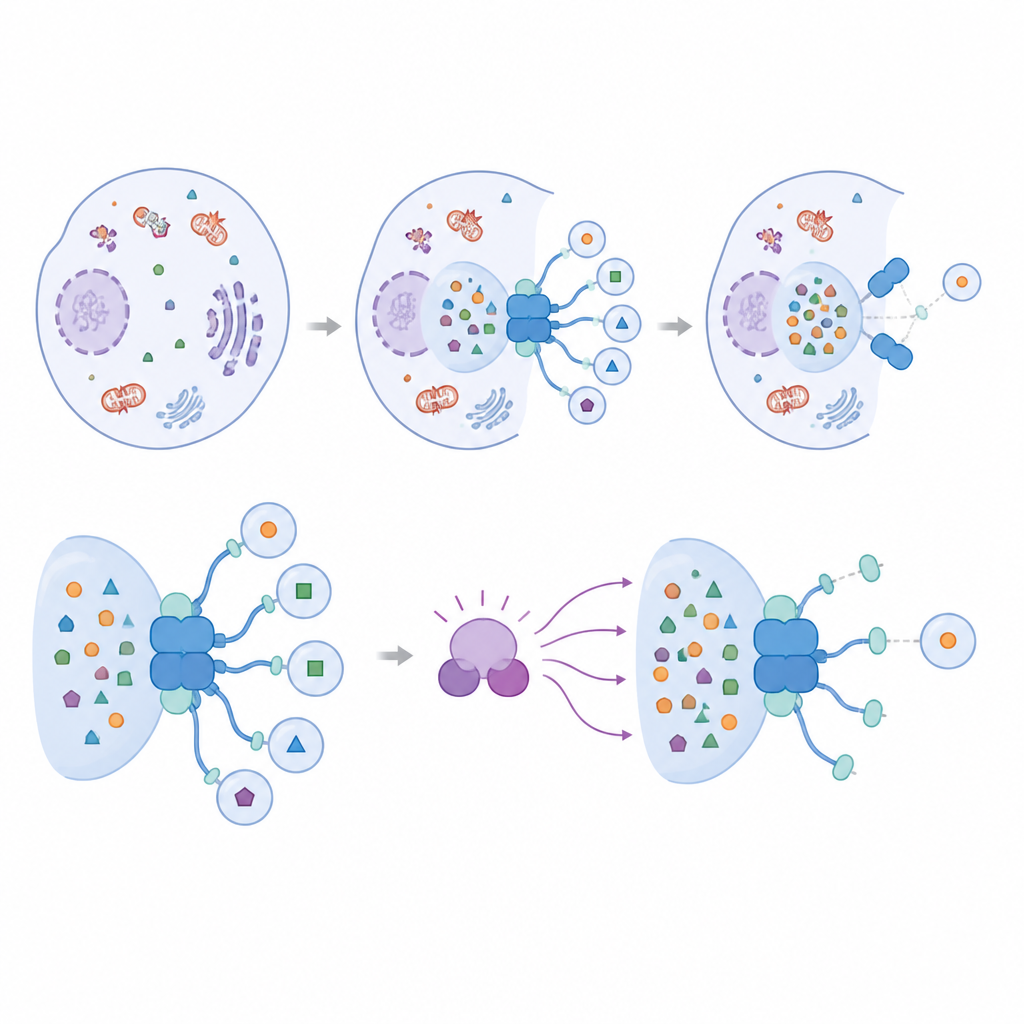
Eine molekulare Bremse für das Aufräum‑Zentrum
Die Studie fragt anschließend, wie dieses starke Initiationszentrum kontrolliert wird. Der Fokus richtet sich auf TBK1, ein Enzym, das bereits dafür bekannt ist, mehrere Formen selektiver Autophagie zu beeinflussen. Die Autorinnen und Autoren zeigen, dass TBK1 GABARAPL2 direkt an einer einzigen Aminosäure in der Nähe des Kontaktpunkts zu IRGQ modifiziert. Wenn diese Stelle so verändert wird, dass sie einen permanent modifizierten Zustand imitiert, schwächt sich die Bindung zwischen IRGQ und GABARAPL2 stark ab und der Komplex fällt auseinander. Fortgeschrittene Modellierungen und zellbasierte Experimente stimmen überein, dass diese Änderung GABARAPL2s Fähigkeit, allgemein mit anderen Partnern zu interagieren, nicht umfassend stört, sondern speziell die Verbindung zu IRGQ und der zugehörigen Initiationsmaschinerie destabilisiert.
Selektive Auswirkungen auf Fracht statt auf das globale Recycling
Das Auseinanderbrechen des IRGQ–GABARAPL2‑Zentrums hat überraschend gezielte Folgen. Die Bulk‑Autophagie, die allgemeine Recyclingantwort der Zelle während des Hungerns, bleibt weitgehend unverändert, selbst wenn die Modifikationsstelle auf GABARAPL2 verändert ist. Allerdings ist der Transport von GABARAPL2 selbst und der von IRGQ erkannter Fracht — einer Untergruppe von MHC‑Klasse‑I‑Molekülen — deutlich beeinträchtigt. In Zellen mit der phospho‑mimetischen Version von GABARAPL2 sammeln sich diese Immunmoleküle an der Zelloberfläche statt in Lysosomen abzubauen, was dem ähnelt, was passiert, wenn IRGQ fehlt. Umgekehrt führt das Blockieren der TBK1‑Aktivität dazu, dass mehr dieser Fracht in lysosomale Kompartimente geleitet wird, was darauf hinweist, dass TBK1 normalerweise diesen speziellen Weg der autophagischen Clearance bremst.
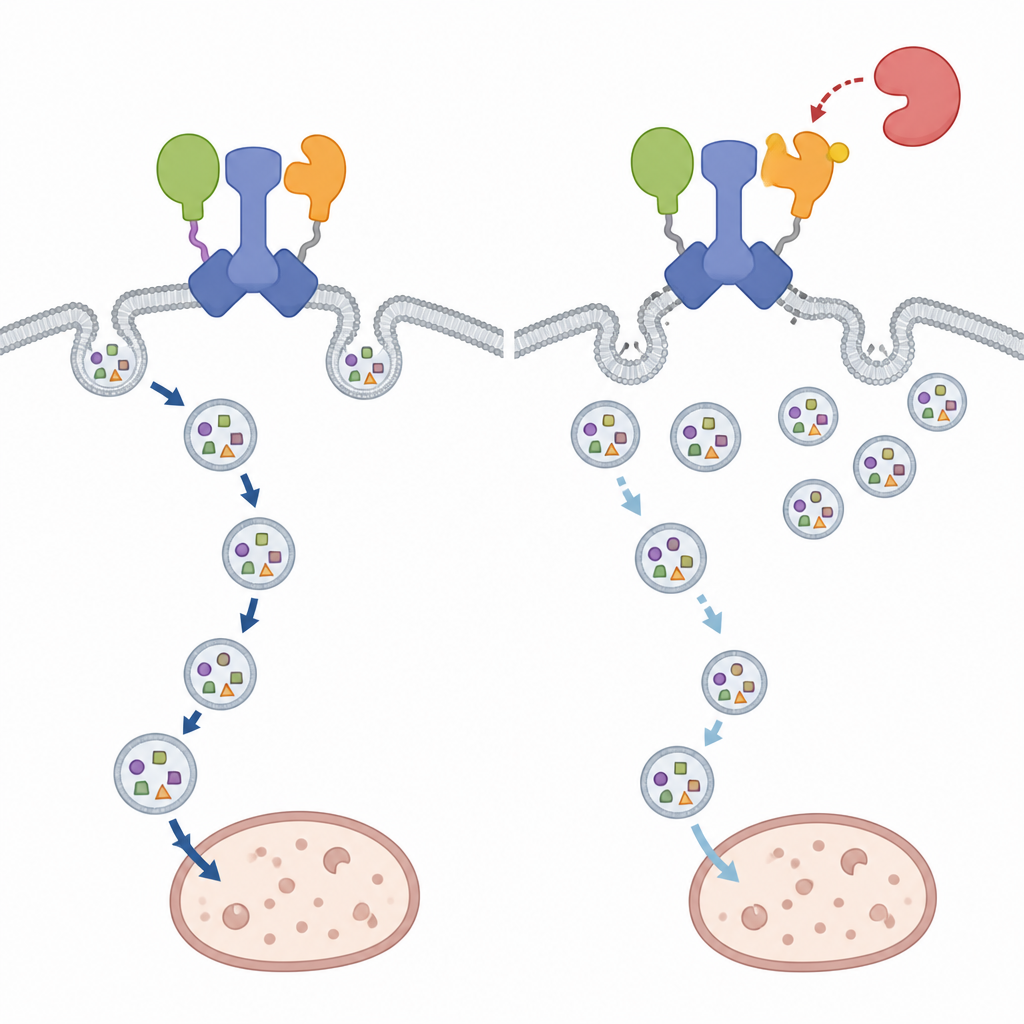
Ein kontextabhängiges Stopp‑Signal für das zelluläre Recycling
Zusammengefasst offenbaren die Ergebnisse IRGQ als zentralen Organisator, der ausgewählte Fracht mit den frühen Schritten der Autophagosomen‑Bildung verbindet, und TBK1 als kontextabhängige Bremse dieses Weges. Indem TBK1 GABARAPL2 im richtigen Moment modifiziert, kann es das IRGQ‑Zentrum ausschalten, ohne das globale Recycling der Zelle abzuschalten. Für eine interessierte Leserschaft bedeutet das: Zellen verfügen über einen fein abgestimmten Schalter, der eine spezifische Aufräumroute an- oder ausschalten kann und so beeinflusst, wie Immun‑Signale dargestellt und beschädigte Komponenten in unterschiedlichen Situationen entfernt werden.
Zitation: Gestal-Mato, U., Lascaux, P., Poveda-Cuevas, S.A. et al. TBK1 restricts IRGQ-mediated autophagy. Nat Commun 17, 4335 (2026). https://doi.org/10.1038/s41467-026-73005-3
Schlüsselwörter: selektive Autophagie, IRGQ, TBK1, GABARAPL2, Qualitätskontrolle von MHC Klasse I