Clear Sky Science · sv
TBK1 begränsar IRGQ-medierad autofagi
Hur celler bestämmer vad som ska behållas och vad som ska kastas
Inuti varje cell sorterar ett intensivt återvinningssystem ständigt ut slitna delar och felveckade proteiner innan de orsakar skada. Denna studie avslöjar hur ett litet proteinhub hjälper till att starta denna cellulära städning för specifikt gods, och hur ett annat enzym kan växla hubben till ett avstängt läge. Att förstå denna strömbrytare belyser hur celler finjusterar avfallshantering, med betydelse för åldrande, cancer, infektioner och immunreaktioner.
En riktad städpatrull inne i cellerna
Celler smälter inte bara slumpmässigt ner sitt innehåll. Istället använder de en process kallad autofagi för att omsluta utvalt material i små membransäckar och leverera det till sura kompartiment för nedbrytning. Specialiserade receptorproteiner hjälper till att välja vilket gods som packas och rekryterar den centrala städmaskineriet. Proteinet IRGQ identifierades nyligen som en sådan receptor som känner igen vissa varianter av immunsignal-molekyler på cellytan. I detta arbete visar författarna att IRGQ är mer än en enkel markerare av gods; det organiserar också de tidiga stegen i bildandet av autofagosomer.
En proteinhubb som förbinder gods och maskineri
IRGQ interagerar med en familj av små adapterproteiner kända som ATG8s, som pryder det framväxande autofagosommembranet och är essentiella för att bygga dessa återvinningssäckar. Forskarna fann att IRGQ bär två separata dockningsställen som kan binda olika ATG8-medlemmar. Ett av dessa ställen visar en påtaglig preferens för ett enskilt ATG8-protein kallat GABARAPL2. Genom strukturella prediktioner, protein-pulldown-assay och mikroskopi demonstrerar teamet att IRGQ och GABARAPL2 tillsammans bildar en hubb som rekryterar nyckelenzymer ansvariga för att fästa ATG8-proteiner på membran. När denna hubb är närvarande ser cellerna ökad ATG8-fästring och mer autofagisk aktivitet för specifika laster, vilket bekräftar att IRGQ aktivt främjar initieringen av selektiv städning snarare än bara att märka material för nedbrytning.
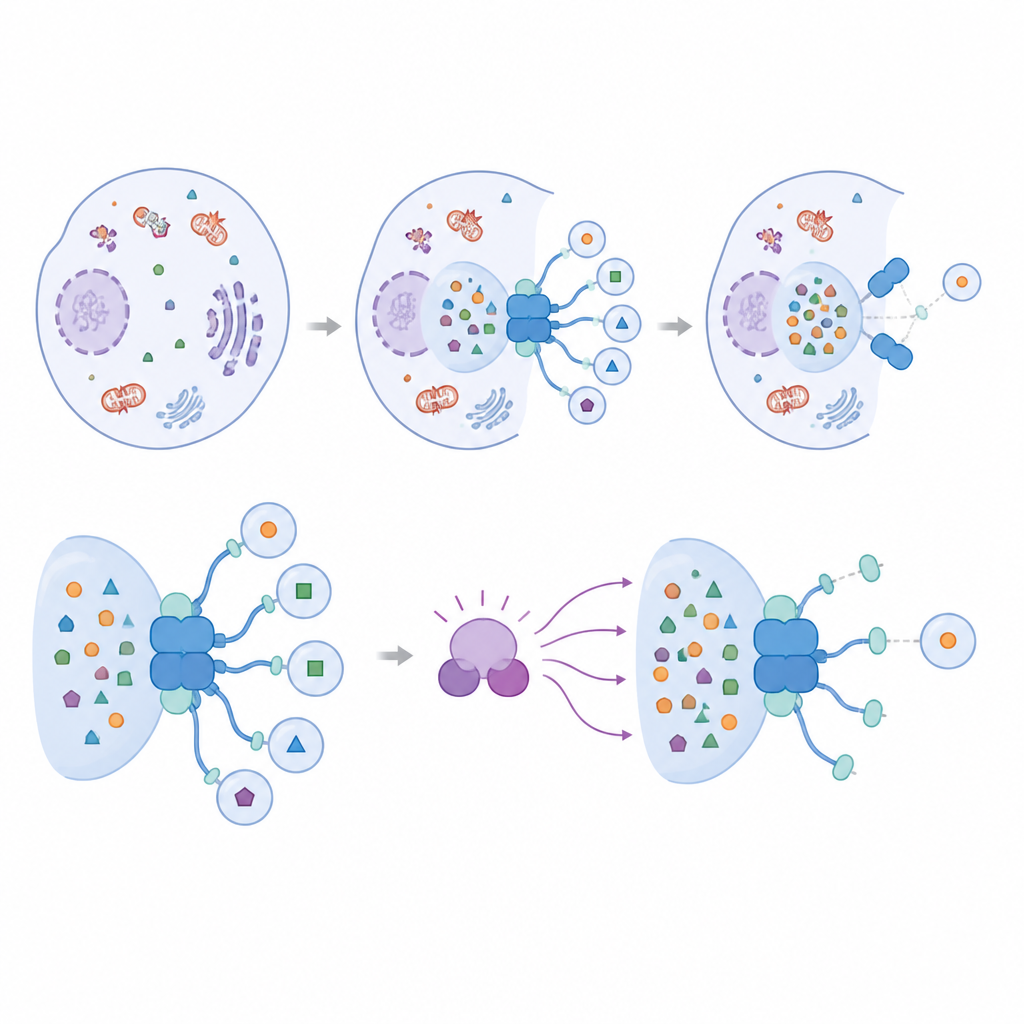
En molekylär broms på städhubben
Studien frågar sedan hur denna kraftfulla initieringshubb kontrolleras. Fokus hamnar på TBK1, ett enzym som redan är känt för att påverka flera former av selektiv autofagi. Författarna visar att TBK1 direkt modifierar GABARAPL2 vid en enda aminosyra nära dess kontaktpunkt med IRGQ. När denna plats ändras för att efterlikna ett permanent modifierat tillstånd försvagas bindningen mellan IRGQ och GABARAPL2 kraftigt och komplexet faller isär. Avancerad modellering och cellbaserade experiment överensstämmer om att denna förändring inte i bred bemärkelse stör GABARAPL2:s förmåga att interagera med andra partners, utan snarare specifikt destab iliserar dess länk till IRGQ och det associerade initieringsmaskineriet.
Selektiva effekter på gods snarare än global återvinning
Att bryta upp IRGQ–GABARAPL2-hubben får förvånansvärt fokuserade konsekvenser. Bulkautofagin, cellens generella återvinningssvar vid svält, fortsätter i stort sett oförändrad även när modifieringsstället på GABARAPL2 är ändrat. Däremot försämras trafiken för GABARAPL2 självt och för IRGQ:s last, en undergrupp av MHC klass I-molekyler, tydligt. I celler som bär den fosfo-mimerande versionen av GABARAPL2 ansamlas dessa immunsignalmolekyler vid cellytan istället för att nå lysosomerna för nedbrytning, vilket nära speglar vad som händer när IRGQ saknas. Omvänt trycker blockering av TBK1-aktivitet mer av detta gods mot lysosomala kompartiment, vilket indikerar att TBK1 normalt agerar för att begränsa just denna väg för autofagisk rensning.
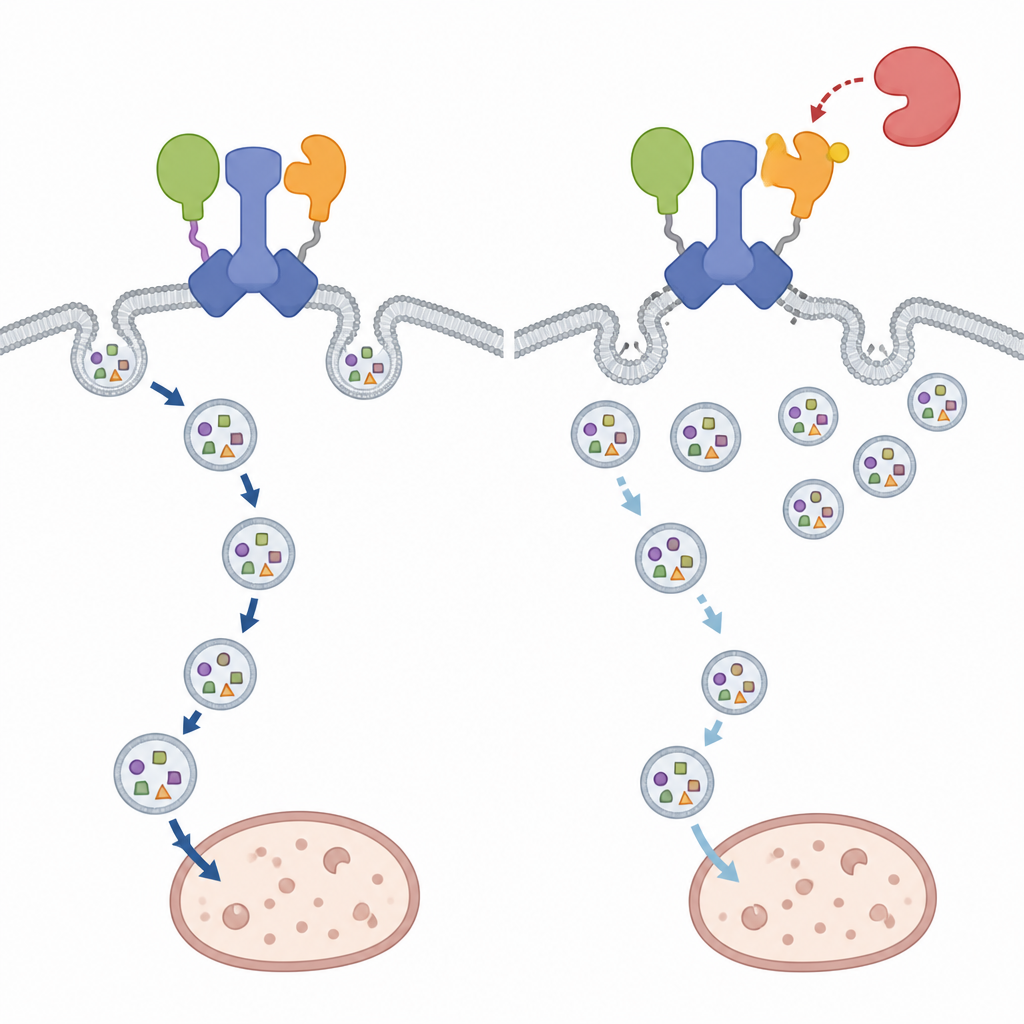
En kontextberoende stoppsignal för cellulär återvinning
Sammantaget visar fynden att IRGQ är en central organisatör som länkar utvalt gods till de tidiga stegen i autofagosombildning, och TBK1 som en kontextberoende broms på denna väg. Genom att modifiera GABARAPL2 vid precis rätt ögonblick kan TBK1 stänga av IRGQ-hubben utan att slå av cellens globala återvinningssystem. För en lekmannaläsare betyder detta att celler har en finjusterad strömbrytare som kan slå på eller av en specifik städrutt och därigenom forma hur immunsignaler visas och hur skadade komponenter avlägsnas i olika situationer.
Citering: Gestal-Mato, U., Lascaux, P., Poveda-Cuevas, S.A. et al. TBK1 restricts IRGQ-mediated autophagy. Nat Commun 17, 4335 (2026). https://doi.org/10.1038/s41467-026-73005-3
Nyckelord: selektiv autofagi, IRGQ, TBK1, GABARAPL2, MHC klass I kvalitetskontroll