Clear Sky Science · it
TBK1 limita l'autofagia mediata da IRGQ
Come le cellule decidono cosa conservare e cosa eliminare
All'interno di ogni cellula, un sistema di riciclaggio attivo seleziona costantemente parti usurate e proteine mal ripiegate prima che causino problemi. Questo studio svela come un piccolo hub proteico aiuti ad avviare questa pulizia cellulare per carichi specifici e come un altro enzima possa mettere questo hub nello stato di spento. Comprendere questo interruttore illumina il modo in cui le cellule regolano finemente lo smaltimento dei rifiuti, con implicazioni per l'invecchiamento, il cancro, le infezioni e le risposte immunitarie.
Una squadra di pulizia mirata all'interno delle cellule
Le cellule non degradano il loro contenuto casualmente. Usano invece un processo chiamato autofagia per avvolgere materiale selezionato in piccole vescicole di membrana e consegnarlo a compartimenti acidi per la degradazione. Proteine recettrici specializzate aiutano a scegliere quali carichi vengono confezionati e reclutano la macchina di pulizia centrale. La proteina IRGQ è stata recentemente identificata come uno di questi recettori che riconosce particolari versioni di molecole che espongono segnali immunitari sulla superficie cellulare. In questo lavoro, gli autori mostrano che IRGQ è più di un semplice etichettatore di carico; organizza anche i primi passi della formazione dell'autofagosoma.
Un hub proteico che collega carico e macchinario
IRGQ interagisce con una famiglia di piccole proteine adattatrici note come ATG8, che decorano la membrana in formazione dell'autofagosoma e sono essenziali per costruire queste vescicole di riciclaggio. Il gruppo ha scoperto che IRGQ possiede due siti di aggancio separati che possono legare differenti membri della famiglia ATG8. Uno di questi siti mostra una netta preferenza per un singolo ATG8 chiamato GABARAPL2. Utilizzando predizioni strutturali, saggi di pull-down proteico e microscopia, i ricercatori dimostrano che IRGQ e GABARAPL2 insieme formano un hub che richiama enzimi chiave responsabili dell'attacco degli ATG8 alle membrane. Quando questo hub è presente, le cellule mostrano un aumento dell'ancoraggio degli ATG8 e maggiore attività autofagica per carichi specifici, confermando che IRGQ promuove attivamente l'inizio della pulizia selettiva piuttosto che limitarsi a marcare il materiale per lo smaltimento.
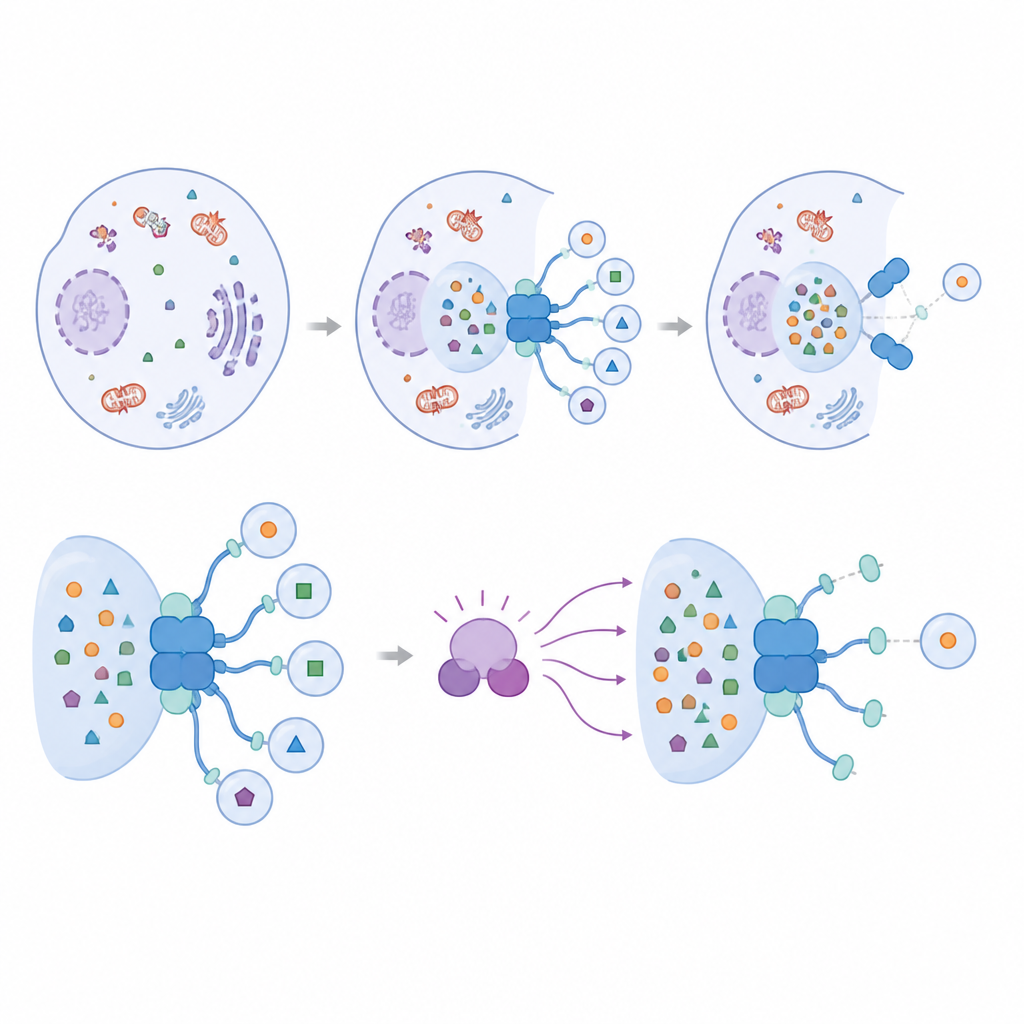
Un freno molecolare sull'hub di pulizia
Lo studio si chiede poi come sia controllato questo potente hub di inizio. L'attenzione si sposta su TBK1, un enzima già noto per influenzare diverse forme di autofagia selettiva. Gli autori mostrano che TBK1 modifica direttamente GABARAPL2 in un singolo amminoacido vicino al suo punto di contatto con IRGQ. Quando questo sito è alterato in modo da imitare uno stato permanentemente modificato, il legame tra IRGQ e GABARAPL2 si indebolisce nettamente e il complesso si disfa. Modellizzazioni avanzate e esperimenti su cellule concordano sul fatto che questo cambiamento non compromette in modo generale la capacità di GABARAPL2 di interagire con altri partner, ma destabilizza specificamente il suo collegamento con IRGQ e il macchinario di inizio associato.
Effetti selettivi sul carico piuttosto che sul riciclaggio globale
La disgregazione dell'hub IRGQ–GABARAPL2 ha conseguenze sorprendentemente specifiche. L'autofagia bulk, la risposta di riciclaggio generale della cellula durante la deprivazione, continua in gran parte invariata anche quando il sito di modificazione su GABARAPL2 è alterato. Tuttavia, il traffico della stessa GABARAPL2 e del carico di IRGQ, un sottoinsieme delle molecole del complesso maggiore di istocompatibilità di classe I, risulta chiaramente compromesso. Nelle cellule che portano la versione fosfo-mimetica di GABARAPL2, queste molecole immunitarie si accumulano sulla superficie cellulare invece di raggiungere i lisosomi per la degradazione, rispecchiando da vicino quanto avviene quando IRGQ è assente. Al contrario, bloccare l'attività di TBK1 spinge una maggiore quantità di questo carico verso i compartimenti lisosomali, indicando che TBK1 agisce normalmente per frenare questa particolare via di eliminazione autofagica.
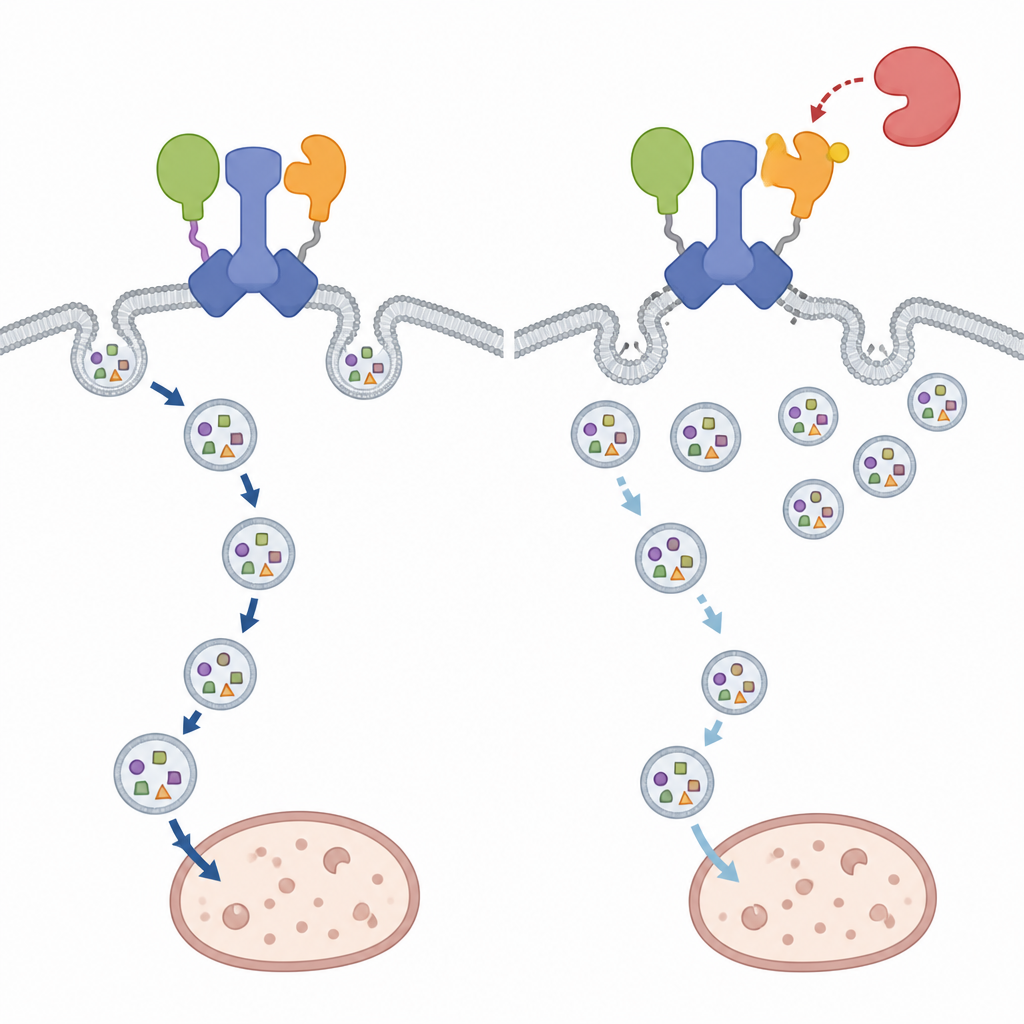
Un segnale di stop dipendente dal contesto per il riciclaggio cellulare
Nel complesso, i risultati rivelano IRGQ come un organizzatore centrale che collega il carico scelto ai primi passi della formazione dell'autofagosoma, e TBK1 come un freno dipendente dal contesto di questa via. Modificando GABARAPL2 nel momento giusto, TBK1 può spegnere l'hub IRGQ senza chiudere il sistema di riciclaggio globale della cellula. Per il lettore non specialistico, ciò significa che le cellule possiedono un interruttore finemente regolato che può attivare o disattivare una specifica via di pulizia, influenzando come vengono esposti i segnali immunitari e come vengono rimossi componenti danneggiati in situazioni diverse.
Citazione: Gestal-Mato, U., Lascaux, P., Poveda-Cuevas, S.A. et al. TBK1 restricts IRGQ-mediated autophagy. Nat Commun 17, 4335 (2026). https://doi.org/10.1038/s41467-026-73005-3
Parole chiave: autofagia selettiva, IRGQ, TBK1, GABARAPL2, controllo qualità delle MHC di classe I