Clear Sky Science · nl
TBK1 beperkt IRGQ-gemedieerde autofagie
Hoe cellen beslissen wat ze bewaren en wat ze weggooien
In elke cel sorteert een druk recyclingsysteem voortdurend versleten onderdelen en misgevouwen eiwitten voordat ze problemen veroorzaken. Deze studie onthult hoe een kleine proteïnehub helpt bij het opstarten van deze cellulare opruiming voor specifiek materiaal, en hoe een ander enzym die hub kan omzetten naar een uit‑stand. Inzicht in deze schakelwerkwijze werpt licht op hoe cellen afvalverwerking nauwkeurig bijsturen, met implicaties voor veroudering, kanker, infecties en immuunreacties.
Een gerichte opruimploeg binnen cellen
Cellen verteren niet zomaar willekeurig hun inhoud. In plaats daarvan gebruiken ze een proces dat autofagie heet om geselecteerd materiaal in kleine membraanzakjes te verpakken en naar zure compartimenten te brengen voor afbraak. Gespecialiseerde receptor‑eiwitten helpen bepalen welk materiaal wordt ingepakt en rekruteren de kernmachinerie voor opruiming. Het eiwit IRGQ werd recentelijk geïdentificeerd als zo’n receptor die bepaalde varianten van immuunpresenterende moleculen op het celoppervlak herkent. In dit werk tonen de auteurs aan dat IRGQ meer is dan een simpele markeerder van lading; het organiseert ook de vroege stappen van de vorming van autofagosomen.
Een proteïnehub die lading en machinerie verbindt
IRGQ wisselt interacties uit met een familie van kleine adaptor‑eiwitten bekend als ATG8’s, die het vormende autofagosoommembraan sieren en essentieel zijn voor de opbouw van deze recyclingszakken. Het team vond dat IRGQ twee afzonderlijke aanhechtingssites draagt die verschillende ATG8‑leden kunnen binden. Eén van deze sites vertoont een opvallende voorkeur voor één enkel ATG8‑eiwit, GABARAPL2. Met structurele voorspellingen, eiwit‑pulldown‑proeven en microscopie laten de onderzoekers zien dat IRGQ en GABARAPL2 samen een hub vormen die sleutelenzymen binnenhaalt die verantwoordelijk zijn voor het koppelen van ATG8‑eiwitten aan membranen. Wanneer deze hub aanwezig is, vertonen cellen verhoogde ATG8‑aanhechting en meer autofagische activiteit voor specifieke ladingen, wat bevestigt dat IRGQ actief de initiatie van selectieve opruiming bevordert in plaats van alleen materiaal te labelen voor afvoer.
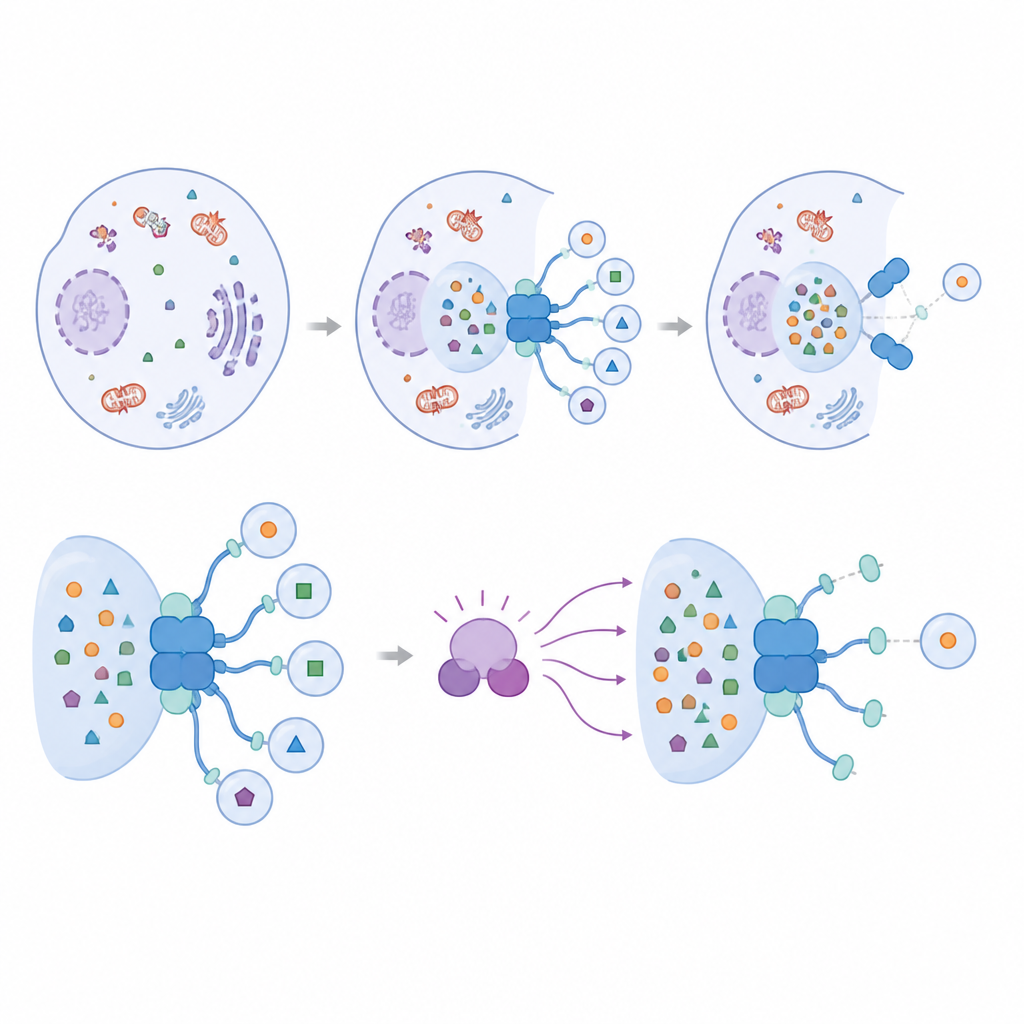
Een moleculaire rem op de opruimhub
De studie vraagt vervolgens hoe deze krachtige initiatiehub wordt gereguleerd. De aandacht gaat uit naar TBK1, een enzym dat al bekendstaat om zijn invloed op meerdere vormen van selectieve autofagie. De auteurs tonen aan dat TBK1 GABARAPL2 rechtstreeks wijzigt op één aminozuur dicht bij het contactpunt met IRGQ. Wanneer deze plaats zodanig is veranderd dat het een permanent gemodificeerde toestand nabootst, verzwakt de binding tussen IRGQ en GABARAPL2 sterk en valt het complex uiteen. Geavanceerde modellering en celgebaseerde experimenten komen overeen dat deze wijziging de algemene vermogen van GABARAPL2 om met andere partners te interacteren niet breed verstoort, maar specifiek zijn verbinding met IRGQ en de bijbehorende initiatiemachinerie destabiliseert.
Selectieve effecten op lading in plaats van globale recycling
Het uiteenvallen van de IRGQ–GABARAPL2‑hub heeft verrassend gerichte gevolgen. Bulk‑autofagie, de algemene recyclingreactie van de cel tijdens uithongering, blijft grotendeels onveranderd zelfs wanneer de modificatieplaats op GABARAPL2 is aangepast. De trafficking van GABARAPL2 zelf en van IRGQ’s lading — een subset van major histocompatibility complex klasse I‑moleculen — wordt echter duidelijk belemmerd. In cellen met de fosfo‑nabootsende versie van GABARAPL2 stapelen deze immuunmoleculen zich op aan het celoppervlak in plaats van naar lysosomen te gaan voor afbraak, wat sterk overeenkomt met wat er gebeurt wanneer IRGQ ontbreekt. Omgekeerd duwt het blokkeren van TBK1‑activiteit meer van deze lading richting lysosomale compartimenten, wat aangeeft dat TBK1 normaal gesproken handelt om deze specifieke route van autofagische klaring te remmen.
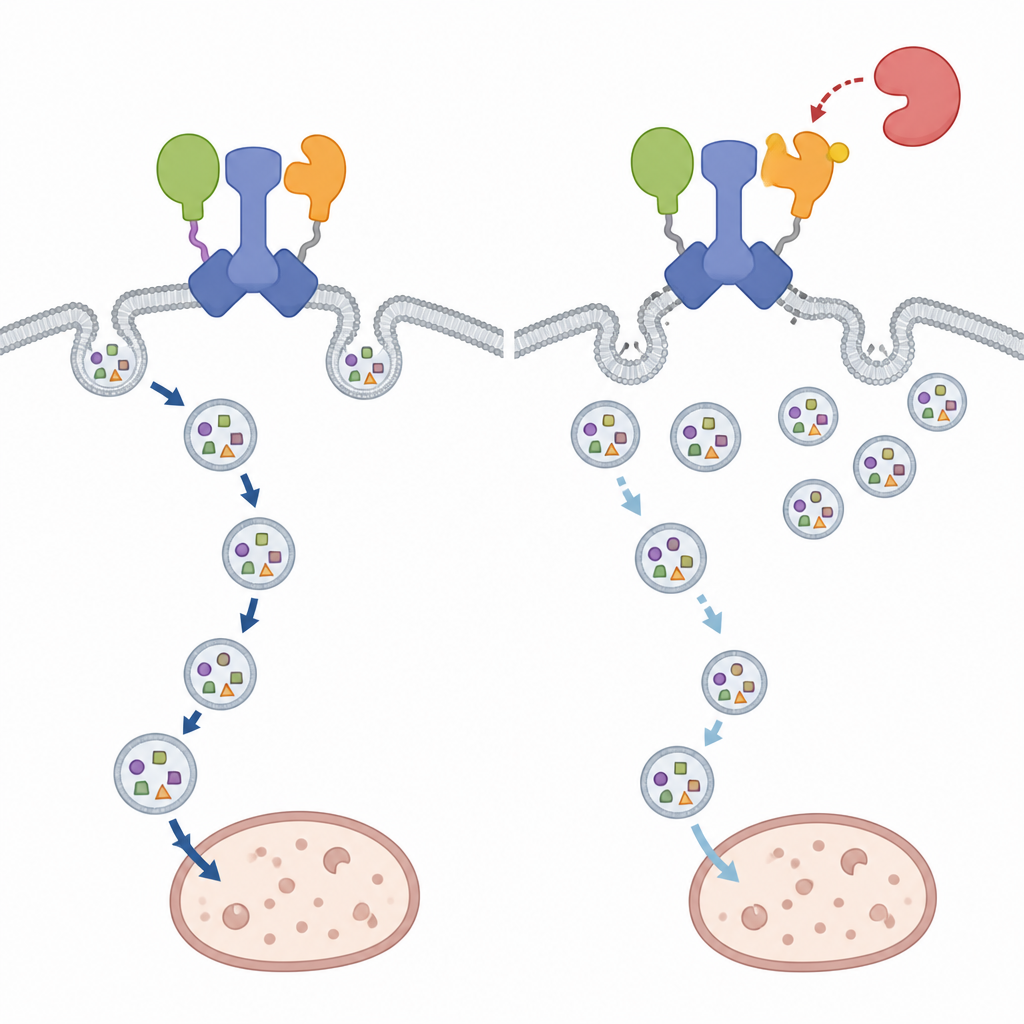
Een contextafhankelijke stop‑signal voor cellulair recyclen
Samengevat onthullen de bevindingen IRGQ als een centrale organisator die geselecteerde lading koppelt aan de vroege stappen van autofagosoomvorming, en TBK1 als een contextafhankelijke rem op deze route. Door GABARAPL2 op het juiste moment te modificeren, kan TBK1 de IRGQ‑hub uitschakelen zonder het globale recyclingsysteem van de cel stop te zetten. Voor een niet‑specialistische lezer betekent dit dat cellen beschikken over een fijn afgestelde schakelaar die een specifieke opruimroute aan of uit kan zetten, en daarmee bepaalt hoe immuunsignalen worden gepresenteerd en hoe beschadigde componenten in verschillende situaties worden verwijderd.
Bronvermelding: Gestal-Mato, U., Lascaux, P., Poveda-Cuevas, S.A. et al. TBK1 restricts IRGQ-mediated autophagy. Nat Commun 17, 4335 (2026). https://doi.org/10.1038/s41467-026-73005-3
Trefwoorden: selectieve autofagie, IRGQ, TBK1, GABARAPL2, MHC klasse I kwaliteitscontrole