Clear Sky Science · fr
TBK1 restreint l’autophagie médiée par IRGQ
Comment les cellules décident quoi garder et quoi jeter
À l’intérieur de chaque cellule, un système de recyclage actif trie en permanence les éléments usés et les protéines mal repliées avant qu’ils ne posent problème. Cette étude dévoile comment un petit hub protéique aide à lancer ce nettoyage cellulaire pour des cargaisons spécifiques, et comment une autre enzyme peut basculer ce hub en position « arrêt ». Comprendre cet interrupteur éclaire la manière dont les cellules ajustent finement l’élimination des déchets, avec des implications pour le vieillissement, le cancer, les infections et les réponses immunitaires.
Une équipe de nettoyage ciblée à l’intérieur des cellules
Les cellules ne digèrent pas leurs contenus au hasard. Elles utilisent plutôt un processus appelé autophagie pour entourer du matériel sélectionné dans de petites vésicules membranaires et l’acheminer vers des compartiments acides pour dégradation. Des protéines réceptrices spécialisées aident à choisir quelles cargaisons sont emballées et recrutent la machinerie centrale du nettoyage. La protéine IRGQ a été récemment identifiée comme l’un de ces récepteurs reconnaissant certaines formes de molécules de présentation immunitaire à la surface cellulaire. Dans ce travail, les auteurs montrent qu’IRGQ est plus qu’un simple marqueur de cargaison : il organise aussi les premières étapes de la formation des autophagosomes.
Un hub protéique qui relie cargaison et machinerie
IRGQ interagit avec une famille de petites protéines adaptatrices connues sous le nom d’ATG8, qui ornent la membrane en formation de l’autophagosome et sont essentielles à la construction de ces vésicules de recyclage. L’équipe a trouvé qu’IRGQ possède deux sites d’ancrage distincts capables de lier différents membres des ATG8. L’un de ces sites montre une préférence marquée pour une seule protéine ATG8 appelée GABARAPL2. À l’aide de prédictions structurelles, d’essais de pulldown protéique et de microscopie, les chercheurs démontrent qu’IRGQ et GABARAPL2 forment ensemble un hub qui attire des enzymes clés responsables de l’attachement des protéines ATG8 aux membranes. En présence de ce hub, les cellules présentent une augmentation de l’attachement des ATG8 et une activité autophagique accrue pour des cargaisons spécifiques, confirmant qu’IRGQ favorise activement l’initiation du nettoyage sélectif plutôt que de se contenter d’étiqueter le matériel à éliminer.
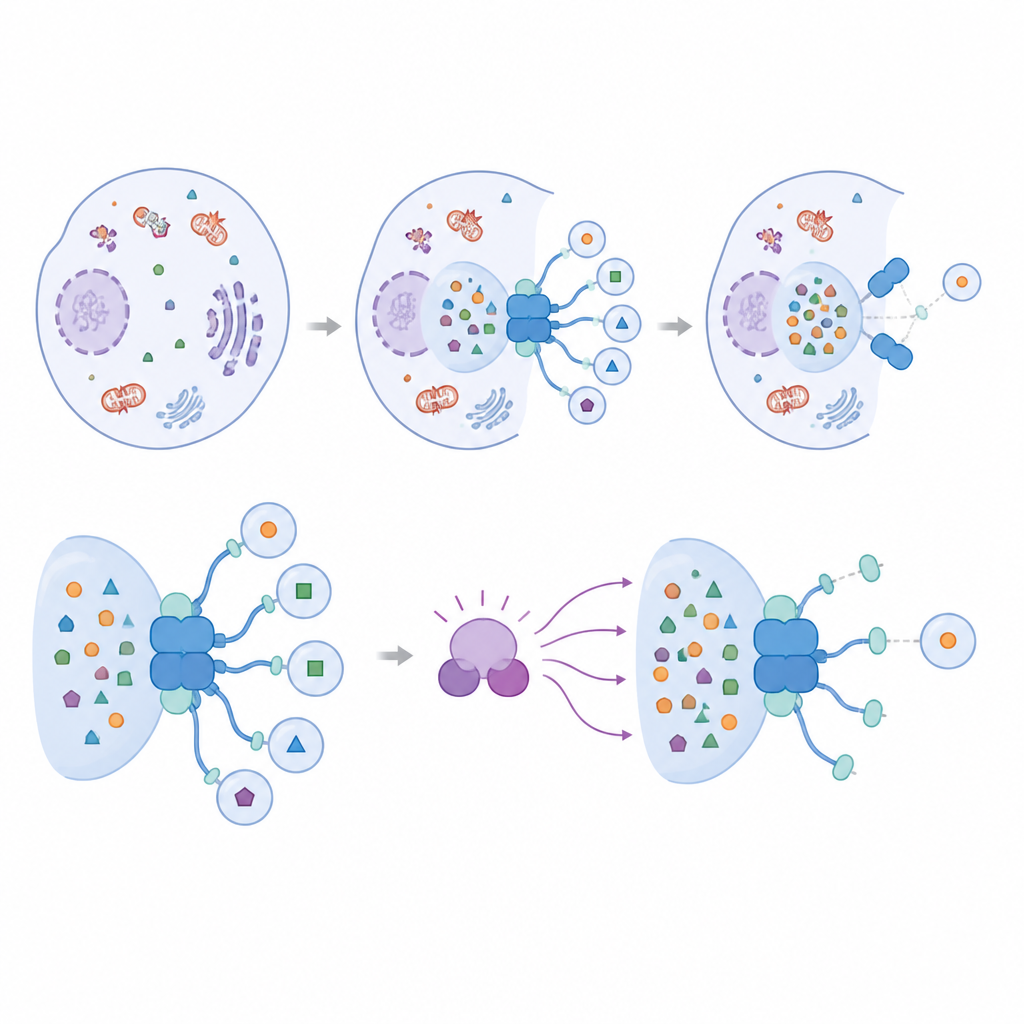
Un frein moléculaire sur le hub de nettoyage
L’étude s’intéresse ensuite à la manière dont ce puissant hub d’initiation est contrôlé. L’attention se porte sur TBK1, une enzyme déjà connue pour influencer plusieurs formes d’autophagie sélective. Les auteurs montrent que TBK1 modifie directement GABARAPL2 en un seul acide aminé situé près de son point de contact avec IRGQ. Lorsque ce site est altéré pour imiter un état constamment modifié, la liaison entre IRGQ et GABARAPL2 s’affaiblit fortement et le complexe se dissocie. Les modélisations avancées et les expériences cellulaires convergent pour indiquer que ce changement ne perturbe pas globalement la capacité de GABARAPL2 à interagir avec d’autres partenaires, mais déstabilise spécifiquement son lien avec IRGQ et la machinerie d’initiation associée.
Effets sélectifs sur la cargaison plutôt que sur le recyclage global
La dissociation du hub IRGQ–GABARAPL2 a des conséquences étonnamment focalisées. L’autophagie en vrac, la réponse de recyclage générale de la cellule pendant la privation, reste en grande partie inchangée même lorsque le site de phosphorylation de GABARAPL2 est modifié. En revanche, le trafic de GABARAPL2 lui‑même et celui de la cargaison d’IRGQ, un sous-ensemble de molécules du complexe majeur d’histocompatibilité de classe I, est clairement perturbé. Dans les cellules portant la version mimant la phosphorylation de GABARAPL2, ces molécules immunitaires s’accumulent à la surface cellulaire au lieu d’atteindre les lysosomes pour être dégradées, reproduisant de près ce qui se passe quand IRGQ est absent. Inversement, bloquer l’activité de TBK1 oriente davantage cette cargaison vers les compartiments lysosomaux, indiquant que TBK1 agit normalement pour freiner cette voie particulière d’élimination autophagique.
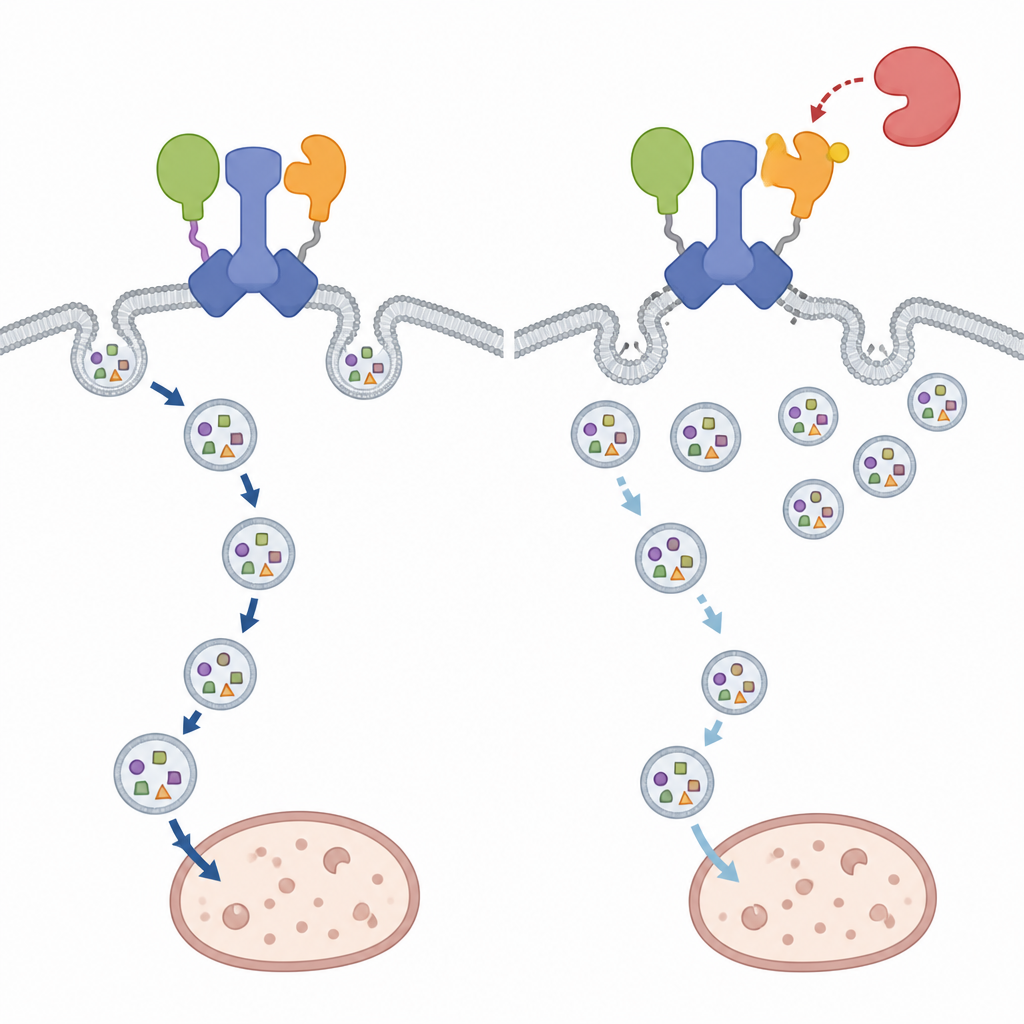
Un signal d’arrêt contextuel pour le recyclage cellulaire
Pris ensemble, les résultats révèlent IRGQ comme un organisateur central reliant les cargaisons choisies aux premières étapes de la formation des autophagosomes, et TBK1 comme un frein contextuel de cette voie. En modifiant GABARAPL2 au moment opportun, TBK1 peut désactiver le hub IRGQ sans interrompre le système de recyclage global de la cellule. Pour le lecteur non spécialiste, cela signifie que les cellules possèdent un interrupteur finement réglé capable d’activer ou d’éteindre une voie de nettoyage spécifique, modulant la manière dont les signaux immunitaires sont affichés et comment les composants endommagés sont éliminés selon les situations.
Citation: Gestal-Mato, U., Lascaux, P., Poveda-Cuevas, S.A. et al. TBK1 restricts IRGQ-mediated autophagy. Nat Commun 17, 4335 (2026). https://doi.org/10.1038/s41467-026-73005-3
Mots-clés: autophagie sélective, IRGQ, TBK1, GABARAPL2, contrôle qualité des CMH de classe I