Clear Sky Science · zh
罕见的调控突变扰乱驱动二尖瓣主动脉瓣形成的间充质分子程序
心脏瓣膜何以不同形成
二尖瓣主动脉瓣是一种常见的先天性心脏缺陷,患者把血液输送到全身的主瓣仅有两个瓣叶,而不是正常的三个。许多患有此情况的人最终需要手术,但临床上仍无法完全解释其发生机制或哪些家庭成员风险更高。本研究深入研究我们基因组的控制开关,揭示在早期发育阶段罕见且难以察觉的基因调控改变如何误导瓣膜的构建,从而促成二尖瓣主动脉瓣的形成。
从正常瓣膜到隐匿风险
主动脉瓣像一道门,位于心脏与全身最大动脉之间。大多数人天生具有三个瓣叶,随每次心跳平稳地开合。然而大约多达1.5%的人群中,瓣膜只有两个瓣叶。这种二尖瓣形态会增加心脏负担,促进危险的瓣膜狭窄或返流,并削弱相邻的升主动脉。家系研究显示该病具有较强的遗传性,但已知的蛋白编码区突变只能解释少数病例。作者怀疑答案可能隐藏在控制基因何时何地表达的非编码DNA中。
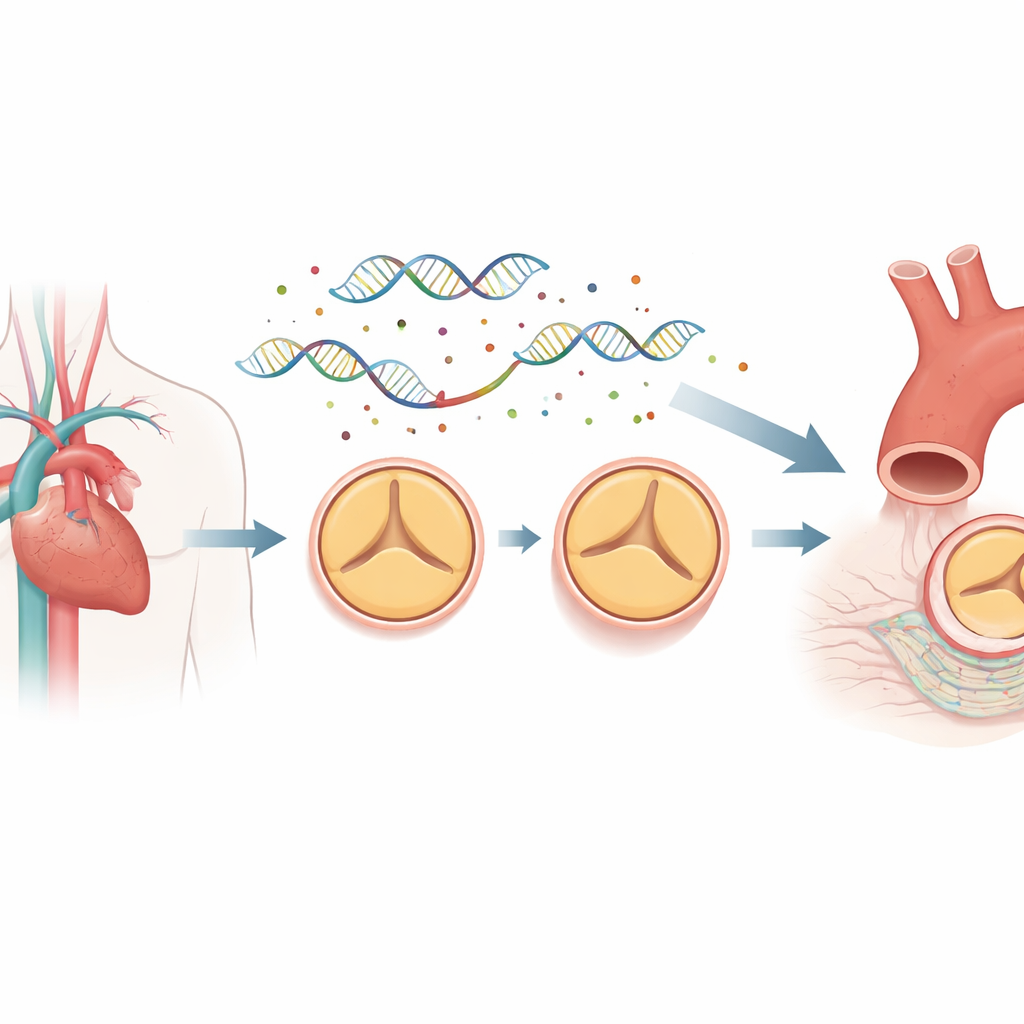
瓣膜发育背后的DNA控制图谱
我们的大部分基因组并不编码蛋白质,而是包含调控元件,如增强子和启动子,类似于基因的调光开关与电路布线。这些区域可以位于其所调控基因的远端,通过三维空间回环接触到目标基因。为了解这些布线在二尖瓣患者与正常瓣膜个体之间如何不同,研究者从正在接受手术的八位二尖瓣患者和八位正常三瓣患者处采集了升主动脉内层衬里细胞。他们使用称为启动子捕获 Hi‑C 的技术绘制出数百万条长程DNA接触,并结合全基因组测序来定位位于这些调控区域内的罕见突变。
重接线发育中瓣膜细胞的罕见突变
研究团队发现高达95%的个体间遗传差异位于非编码区域,且二尖瓣患者在与瓣膜发育相关基因周围的DNA回环中显示出更多与突变相关的改变,而对照组则较少。研究者不仅依赖成年组织信号,还将他们的布线图与来自人类胚胎心脏的单细胞与空间基因表达数据叠加。这使他们能询问哪些早期细胞类型会受到改变调控开关的影响。最强的信号来自参与形成所谓心内膜垫的间充质细胞——这些胚胎心脏中的临时组织垫随后重塑为成熟瓣膜及流出道的一部分。
胎儿心脏中受扰乱的垫组织程序
通过追踪与突变增强子和启动子相连的基因,作者鉴定出198个与二尖瓣主动脉瓣相关的候选基因,约为先前已知数量的三十倍左右。这些基因聚集在驱动扁平衬里细胞向侵入性垫细胞转变的通路中,该过程称为上皮‑间充质转化(epithelial‑to‑mesenchymal transition),以及如TGF‑beta及相关网络等信号通路中。他们还在一类与 NFAT 相关的调控蛋白的结合位点中观察到反复命中,NFAT 对将垫组织塑造成成熟瓣膜至关重要。调控活性的计算模型支持许多这些变体特异性在胎儿心脏组织和升主动脉中起作用的观点。总体而言,结果表明罕见的调控突变细微地扭曲了形成垫组织的间充质细胞的基因程序,推动发育走向异常的两瓣瓣膜。
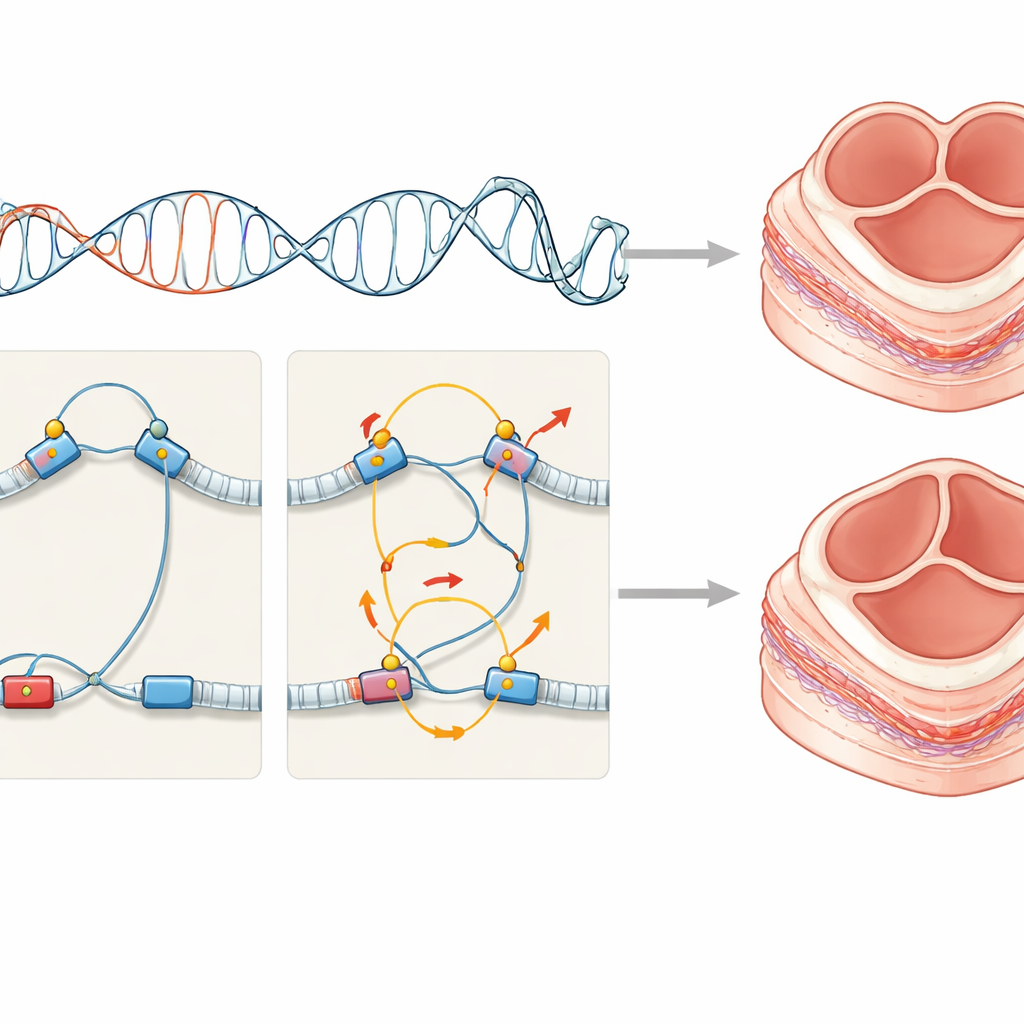
由许多小片段组成的复杂遗传拼图
在患者间观察时,研究者发现每个人携带自己特有的一组罕见调控改变,常与改变蛋白的突变共存,且只有少数受影响基因在个体间共享。然而,这些多样的改变连接成一个相互作用的蛋白网络,指向一个共同的生物学主题,而非随机损伤。该研究还表明,胚胎期建立的一些调控布线模式在成体细胞中仍可检测到,为研究产前事件提供了现实的观察窗口。
这对患者与家属意味着什么
对非专业读者来说,主要信息是二尖瓣主动脉瓣通常并非由单一有缺陷的基因引起,而是由多个微妙的基因开启方式变化在早期心脏形成期间共同作用引起的。这些罕见的调控突变有助于解释为什么该病具有家族性但在遗传上又呈高度多样性。长期来看,绘制这层隐藏的基因组控制图谱可能改进对亲属的遗传风险评估,并指导研究开发新的方法以监测或治疗先天携带这种常见瓣膜缺陷的人群。
引用: Zhigulev, A., Buyan, A., Lázár, E. et al. Rare regulatory mutations disrupt mesenchymal molecular programs driving endocardial cushion formation in bicuspid aortic valve. Nat Commun 17, 3587 (2026). https://doi.org/10.1038/s41467-026-71758-5
关键词: 二尖瓣主动脉瓣, 心脏瓣膜发育, 非编码 DNA, 调控突变, 间充质细胞