Clear Sky Science · fr
Des mutations régulatrices rares perturbent les programmes moléculaires mésenchymateux guidant la formation des coussins endocardiques dans la valvule aortique bicuspide
Quand les valves cardiaques se forment différemment
La valvule aortique bicuspide est une malformation cardiaque congénitale fréquente dans laquelle la principale valve assurant la sortie du cœur vers le corps comporte seulement deux feuillets au lieu de trois. De nombreuses personnes atteintes finissent par nécessiter une intervention chirurgicale, et pourtant les médecins ne peuvent pas encore expliquer entièrement pourquoi cela survient ni quels membres de la famille sont les plus à risque. Cette étude explore en profondeur les interrupteurs de commande de notre ADN pour révéler comment des changements rares et difficiles à détecter dans la régulation des gènes au cours du développement précoce peuvent dévier la construction des valves cardiaques et contribuer à l’apparition d’une valvule aortique bicuspide.
De la valve normale à un risque caché
La valve aortique fonctionne comme une porte entre le cœur et la plus grosse artère du corps. La plupart des personnes naissent avec trois feuillets qui s’ouvrent et se referment harmonieusement à chaque battement. Cependant, chez environ 1,5 % de la population, la valve ne comporte que deux feuillets. Cette forme bicuspide peut surcharger le cœur, favoriser un rétrécissement ou un reflux dangereux de la valve et affaiblir l’aorte voisine. Les études familiales montrent que l’affection est fortement héréditaire, mais les mutations connues dans les régions codantes des gènes n’expliquent qu’une petite fraction des cas. Les auteurs ont émis l’hypothèse que les réponses manquantes pourraient se trouver dans l’ADN non codant qui contrôle quand et où les gènes sont activés.
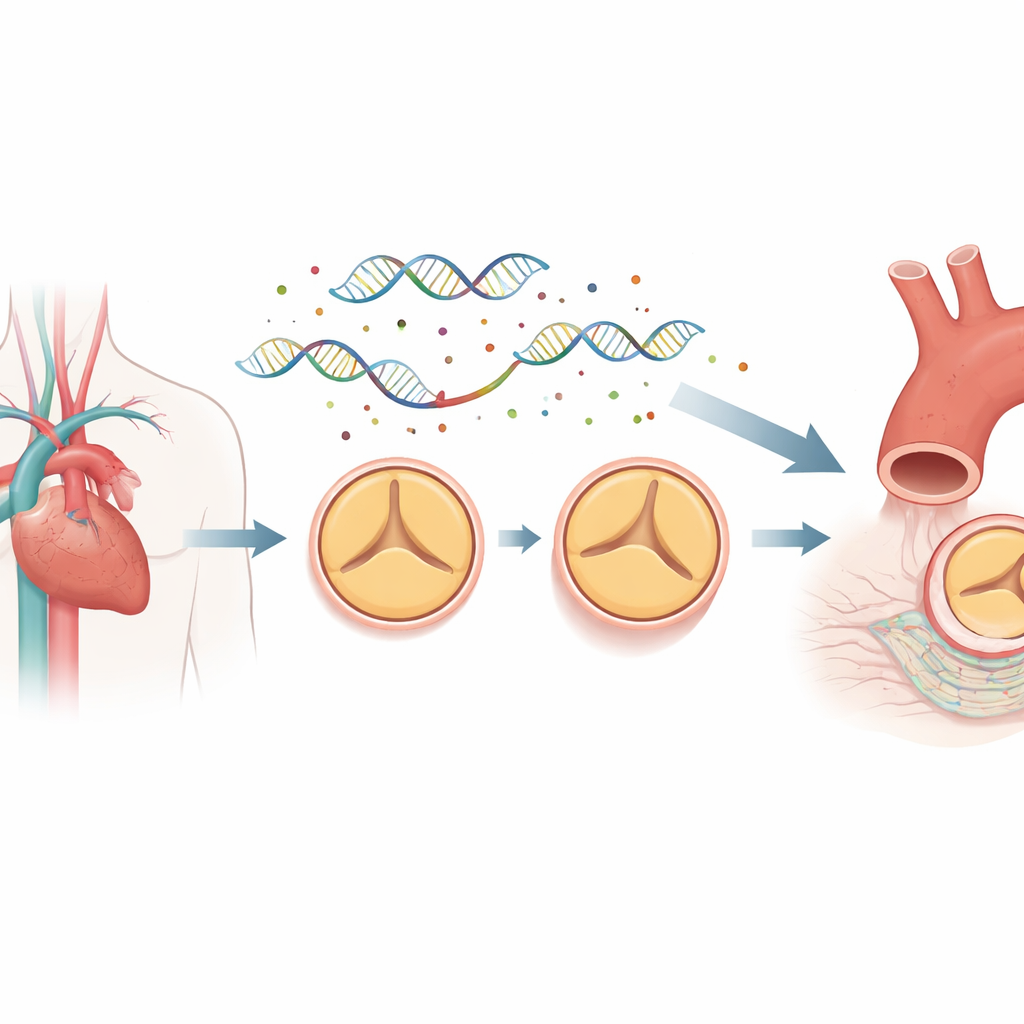
La carte de contrôle de l’ADN derrière le développement des valves
La plus grande partie de notre génome ne code pas pour des protéines. Elle contient en revanche des éléments régulateurs, tels que des enhanceurs et des promoteurs, qui agissent comme des variateurs et des câblages pour les gènes. Ces régions peuvent se situer loin des gènes qu’elles contrôlent, se rapprochant par boucles dans l’espace tridimensionnel pour entrer en contact. Pour voir en quoi ce câblage diffère entre personnes ayant une valve bicuspide et valves normales, les chercheurs ont prélevé des cellules de la paroi interne de l’aorte ascendante chez huit patients porteurs d’une valve bicuspide et huit patients présentant une valve normale à trois feuillets, tous opérés. Ils ont utilisé une technique appelée promoter capture Hi‑C pour cartographier des millions de contacts ADN à longue portée et ont combiné cela avec un séquençage du génome complet afin de localiser des mutations rares situées dans ces régions régulatrices.
Mutations rares qui reconfigurent les cellules en développement des valves
L’équipe a constaté que jusqu’à 95 % des différences génétiques entre individus se situaient dans des régions non codantes, et que les patients avec valve bicuspide présentaient bien plus de changements liés à des mutations dans les boucles d’ADN autour de gènes impliqués dans le développement valvulaire que les témoins. Plutôt que de se fier uniquement aux signaux des tissus adultes, les scientifiques ont superposé leurs cartes de câblage aux données d’expression génique en cellule unique et spatiales provenant de cœurs embryonnaires humains. Cela leur a permis de déterminer quels types cellulaires précoces subiraient l’impact des interrupteurs régulateurs altérés. Le signal le plus fort provenait des cellules mésenchymateuses qui contribuent à la formation de structures appelées coussins endocardiques — des coussinets tissulaires temporaires du cœur fœtal qui se remodelent ensuite en valves matures et en parties du tractus de sortie.
Programmes des coussins perturbés dans le cœur fœtal
En retraçant les gènes reliés aux enhanceurs et promoteurs mutés, les auteurs ont identifié 198 gènes candidats associés à la valvule aortique bicuspide, soit environ trente fois plus que ce qui était connu auparavant. Ces gènes se regroupaient dans des voies qui pilotent la transformation de cellules de revêtement aplaties en cellules invasives des coussins, un processus connu sous le nom de transition épithélium‑mésenchyme, ainsi que dans des réseaux de signalisation tels que TGF‑beta et voies apparentées. Ils ont également observé des atteintes répétées dans des sites de liaison pour une famille de protéines de contrôle apparentées à NFAT, reconnues pour leur rôle crucial dans la morphogenèse des coussins en valves matures. Des modèles informatiques de l’activité régulatrice ont soutenu l’idée que nombre de ces variants agissent spécifiquement dans les tissus cardiaques fœtaux et dans l’aorte ascendante. Ensemble, les résultats suggèrent que des mutations régulatrices rares déforment subtilement les programmes géniques des cellules mésenchymateuses formant les coussins, orientant le développement vers une valve anormale à deux feuillets.
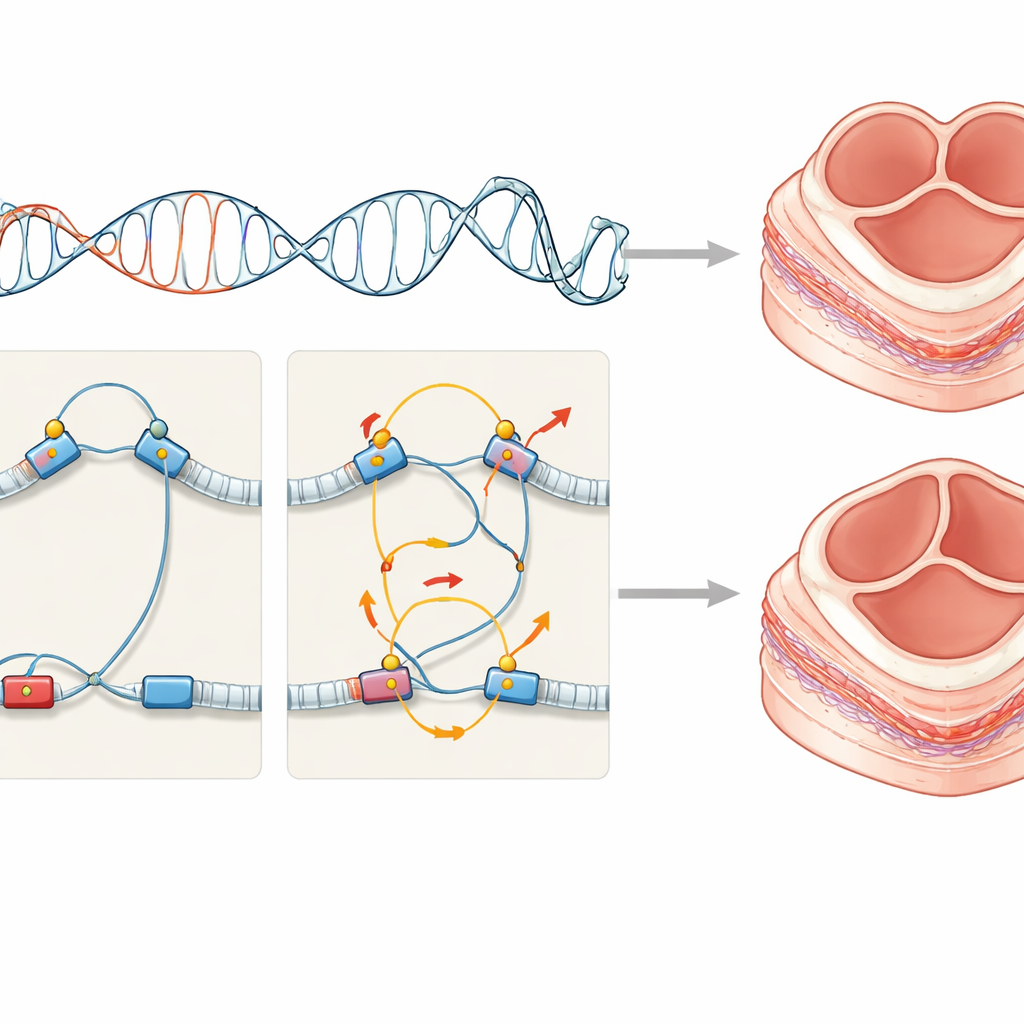
Un puzzle génétique complexe composé de nombreuses petites pièces
En examinant l’ensemble des patients, les chercheurs ont observé que chaque personne portait sa propre combinaison de modifications régulatrices rares, souvent associées à des mutations altérant des protéines, et que seule une minorité de gènes affectés était partagée entre les individus. Pourtant, ces changements divers se connectaient en un réseau protéique interactif, indiquant un thème biologique commun plutôt qu’une lésion aléatoire. Le travail montre également que certains schémas de câblage régulateur établis dès l’embryon peuvent encore être détectés dans les cellules adultes, offrant une fenêtre pratique sur des événements prénataux.
Ce que cela signifie pour les patients et les familles
Pour les non‑spécialistes, le message principal est que la valvule aortique bicuspide n’est généralement pas causée par un seul gène défectueux, mais par de nombreux changements subtils dans la façon dont les gènes sont activés pendant la formation précoce du cœur. Ces mutations régulatrices rares aident à expliquer pourquoi l’affection se transmet dans les familles tout en étant si génétiquement diverse d’une personne à l’autre. À long terme, cartographier cette couche de contrôle cachée du génome pourrait améliorer l’évaluation du risque génétique chez les proches et orienter la recherche vers de nouvelles façons de surveiller ou de traiter les personnes nées avec ce défaut valvulaire fréquent.
Citation: Zhigulev, A., Buyan, A., Lázár, E. et al. Rare regulatory mutations disrupt mesenchymal molecular programs driving endocardial cushion formation in bicuspid aortic valve. Nat Commun 17, 3587 (2026). https://doi.org/10.1038/s41467-026-71758-5
Mots-clés: valvule aortique bicuspide, développement des valves cardiaques, ADN non codant, mutations régulatrices, cellules mésenchymateuses