Clear Sky Science · he
מוטציות בקרה נדירות משבשות תכניות מולקולריות מזנכימליות המניעות יצירת כריות אנדוקרדיאליות בטריקת אאורטית בעלת שני עלים
כשהסתימות של מסתמים בלב נוצרות אחרת
טריקת אאורטה דו־עלייתית היא מום מולד נפוץ של הלב שבו המסתם הראשי שמוביל אל הגוף כולל שני עלים במקום שלושה. רבים מהאנשים עם מצב זה זקוקים בסופו של דבר לניתוח, ועדיין הרופאים אינם יכולים להסביר במלואו מדוע זה קורה או אילו בני משפחה נמצאים בסיכון הגבוה ביותר. מחקר זה חותר עמוק אל מתגי הבקרה של ה‑DNA שלנו כדי לחשוף כיצד שינויים נדירים, שקשה לאתרם, בבקרת הגנים במהלך ההתפתחות המוקדמת יכולים לסטות את בניית מסתמי הלב ולהוביל לטריקת אאורטה דו־עלייתית.
מסתם תקין לסיכון חבוי
מסתם האאורטה פועל כמו דלת בין הלב לעורק הגדול של הגוף. רוב האנשים נולדים עם שלושה עלים הנפתחים ונעשים חלק עם כל פעימה. אצל עד כ‑1.5% מהאוכלוסייה, עם זאת, המסתם כולל רק שני עלים. צורה דו־עלייתית זו עלולה להעמיס על הלב, לעודד היצרות או דליפה מסוכנת של המסתם ולחלש את האאורטה הסמוכה. מחקרי משפחה מראים שהמצב נטוע בחוזק בתורשה, אך מוטציות ידועות בחלקים המקודדים לחלבון של הגנים מסבירות רק חלק קטן מהמקרים. המחברים שיערו שהתשובות החסרות עשויות להימצא ב‑DNA שאינו מקודד, זה השולט מתי והיכן גנים נדלקים.
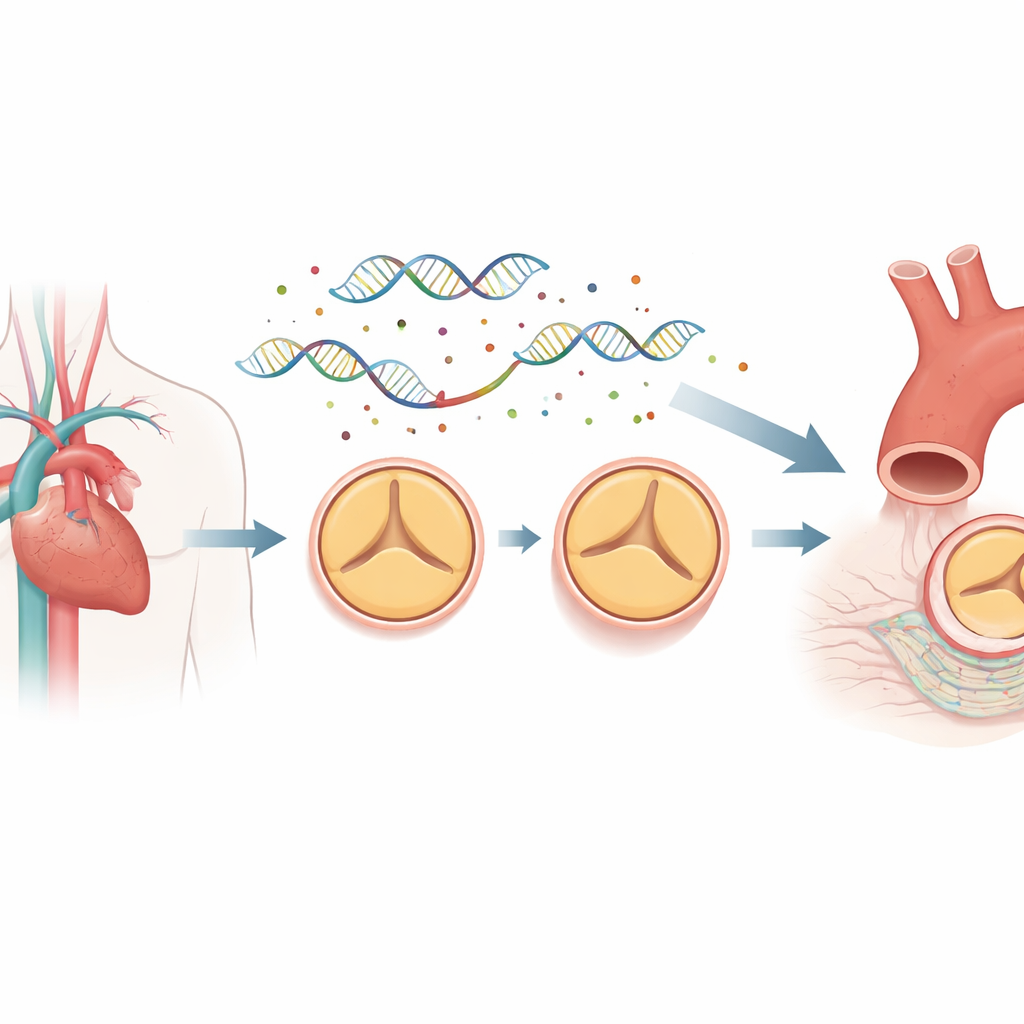
מפת הבקרה ביסוד התפתחות המסתם
חלק גדול מהגנום שלנו אינו מקודד לחלבונים. במקום זאת הוא מכיל אלמנטים רגולטוריים, כגון enhancer ו‑promoter, שפועלים כמו מעמדי עמעום וחיווט עבור גנים. אזורים אלה יכולים לשבת מרוחקים מהגנים שהם שולטים בהם, ומתעגלים במרחב תלת־ממדי כדי ליצור מגע. כדי לראות כיצד חיווט זה שונה בין אנשים עם טריקה דו־עלייתית ונורמלית, החוקרים אספו תאים מן הציפוי הפנימי של האאורטה העולה משמונה מטופלים עם טריקה דו־עלייתית ושמונה עם מסתם תלת־עלייתי תקין, כולם עוברים ניתוח. הם השתמשו בטכניקה הנקראת promoter capture Hi‑C למיפוי מיליוני מגעי DNA לטווח ארוך ושילבו זאת עם רצף גנום מלא למיקום מוטציות נדירות הנמצאות בתוך אזורים רגולטוריים אלה.
מוטציות נדירות שמשנות את חיווט תאי המסתם המתפתחים
הקבוצה מצאה שעד כ‑95% מהשונות הגנטית בין אנשים התרחשו באזורי DNA שאינם מקודדים, ושחולי טריקה דו־עלייתית הראו הרבה יותר שינויים מקושרים למוטציות בלולאות ה‑DNA סביב גנים המעורבים בהתפתחות המסתם מאשר קבוצת הביקורת. במקום להסתמך רק על אותות מרקמות בוגרות, המדענים הטילו את מפות החיווט שלהם על נתוני ביטוי גנים בתא יחיד ומרחביים מתוך לבבות עובריים אנושיים. זאת אפשרה להם לשאול אילו סוגי תאים מוקדמים ירגישו את השפעת מתגי הבקרה השונים. האות החזק ביותר הגיע מתאים מזנכימליים שתורמים למבנים שנקראים כריות אנדוקרדיאליות — ריפודי רקמה זמניים בלב העוברים שלבסוף עוברים עיצוב מחדש למסתמים הבוגרים ולחלקים של נתיב יציאת הדם.
תוכניות כריות מופרעות בלב העובר
על ידי מעקב אחרי אילו גנים היו מקושרים ל‑enhancer ו‑promoter מוטנטיים, המחברים זיהו 198 גנים מועמדים המקושרים לטריקת אאורטה דו‑עלייתית, כעשרים־ושלוש פעמים יותר מאשר עד כה. גנים אלה קיבצו במסלולים המניעים את ההמרה של תאי ציפוי שטוחים לתאי כרית פולשים, תהליך הידוע כהעברה אפיתליאלית־אל־מזנכימלית, ובנתיבי איתות כגון TGF‑beta ורשתות קשורות. הם גם ראו מטרות חזרה באתרים קשירתיים למשפחה של חלבוני בקרה שקשורים ל‑NFAT, הידועים כחיוניים לעיצוב הכריות למסתמים בוגרים. מודלים חישוביים של פעילות רגולטורית תאמו לרעיון שרבים מהשינויים האלה פועלים במיוחד ברקמת לב עוברית ובאאורטה העולה. יחדיו, התוצאות מרמזות שמוטציות רגולטוריות נדירות מעוותות בעדינות את תכניות הגנים של תאי מזנכימה יוצרים־כרית, ודוחפות את ההתפתחות לכיוון מסתם דו־עלייתי לא תקין.
פאזל גנטי מורכב עם הרבה חלקים קטנים
במבט על המטופלים, החוקרים ראו שכל אדם נשא את התערובת שלו של שינויים רגולטוריים נדירים, לעתים בשילוב עם מוטציות שמשנות חלבון, ורק מיעוט מהגנים המושפעים שותפו בין פרטים. עם זאת, שינויים מגוונים אלה התקשרו לרשת חלבונית אינטראקטיבית, מה שמצביע על נושא ביולוגי משותף במקום נזק אקראי. המחקר גם מראה שחלק מתבניות החיווט הרגולטוריות שנקבעו בעובר עדיין ניתנות לזיהוי בתאים בוגרים, ומציע צוהר שימושי לאירועים פרה־נטליים.
מה המשמעות עבור חולים ובני משפחה
ללא־מומחים, המסר המרכזי הוא שטריקת אאורטה דו־עלייתית אינה בדרך כלל תוצאה של גן יחיד פגום, אלא של רבות משנה עדינות באופן שבו גנים נדלקים במהלך יצירת הלב המוקדמת. מוטציות רגולטוריות נדירות אלה מסייעות להסביר מדוע המצב רץ במשפחות ובו־זמנית גנטית כל כך מגוון מאדם לאדם. בטווח הארוך, מיפוי שכבת הבקרה החבויה הזו של הגנום יכול לשפר הערכת סיכון גנטית לקרובי משפחה ולהנחות מחקר לפיתוח דרכים חדשות לנטר או לטפל בלידים שנולדו עם המום המסתמי הנפוץ הזה.
ציטוט: Zhigulev, A., Buyan, A., Lázár, E. et al. Rare regulatory mutations disrupt mesenchymal molecular programs driving endocardial cushion formation in bicuspid aortic valve. Nat Commun 17, 3587 (2026). https://doi.org/10.1038/s41467-026-71758-5
מילות מפתח: טריקת אאורטה דו־עלייתית, התפתחות מסתם הלב, DNA שאינו מקודד, מוטציות רגולטוריות, תאי מזנכימה