Clear Sky Science · es
Mutaciones regulatorias raras alteran programas moleculares mesenquimales que impulsan la formación de los cojines endocárdicos en la válvula aórtica bicúspide
Cuando las válvulas cardíacas se forman de manera diferente
La válvula aórtica bicúspide es un defecto congénito cardíaco frecuente en el que la principal válvula que conecta el corazón con el cuerpo tiene solo dos velos en lugar de tres. Muchas personas con esta condición acaban necesitando cirugía, pero los médicos todavía no pueden explicar por completo por qué ocurre ni qué familiares corren mayor riesgo. Este estudio explora en profundidad los interruptores de control de nuestro ADN para revelar cómo cambios raros y difíciles de detectar en la regulación génica durante el desarrollo temprano pueden desviar la construcción de las válvulas cardíacas y contribuir a la aparición de una válvula aórtica bicúspide.
De una válvula normal a un riesgo oculto
La válvula aórtica funciona como una puerta entre el corazón y la arteria más grande del cuerpo. La mayoría de las personas nacen con tres valvas que se abren y cierran suavemente con cada latido. Sin embargo, en hasta aproximadamente el 1,5 % de la población, la válvula tiene solo dos valvas. Esta forma bicúspide puede sobrecargar el corazón, favorecer un estrechamiento o fuga peligrosos de la válvula y debilitar la aorta adyacente. Los estudios familiares muestran que la condición es fuertemente heredable, pero las mutaciones conocidas en las regiones codificantes de proteínas explican solo una pequeña fracción de los casos. Los autores sospecharon que las respuestas faltantes podrían encontrarse en el ADN no codificante que controla cuándo y dónde se activan los genes.
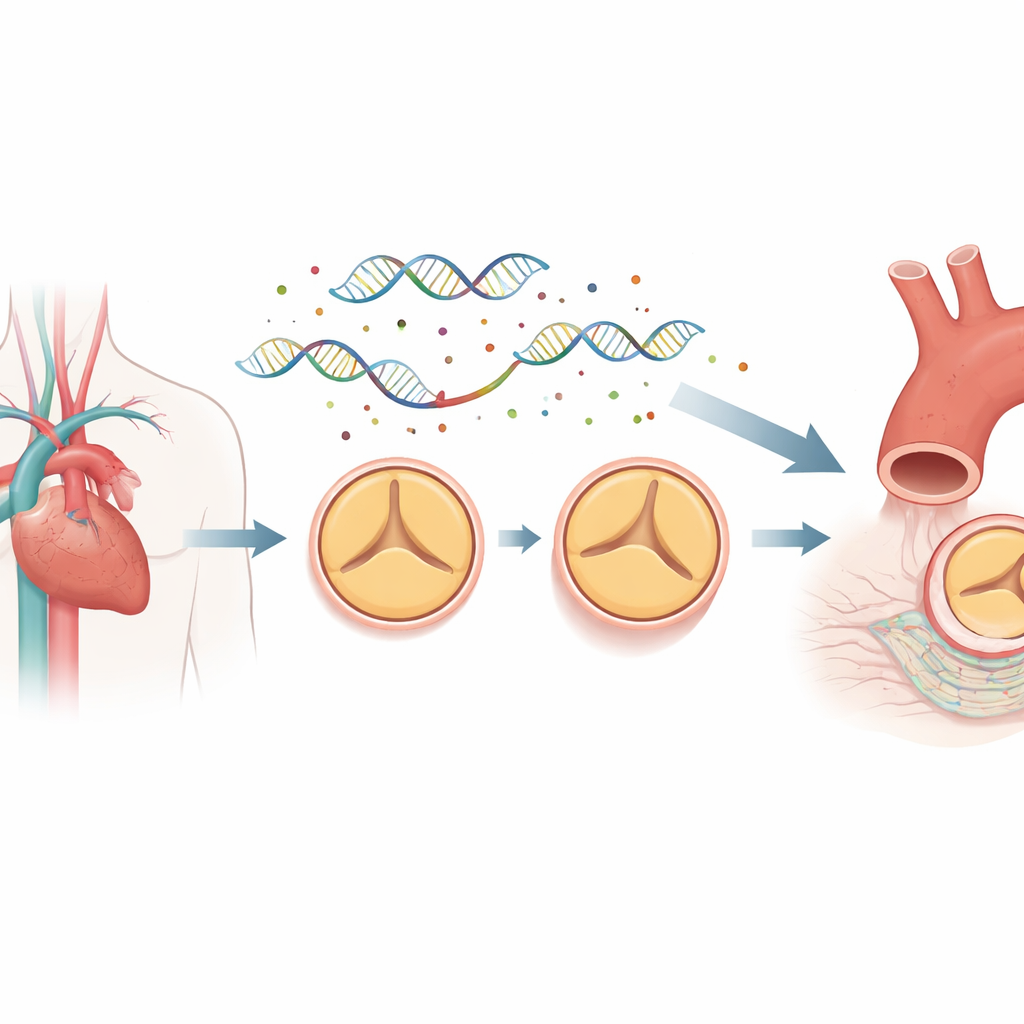
El mapa de control del ADN detrás del desarrollo valvular
La mayor parte de nuestro genoma no codifica proteínas. En su lugar contiene elementos regulatorios, como potenciadores y promotores, que actúan como atenuadores y cableado para los genes. Estas regiones pueden ubicarse lejos de los genes que controlan, plegándose en el espacio tridimensional para establecer contacto. Para ver cómo varía este cableado entre personas con válvulas bicúspides y normales, los investigadores recogieron células del revestimiento interno de la aorta ascendente de ocho pacientes con válvulas bicúspides y ocho con válvulas normales de tres valvas, todos sometidos a cirugía. Utilizaron una técnica llamada promoter capture Hi‑C para mapear millones de contactos de ADN a larga distancia y combinaron esto con secuenciación del genoma completo para localizar mutaciones raras situadas dentro de estas regiones regulatorias.
Mutaciones raras que reconfiguran las células valvulares en desarrollo
El equipo halló que hasta el 95 % de las diferencias genéticas entre personas ocurrían en regiones no codificantes, y que los pacientes con válvula bicúspide mostraban muchos más cambios vinculados a mutaciones en el enrollamiento del ADN alrededor de genes implicados en el desarrollo valvular que los controles. En lugar de basarse únicamente en señales de tejido adulto, los científicos superpusieron sus mapas de cableado con datos de expresión génica a nivel de célula única y espacial de corazones embrionarios humanos. Esto les permitió preguntar qué tipos celulares tempranos sentirían el impacto de los interruptores regulatorios alterados. La señal más fuerte procedía de células mesenquimales que contribuyen a estructuras llamadas cojines endocárdicos —almohadillas temporales de tejido en el corazón fetal que posteriormente se remodelan para formar las válvulas maduras y partes del tracto de salida.
Programas de los cojines alterados en el corazón fetal
Trazando qué genes estaban conectados a potenciadores y promotores mutados, los autores identificaron 198 genes candidatos vinculados a la válvula aórtica bicúspide, aproximadamente treinta veces más de los que se conocían antes. Estos genes se agruparon en rutas que impulsan la transformación de células del revestimiento planas en células invasivas de los cojines, un proceso conocido como transición epitelio‑mesénquima, y en vías de señalización como TGF‑beta y redes afines. También observaron impactos repetidos en sitios de unión para una familia de proteínas reguladoras relacionadas con NFAT, conocidas por ser cruciales para dar forma a los cojines y convertirlos en válvulas maduras. Modelos computacionales de la actividad regulatoria respaldaron la idea de que muchas de estas variantes actúan específicamente en tejido cardíaco fetal y en la aorta ascendente. En conjunto, los resultados sugieren que mutaciones regulatorias raras distorsionan de forma sutil los programas génicos de las células mesenquimales formadoras de cojines, empujando el desarrollo hacia una válvula anormal de dos valvas.
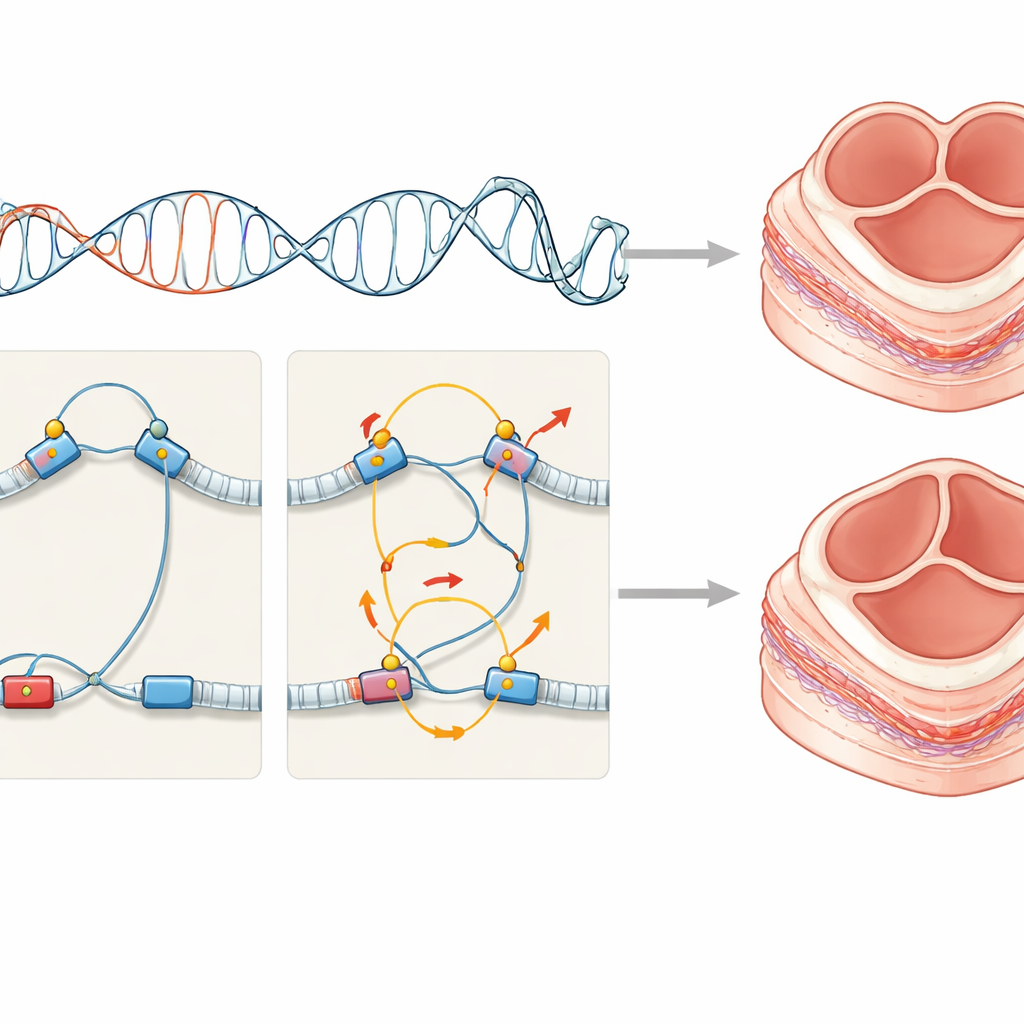
Un rompecabezas genético complejo con muchas piezas pequeñas
Al comparar entre pacientes, los investigadores vieron que cada persona portaba su propia mezcla de cambios regulatorios raros, a menudo combinados con mutaciones que alteran proteínas, y que solo una minoría de genes afectados se compartían entre individuos. Sin embargo, estos cambios diversos se conectaban en una red de proteínas interactivas, lo que apunta a un tema biológico común más que a un daño aleatorio. El trabajo también muestra que algunos patrones de cableado regulatorio establecidos inicialmente en el embrión pueden aún detectarse en células adultas, ofreciendo una ventana práctica hacia eventos prenatales.
Qué significa esto para pacientes y familias
Para el público no especializado, el mensaje principal es que la válvula aórtica bicúspide no suele deberse a un único gen defectuoso, sino a muchos cambios sutiles en cómo se activan los genes durante la formación temprana del corazón. Estas mutaciones regulatorias raras ayudan a explicar por qué la condición se transmite en familias y, a la vez, es tan diversa desde el punto de vista genético entre unas personas y otras. A largo plazo, cartografiar esta capa de control oculta del genoma podría mejorar la evaluación del riesgo genético para los parientes y orientar la investigación hacia nuevas formas de vigilar o tratar a las personas nacidas con este defecto valvular común.
Cita: Zhigulev, A., Buyan, A., Lázár, E. et al. Rare regulatory mutations disrupt mesenchymal molecular programs driving endocardial cushion formation in bicuspid aortic valve. Nat Commun 17, 3587 (2026). https://doi.org/10.1038/s41467-026-71758-5
Palabras clave: válvula aórtica bicúspide, desarrollo de válvulas cardíacas, ADN no codificante, mutaciones regulatorias, células mesenquimales