Clear Sky Science · pl
Rzadkie mutacje regulatorowe zaburzają mezynchymalne programy molekularne napędzające tworzenie poduszek wsierdziowych w zastawce aortalnej dwupłatkowej
Kiedy zastawki serca formują się inaczej
Zastawka aortalna dwupłatkowa to częsta wada wrodzona serca, w której główna zastawka od serca do organizmu ma tylko dwa płatki zamiast trzech. Wiele osób z tą przypadłością ostatecznie wymaga zabiegu chirurgicznego, jednak lekarze wciąż nie potrafią w pełni wyjaśnić, dlaczego się to zdarza ani którzy członkowie rodziny są najbardziej narażeni. To badanie zagłębia się w przełączniki kontrolne naszej DNA, aby ujawnić, jak rzadkie, trudne do wykrycia zmiany w regulacji genów podczas wczesnego rozwoju mogą błędnie ukierunkować budowę zastawek serca i prowadzić do powstania zastawki aortalnej dwupłatkowej.
Od normalnej zastawki do ukrytego ryzyka
Zastawka aortalna działa jak drzwi między sercem a największą tętnicą ciała. Większość osób rodzi się z trzema płatkami, które otwierają się i zamykają płynnie przy każdym uderzeniu serca. U do około 1,5% populacji jednak zastawka ma tylko dwa płatki. Ta dwupłatkowa budowa może obciążać serce, sprzyjać niebezpiecznemu zwężeniu lub niedomykalności zastawki oraz osłabiać pobliską aortę. Badania rodzinne pokazują, że wada jest silnie dziedziczna, lecz znane mutacje w kodujących białka częściach genów tłumaczą tylko niewielką część przypadków. Autorzy przypuszczali, że brakujące odpowiedzi mogą leżeć w niekodującym DNA, który kontroluje, kiedy i gdzie geny są włączane.
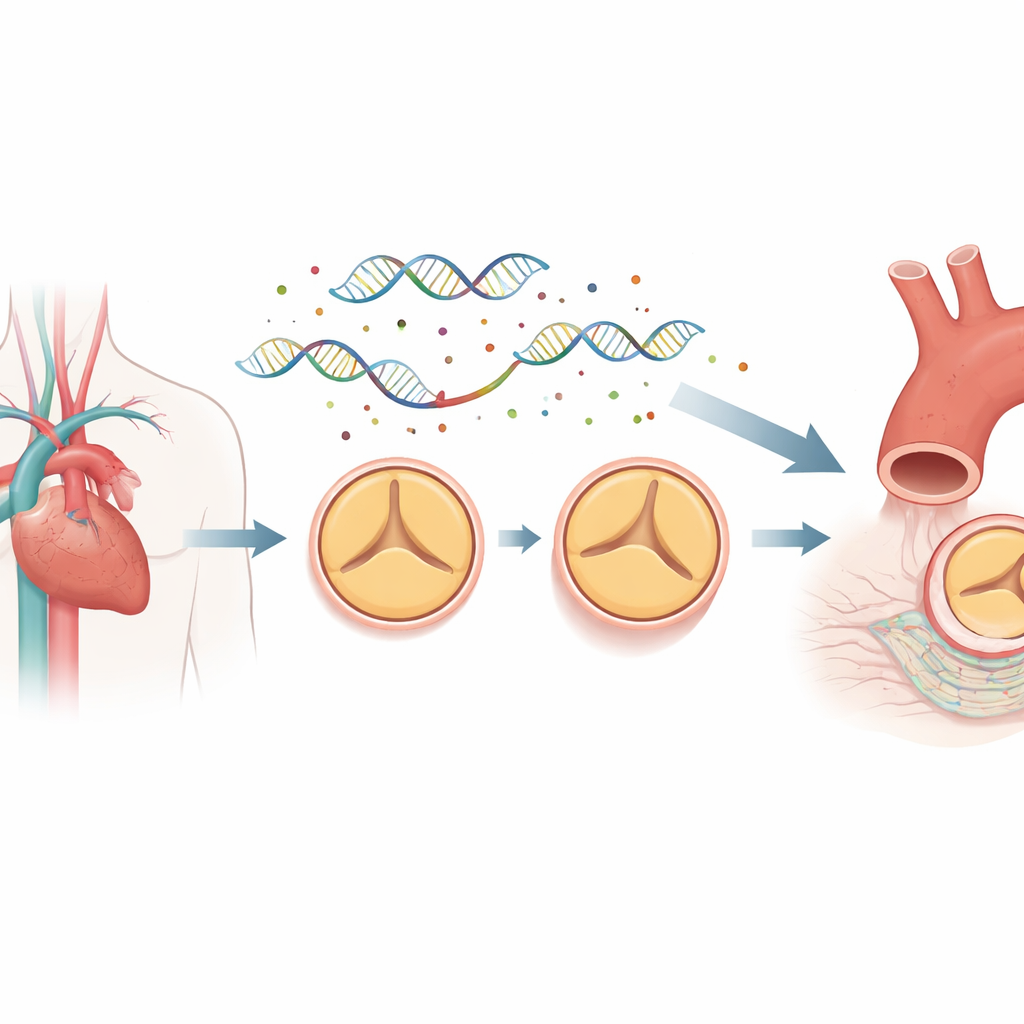
Mapa kontrolna DNA stojąca za rozwojem zastawek
Większość naszego genomu nie koduje białek. Zamiast tego zawiera elementy regulatorowe, takie jak wzmacniacze (enhancery) i promotory, które działają jak ściemniacze i okablowanie dla genów. Regiony te mogą znajdować się daleko od genów, które kontrolują, tworząc pętle w trójwymiarowej przestrzeni, aby nawiązać kontakt. Aby zobaczyć, jak to okablowanie różni się między osobami z zastawkami dwupłatkowymi a normalnymi, badacze pobrali komórki z wewnętrznej wyściółki wstępującej aorty od ośmiu pacjentów z zastawkami dwupłatkowymi i ośmiu z normalnymi, trzypłatkowymi zastawkami, wszyscy poddawani operacji. Użyli techniki zwanej promoter capture Hi‑C do mapowania milionów długozasięgowych kontaktów DNA i połączyli to z sekwencjonowaniem całego genomu, aby zlokalizować rzadkie mutacje siedzące w tych regionach regulatorowych.
Rzadkie mutacje, które przepiętrzają komórki rozwijającej się zastawki
Zespół odkrył, że do 95% różnic genetycznych między ludźmi występuje w regionach niekodujących, i że pacjenci z zastawkami dwupłatkowymi wykazywali znacznie więcej zmian powiązanych z mutacjami w pętlach DNA wokół genów zaangażowanych w rozwój zastawek niż kontrolni. Zamiast polegać wyłącznie na sygnałach z tkanki dorosłej, naukowcy nałożyli swoje mapy okablowania na dane o ekspresji genów w skali pojedynczych komórek i w przestrzeni pochodzące z ludzkich zarodkowych serc. Pozwoliło im to zapytać, które wczesne typy komórek odczułyby wpływ zmienionych przełączników regulatorowych. Najsilniejszy sygnał pochodził od komórek mezenchymalnych, które uczestniczą w tworzeniu struktur zwanych poduszkami wsierdziowymi — tymczasowych poduszek tkankowych w sercu płodowym, które później przekształcają się w dojrzałe zastawki serca i części pnia tętniczego.
Zakłócone programy poduszek w sercu płodowym
Śledząc, które geny były połączone z wymienionymi mutowanymi enhancerami i promotorami, autorzy zidentyfikowali 198 kandydatów na geny związane z zastawką aortalną dwupłatkową, około trzydzieści razy więcej niż wcześniej znano. Geny te skupiały się w szlakach napędzających przemianę płaskich komórek wyściółki w komórki inwazyjne poduszek, proces znany jako przejście epitelialno‑mezenchymalne (epithelial‑to‑mesenchymal transition), oraz w szlakach sygnalizacyjnych takich jak TGF‑beta i powiązane sieci. Zaobserwowano także powtarzające się trafienia w miejsca wiązania dla rodziny białek regulatorowych powiązanych z NFAT, znanych z kluczowej roli w kształtowaniu poduszek w dojrzałe zastawki. Modele komputerowe aktywności regulatorowej wspierały koncepcję, że wiele z tych wariantów działa specyficznie w tkance serca płodowego i wstępującej aorcie. Razem wyniki sugerują, że rzadkie mutacje regulatorowe subtelnie zniekształcają programy genowe komórek mezenchymalnych formujących poduszki, popychając rozwój w kierunku nieprawidłowej zastawki dwupłatkowej.
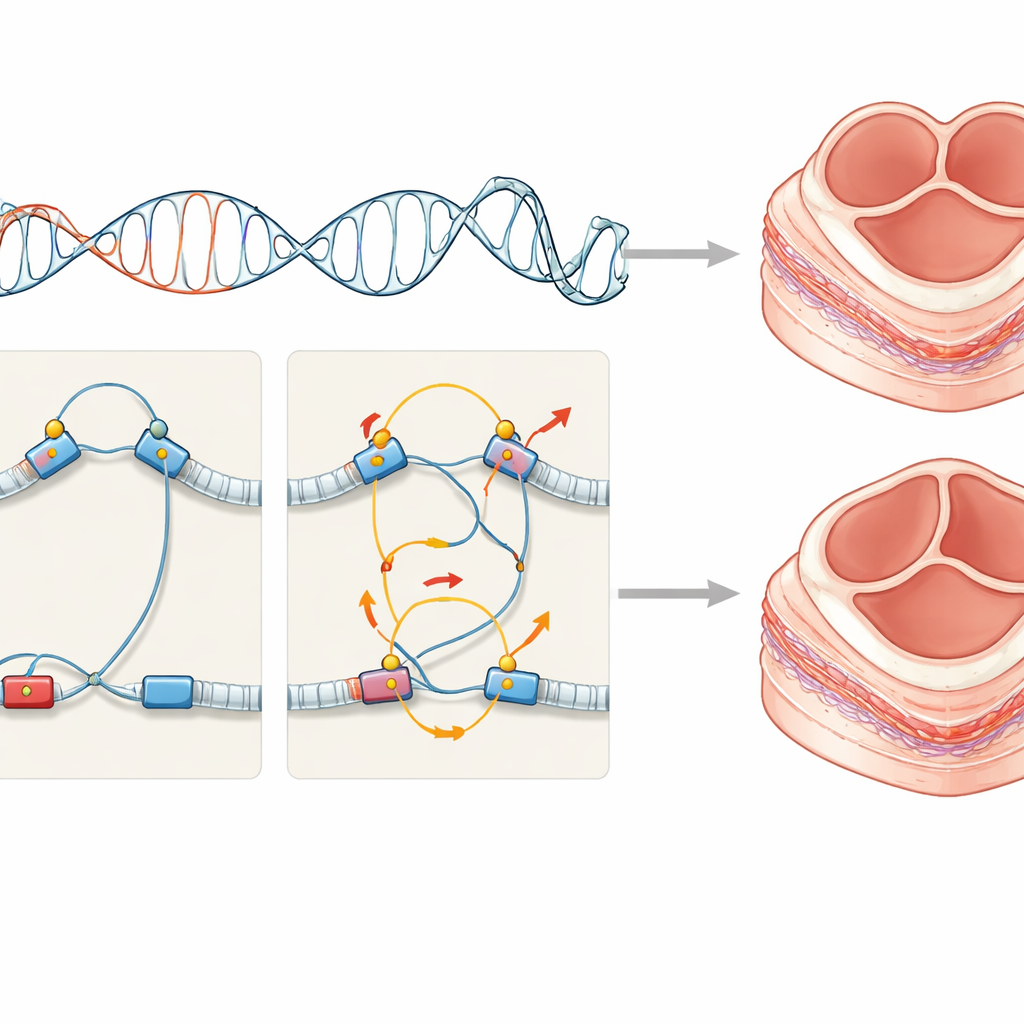
Złożona zagadka genetyczna z wieloma drobnymi elementami
Analizując pacjentów, badacze zauważyli, że każda osoba nosiła własną mieszankę rzadkich zmian regulatorowych, często w połączeniu z mutacjami zmieniającymi białka, i że tylko mniejszość dotkniętych genów była wspólna między osobnikami. Mimo to te zróżnicowane zmiany łączyły się w sieć interakcji białkowych, wskazując na wspólny motyw biologiczny zamiast przypadkowego uszkodzenia. Praca pokazuje również, że niektóre wzorce okablowania regulatorowego ustalone w embrionie można nadal wykryć w komórkach dorosłych, co daje praktyczne okno na wydarzenia prenatalne.
Co to oznacza dla pacjentów i rodzin
Dla osób niebędących specjalistami główne przesłanie jest takie, że zastawka aortalna dwupłatkowa zwykle nie jest powodowana przez jeden wadliwy gen, lecz przez wiele subtelnych zmian w tym, jak geny są włączane podczas wczesnego formowania serca. Te rzadkie mutacje regulatorowe pomagają wyjaśnić, dlaczego wada występuje w rodzinach, a jednocześnie jest tak genetycznie zróżnicowana u poszczególnych osób. W dłuższej perspektywie mapowanie tej ukrytej warstwy kontroli genomu może poprawić ocenę ryzyka genetycznego dla krewnych i ukierunkować badania nad nowymi sposobami monitorowania lub leczenia osób urodzonych z tą częstą wadą zastawki.
Cytowanie: Zhigulev, A., Buyan, A., Lázár, E. et al. Rare regulatory mutations disrupt mesenchymal molecular programs driving endocardial cushion formation in bicuspid aortic valve. Nat Commun 17, 3587 (2026). https://doi.org/10.1038/s41467-026-71758-5
Słowa kluczowe: zastawka aortalna dwupłatkowa, rozwój zastawek serca, DNA niekodujące białek, mutacje regulatorowe, komórki mezenchymalne