Clear Sky Science · nl
Zeldzame regulerende mutaties verstoren mesenchymale moleculaire programma's die endocardiale kussenvorming aandrijven bij bicuspidale aortaklep
Wanneer hartkleppen zich anders vormen
De bicuspidale aortaklep is een veelvoorkomend aangeboren hartafwijking waarbij de belangrijkste hartklep naar het lichaam twee slagen heeft in plaats van drie. Veel mensen met deze aandoening hebben uiteindelijk operatief ingrijpen nodig, maar artsen kunnen nog steeds niet volledig verklaren waarom het voorkomt of welke familieleden het meest risico lopen. Deze studie gaat diep in op de schakelaars in ons DNA om te onthullen hoe zeldzame, moeilijk te zien veranderingen in genregulatie tijdens de vroege ontwikkeling het bouwen van hartkleppen kunnen misleiden en kunnen bijdragen aan het ontstaan van een bicuspidale aortaklep.
Van normale klep naar verborgen risico
De aortaklep werkt als een deur tussen het hart en de grootste lichaamsslagader. De meeste mensen worden geboren met drie slippen die bij elke hartslag soepel openen en sluiten. Bij maximaal ongeveer 1,5% van de bevolking heeft de klep echter slechts twee slippen. Deze bicuspide vorm kan het hart belasten, gevaarlijke vernauwing of lekkage van de klep bevorderen en de nabijgelegen aorta verzwakken. Familieonderzoeken tonen aan dat de aandoening sterk erfelijk is, maar bekende mutaties in de eiwitcoderende delen van genen verklaren slechts een klein deel van de gevallen. De auteurs vermoedden dat de ontbrekende antwoorden te vinden zijn in het niet-coderende DNA dat regelt wanneer en waar genen aan gaan.
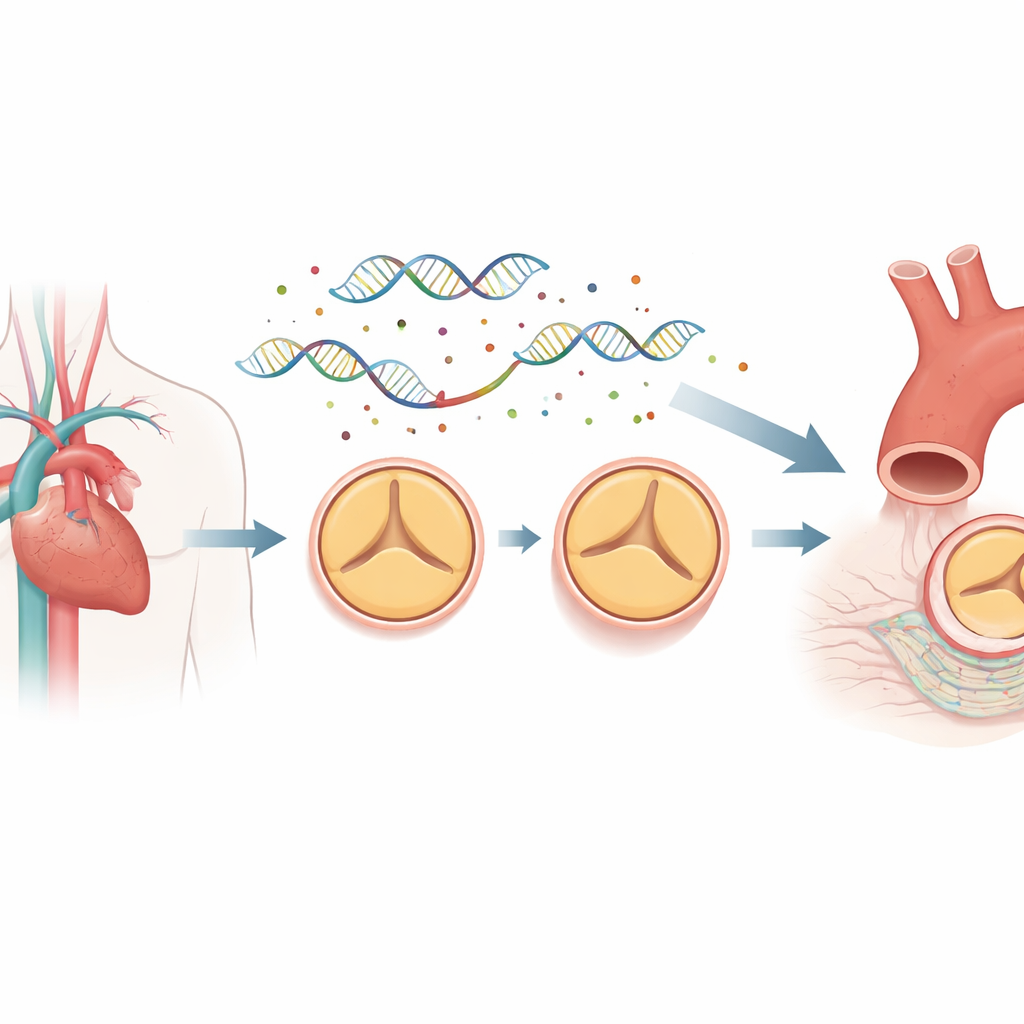
De DNA-regelkaart achter klepontwikkeling
Het grootste deel van ons genoom codeert niet voor eiwitten. In plaats daarvan bevat het regulatorische elementen, zoals enhancers en promoters, die functioneren als dimmers en bedrading voor genen. Deze regio’s kunnen ver van de genen die ze controleren liggen en door driedimensionale vouwing contact maken. Om te zien hoe deze bedrading verschilt tussen mensen met bicuspide en normale kleppen, verzamelden de onderzoekers cellen van de binnenbekleding van de opgaande aorta van acht patiënten met bicuspide kleppen en acht met normale driezijdige kleppen, allen tijdens operaties. Ze gebruikten een techniek genaamd promoter capture Hi-C om miljoenen langafstand-DNA-contacten in kaart te brengen en combineerden dit met whole-genome sequencing om zeldzame mutaties binnen deze regulatorische regio’s te lokaliseren.
Zeldzame mutaties die zich ontwikkelende klepcellen herschakelen
Het team ontdekte dat tot 95% van de genetische verschillen tussen mensen zich in niet-coderende regio’s voordeed, en dat patiënten met bicuspide kleppen veel meer mutatie-gekoppelde veranderingen in DNA-lusvorming rond genen betrokken bij klepontwikkeling vertoonden dan controles. In plaats van alleen te vertrouwen op signalen uit volwassen weefsel, legden de wetenschappers hun bedradingkaarten over single-cell en ruimtelijke genexpressiegegevens van menselijke embryonale harten. Dit stelde hen in staat te vragen welke vroege celtypen de impact van de veranderde regelknoppen zouden voelen. Het sterkste signaal kwam van mesenchymale cellen die bijdragen aan structuren die endocardiale kussens worden genoemd—tijdelijke weefselkussentjes in het foetale hart die later worden omgevormd tot de rijpe hartkleppen en delen van het uitstroombaan.
Verstoorde kussenprogramma's in het foetale hart
Door te volgen welke genen verbonden waren met gemuteerde enhancers en promoters, identificeerden de auteurs 198 kandidaatgenen die geassocieerd zijn met bicuspide aortaklep, ongeveer dertig keer meer dan eerder bekend. Deze genen clusteren in routes die de transformatie aandrijven van platte bekledingcellen naar invasieve kussencellen, een proces dat bekendstaat als epitheel-naar-mesenchymale transitie, en in signaalroutes zoals TGF-beta en verwante netwerken. Ze zagen ook herhaalde treffers in bindingsplaatsen voor een familie van regelproteïnen gerelateerd aan NFAT, waarvan bekend is dat ze cruciaal zijn voor het vormen van kussens tot rijpe kleppen. Computermodellen van regulerende activiteit ondersteunden het idee dat veel van deze varianten specifiek in foetaal hartweefsel en in de opgaande aorta werkzaam zijn. Gezamenlijk suggereren de resultaten dat zeldzame regulerende mutaties de genprogramma's van kussenvormende mesenchymale cellen subtiel vervormen, en zo de ontwikkeling richting een abnormale tweeslippige klep duwen.
Een complex genetisch puzzel met veel kleine stukjes
Over de patiënten heen zagen de onderzoekers dat elke persoon zijn eigen mix van zeldzame regulerende veranderingen droeg, vaak gecombineerd met eiwitveranderende mutaties, en dat slechts een minderheid van de aangedane genen tussen individuen werd gedeeld. Toch vormden deze diverse veranderingen een interactief eiwitnetwerk, wat wijst op een gemeenschappelijk biologisch thema in plaats van willekeurige schade. Het werk toont ook aan dat sommige regulatorische bedradingpatronen die in het embryo zijn vastgesteld nog steeds in volwassen cellen detecteerbaar zijn, wat een praktische inkijk geeft in prenatale gebeurtenissen.
Wat dit betekent voor patiënten en families
Voor niet-specialisten is de belangrijkste boodschap dat de bicuspide aortaklep meestal niet wordt veroorzaakt door één kapot gen, maar door veel subtiele veranderingen in hoe genen worden aangezet tijdens vroege hartvorming. Deze zeldzame regulerende mutaties helpen verklaren waarom de aandoening in families voorkomt maar genetisch zo divers is tussen verschillende mensen. Op de lange termijn kan het in kaart brengen van deze verborgen regellaag van het genoom de genetische risicobeoordeling voor familieleden verbeteren en onderzoek sturen naar nieuwe manieren om mensen met dit veelvoorkomende klepdefect te monitoren of te behandelen.
Bronvermelding: Zhigulev, A., Buyan, A., Lázár, E. et al. Rare regulatory mutations disrupt mesenchymal molecular programs driving endocardial cushion formation in bicuspid aortic valve. Nat Commun 17, 3587 (2026). https://doi.org/10.1038/s41467-026-71758-5
Trefwoorden: bicuspidale aortaklep, hartklepontwikkeling, niet-coderend DNA, regulerende mutaties, mesenchymale cellen