Clear Sky Science · zh
周细胞是器官特异性的组织形态发生调控者
支持细胞如何悄然塑造生长中的器官
体内每个器官都布满了输送氧气和营养的小血管。但这些血管不仅仅是血液通道。该研究揭示了一类围绕毛细血管的、鲜为人知的支持细胞——周细胞,如何通过局部化学信号帮助肺和大脑在出生后成熟时构建恰当的结构。
血管旁的隐形帮手
血管由内皮细胞衬里,这些细胞不仅形成血流通道,还释放信号以指导附近细胞在器官生长和修复过程中的行为。周细胞紧贴小血管附着,众所周知它们能维持血管壁稳定。但到目前为止,它们在塑造整体组织方面的更广泛作用尚不清楚。研究人员利用小鼠的先进基因工具,有选择地关闭周细胞产生的特定信号分子,然后追踪肺和脑的发育变化。他们的工作表明,周细胞并非通用的辅助者;相反,它们以器官特异性的方式行事,并在不同组织中与不同的邻近细胞“对话”。
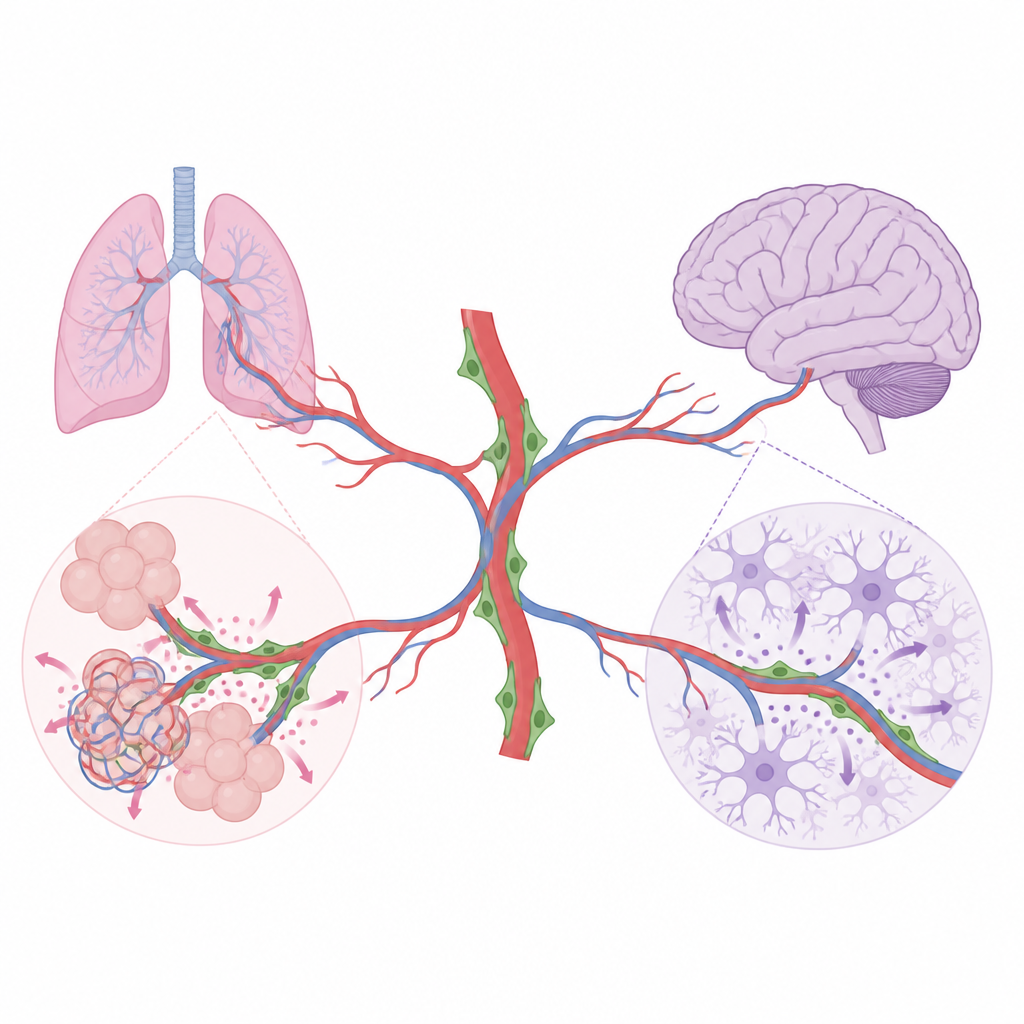
构建健康肺的周细胞信息
在发育中的肺中,肺泡必须大量形成并与毛细血管紧密交织,以便气体交换高效进行。研究团队发现,肺周细胞产生两种重要的生长因子:HGF 和 BDNF。当仅在周细胞中去除 HGF 时,衬里肺泡的小型“类干”Ⅱ型细胞增殖减少,成熟的表面衬里细胞生成也变少。肺泡变得更大、更简化,总体容积减小,尽管年轻小鼠的基本呼吸仍然足够。当从周细胞中去除 BDNF 时,肺毛细血管生长不良,内皮细胞分裂减少,肺泡空间同样变大。随后的实验显示,来自周细胞的 BDNF 激活肺内皮细胞上的其配体受体,帮助驱动血管网络的扩展,而这对正常肺泡形成是必需的。
脑发育的不同规则
相同的周细胞信号并非在所有地方都重要。在大脑中,周细胞产生很少或几乎不产生 HGF 和 BDNF,在壁细胞中关闭这些分子并未检测到血管密度、屏障紧密性或邻近神经支持细胞行为的变化。相反,脑周细胞依赖于另一种信号蛋白,称为 Nodal。当在出生后特异性阻断这些周细胞的 Nodal 产生时,脑毛细血管未能正常扩展,并出现血液成分向脑组织的轻微渗漏。与培养的小鼠脑内皮细胞的体外试验表明,Nodal 能通过一个已知的信号通路直接促进它们的增殖和迁移,支持其作为脑微血管促生长信号的作用。
保持脑支持细胞的平衡
缺失周细胞来源的 Nodal 还有另一个显著影响:它使关键的脑支持细胞进入应激状态。星形胶质细胞——这些包绕血管并帮助维持血脑屏障的星形细胞,出现肥大并表达更高水平与损伤反应相关的标志物。小胶质细胞,脑内的固有免疫细胞,呈现更活化的形态并开启与炎症相关的基因表达。单细胞 RNA 测序证实,没有 Nodal 时小胶质细胞朝更促炎的谱系转变,星形胶质细胞展示出反应性分子的特征。在培养中,对分离的星形胶质细胞和小胶质细胞补充 Nodal 能激活相同的细胞内信号开关并抑制若干活化标志,提示周细胞来源的 Nodal 通常有助于使这些支持细胞及脑环境保持更平静、更具保护性的状态。
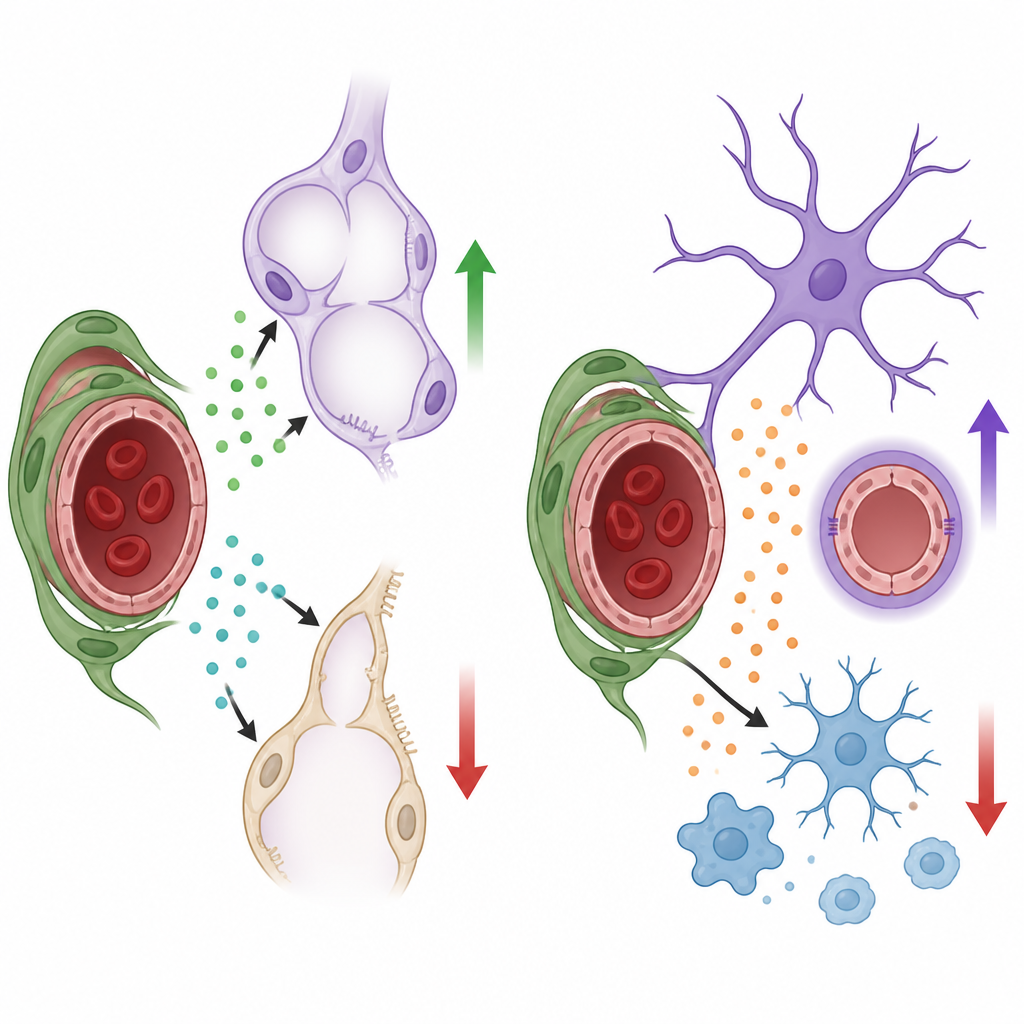
这对器官健康意味着什么
总体而言,这些发现表明周细胞使用器官特异性的生长因子“词汇”,来引导发育:在肺中,它们通过 HGF 和 BDNF 促进肺泡和血管的形成;而在脑中,它们通过 Nodal 促进血管生长并抑制炎性反应。周细胞并非被动的结构支撑,而是作为局部信号枢纽,根据每个器官的需要调整血管行为和邻近细胞的反应。理解这些隐秘的对话可能为将来支持早产儿肺成熟、保护疾病状态下的大脑屏障或在不扰动重要血流的情况下微调神经疾病中的炎症提供策略。
引用: Rasouli, S.J., Kruse, K., Diéguez-Hurtado, R. et al. Pericytes are organ-specific regulators of tissue morphogenesis. Nat Commun 17, 4229 (2026). https://doi.org/10.1038/s41467-026-71643-1
关键词: 周细胞, 肺发育, 脑血管, 血管分泌信号, 神经炎症