Clear Sky Science · ru
Перициты — органоспецифические регуляторы морфогенеза тканей
Как клетки поддержки незаметно формируют растущие органы
Каждый орган пронизан крошечными кровеносными сосудами, доставляющими кислород и питательные вещества. Но эти сосуды выполняют не только транспортную функцию. В этом исследовании показано, как малознакомая группа клеток поддержки, обвивающих капилляры — перициты — посылает локальные химические сигналы, помогающие лёгким и мозгу выстраивать нужные структуры по мере их созревания после рождения.
Скрытые помощники вдоль сосудов
Кровеносные сосуды выстланы эндотелиальными клетками, которые не только формируют трубки для кровотока, но и выделяют сигналы, направляющие соседние клетки во время роста органов и их восстановления. Перициты плотно прилегают к мелким сосудам и известны своей ролью в поддержании стабильности сосудистой стенки. До сих пор их более широкая роль в формировании тканей оставалась неясной. Используя современные генетические методы у мышей, исследователи выборочно отключали определённые сигнальные молекулы, вырабатываемые перицитами, а затем отслеживали изменения в развитии лёгких и мозга. Их работа показывает, что перициты не являются универсальными помощниками; напротив, они действуют по-разному в каждом органе и общаются с разными соседними клетками в каждой ткани.
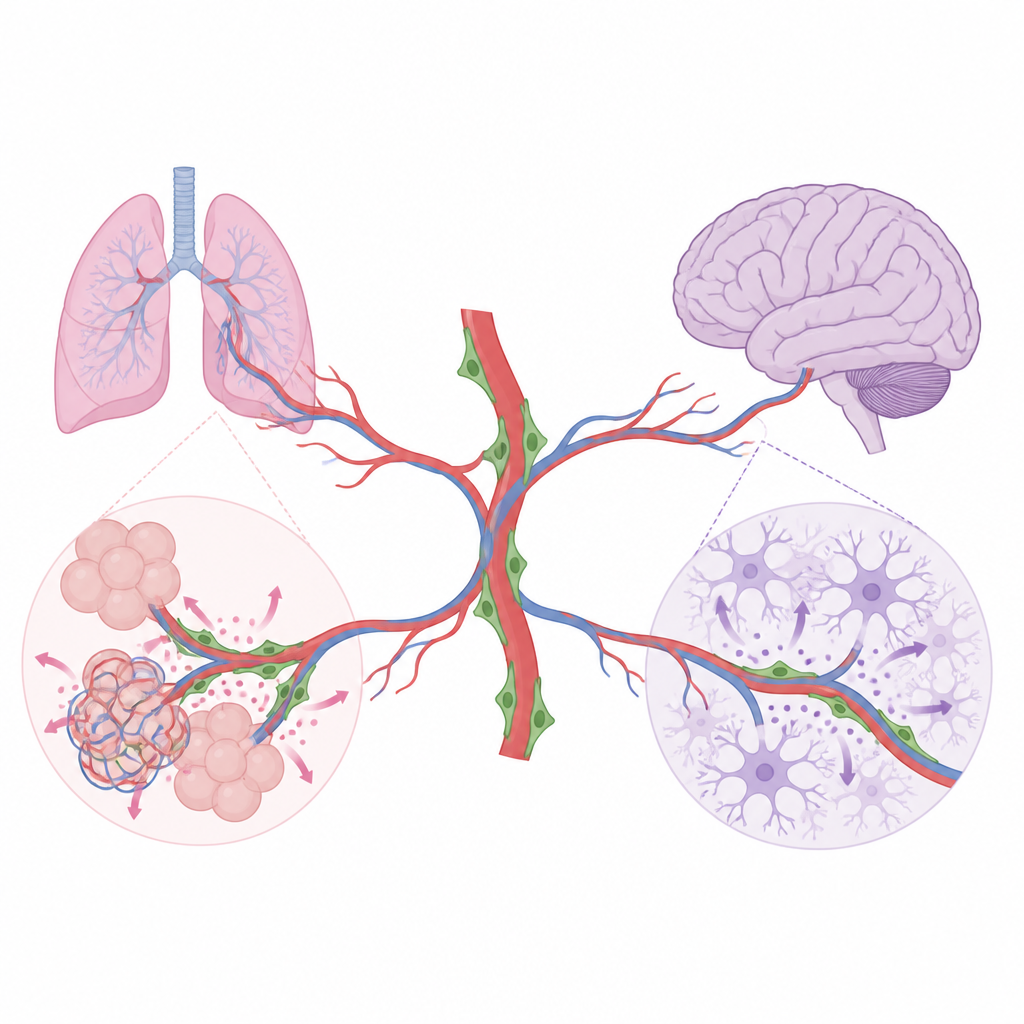
Сообщения перицитов, которые формируют здоровые лёгкие
В развивающемся лёгком альвеолы должны образоваться в большом количестве и тесно переплетаться с капиллярами, чтобы газообмен работал эффективно. Группа обнаружила, что перициты лёгкого продуцируют два важных фактора роста — HGF и BDNF. Когда HGF был удалён только из перицитов, малые «стволовоподобные» альвеолярные клетки типа 2, выстилающие альвеолы, реже размножались и давали меньше зрелых поверхностных клеток. Лёгкие имели большие, упрощённые пространства альвеол и уменьшенный общий объём, хотя базовое дыхание у молодых мышей оставалось достаточным. При удалении BDNF из перицитов капилляры лёгкого плохо росли, эндотелиальные клетки делились реже, и альвеолярные пространства снова расширялись. Последующие эксперименты показали, что BDNF от перицитов активирует свой рецептор на эндотелиальных клетках лёгкого, способствуя расширению сосудистой сети, необходимой для нормального формирования альвеол.
Другие правила для роста мозга
Те же перицитарные сигналы оказались неважными повсюду. В мозге перициты продуцировали мало или не продуцировали HGF и BDNF, и отключение этих молекул в муральных клетках не вызывало заметных изменений в плотности сосудов, проницаемости барьера или поведении соседних нервоподдерживающих клеток. Вместо этого мозговые перициты полагались на другой сигнал — белок под названием Nodal. Когда после рождения синтез Nodal в этих перицитах был блокирован, капилляры мозга не смогли нормально расшириться, и возникла тонкая утечка компонентов крови в ткань мозга. Исследования в культуре с эндотелиальными клетками мозга мыши показали, что Nodal прямо стимулирует их рост и миграцию через хорошо известный сигнальный путь, подтверждая его роль как про-ростового фактора для микрососудов мозга.
Поддержание баланса мозговых клеток поддержки
Потеря Nodal, вырабатываемого перицитами, имела ещё один заметный эффект: она переводила ключевые клетки поддержки мозга в состояние стресса. Астроциты, звездообразные клетки, обвивающие сосуды и помогающие поддерживать гематоэнцефалический барьер, стали гипертрофированными и выражали более высокие уровни маркёров, связанных с реактивными ответами на повреждение. Микроглия, резидентные иммунные клетки мозга, приобрела более активные формы и включила гены, связанные с воспалением. Секвенирование РНК по отдельным клеткам подтвердило, что без Nodal микроглия смещается в более провоспалительный профиль, а астроциты демонстрируют молекулярную подпись реактивности. В культуре добавление Nodal к изолированным астроцитам и микроглии активировало тот же внутренний сигнальный переключатель и снижало несколько маркёров активации, что указывает на то, что перицитарный Nodal обычно помогает удерживать эти клетки поддержки и среду мозга в более спокойном, защитном состоянии.
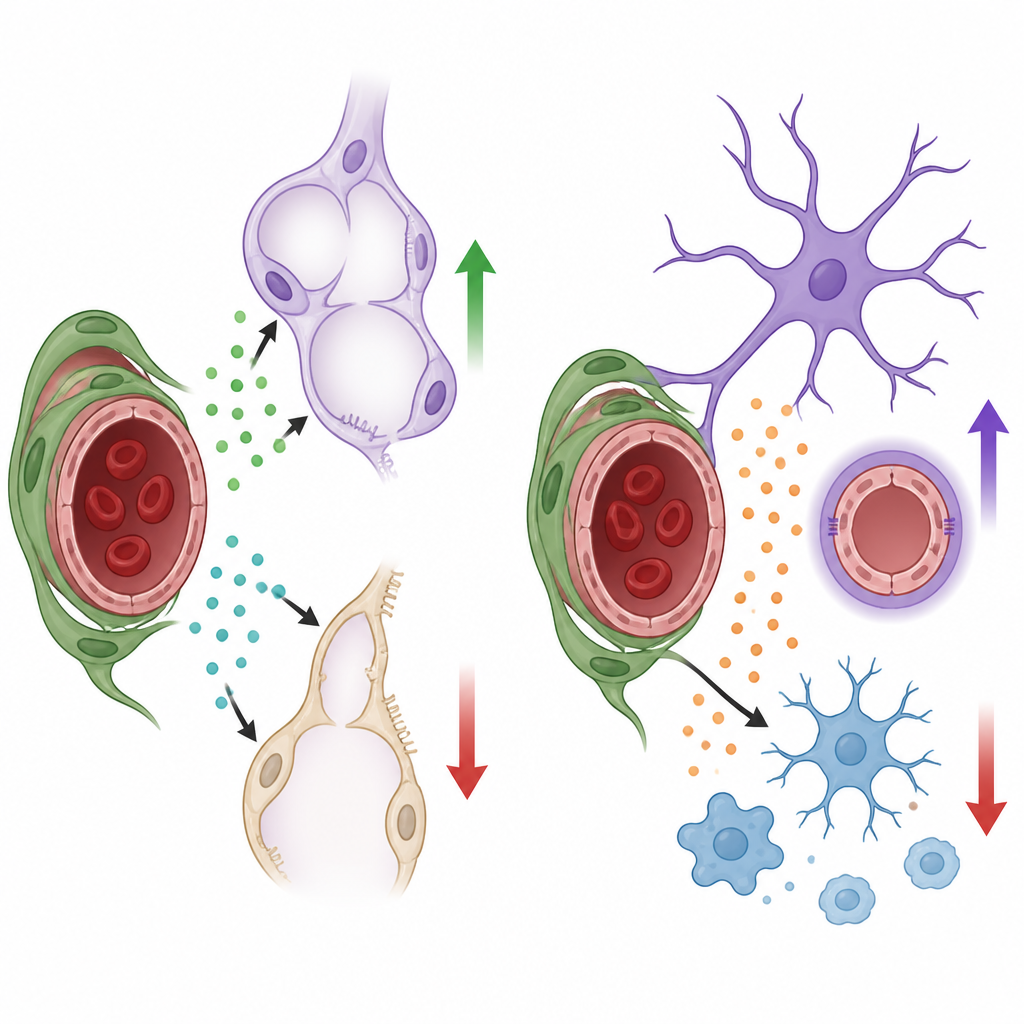
Что это значит для здоровья органов
В совокупности результаты демонстрируют, что перициты используют органоспецифические «лексиконы» факторов роста для управления развитием: в лёгких они стимулируют формирование альвеол и сосудов через HGF и BDNF, тогда как в мозге они способствуют росту сосудов и сдерживают воспалительные реакции через Nodal. Вместо того чтобы выступать пассивными структурными опорами, перициты функционируют как локальные сигнальные узлы, адаптирующие поведение кровеносных сосудов и ответы соседних клеток под потребности каждого органа. Понимание этих скрытых «разговоров» может помочь в разработке стратегий поддержки созревания лёгких у недоношенных детей, защите барьера мозга при заболеваниях или точной модуляции воспаления при неврологических расстройствах без нарушения жизненно важного кровообращения.
Цитирование: Rasouli, S.J., Kruse, K., Diéguez-Hurtado, R. et al. Pericytes are organ-specific regulators of tissue morphogenesis. Nat Commun 17, 4229 (2026). https://doi.org/10.1038/s41467-026-71643-1
Ключевые слова: перициты, развитие лёгких, сосудистая система мозга, ангиокринная сигнализация, нейровоспаление