Clear Sky Science · de
Perizyten sind organspezifische Regulatoren der Gewebemorphogenese
Wie Stützzellen still und leise wachsende Organe formen
Jedes Organ im Körper ist von feinen Blutgefäßen durchzogen, die Sauerstoff und Nährstoffe liefern. Doch diese Gefäße transportieren nicht nur Blut. Die Studie zeigt, wie eine weniger bekannte Gruppe von Stützzellen, die Kapillaren eng umhüllen — Perizyten — lokale chemische Signale aussendet, die Lungen und Gehirne dabei helfen, nach der Geburt die richtigen Strukturen auszubilden.
Die verborgenen Helfer entlang der Blutgefäße
Blutgefäße sind von Endothelzellen ausgekleidet, die nicht nur Röhren für den Blutfluss bilden, sondern auch Signale freisetzen, die benachbarte Zellen während des Organwachstums und der Reparatur lenken. Perizyten sitzen dicht an kleinen Gefäßen und sind dafür bekannt, die Gefäßwände stabil zu halten. Ihre weiterreichende Rolle bei der Formung ganzer Gewebe war bisher unklar. Mit fortschrittlichen genetischen Werkzeugen in Mäusen schalteten die Forscher gezielt bestimmte von Perizyten produzierte Signalmoleküle aus und verfolgten, wie sich Lungen- und Gehirnentwicklung veränderten. Ihre Arbeit zeigt, dass Perizyten keine generischen Helfer sind; vielmehr agieren sie organspezifisch und kommunizieren in jedem Gewebe mit unterschiedlichen Nachbarzellen.
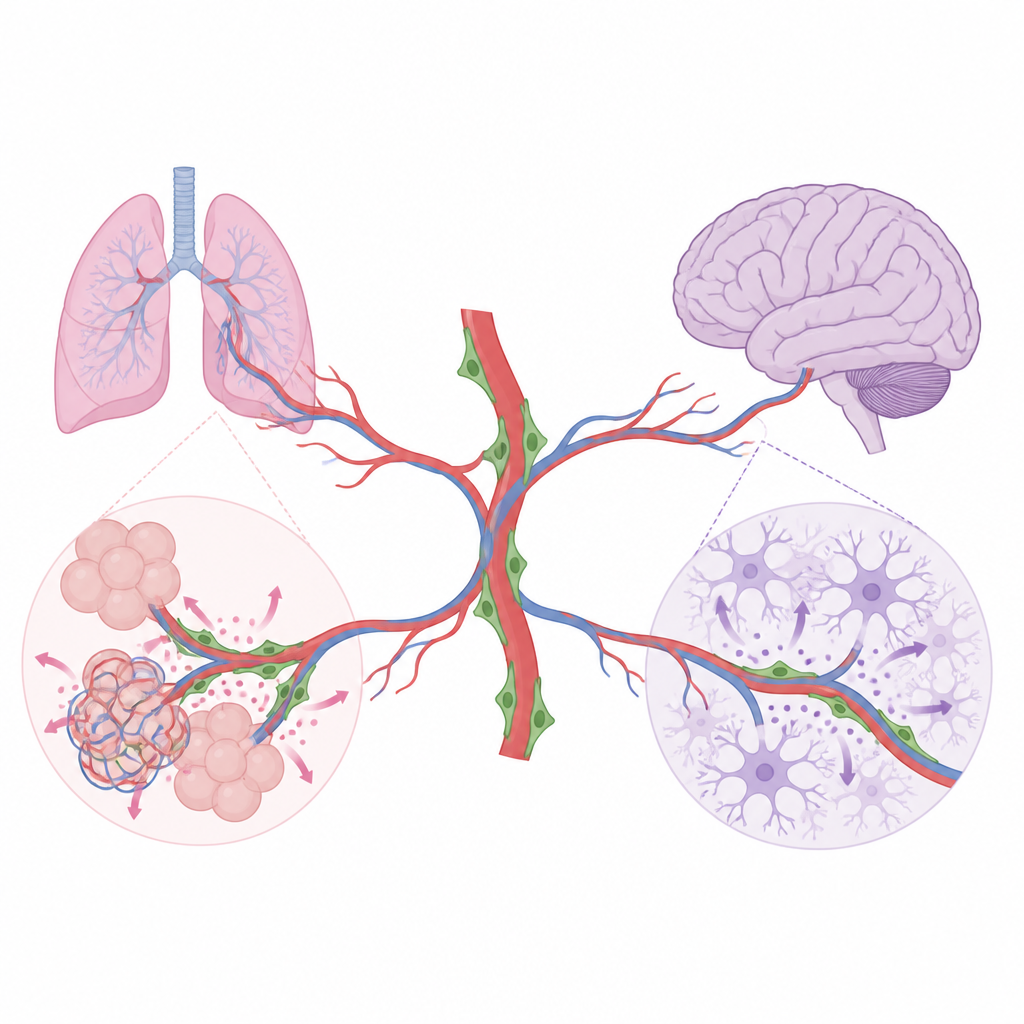
Perizyten-Botschaften, die gesunde Lungen aufbauen
In der sich entwickelnden Lunge müssen sich zahlreiche Alveolen (Lungenbläschen) bilden und eng mit Kapillaren verflochten werden, damit der Gasaustausch effizient funktioniert. Das Team fand heraus, dass Lungenperizyten zwei wichtige Wachstumsfaktoren produzieren: HGF und BDNF. Wurde HGF nur in Perizyten entfernt, teilten sich die kleinen, „stammzellähnlichen“ Typ-2-Alveolarzellen, die Alveolen auskleiden, weniger und bildeten weniger ausgereifte Oberflächenzellen. Die Lungen zeigten größere, vereinfachte Lufträume und ein geringeres Gesamtvolumen, obwohl die grundlegende Atmung bei jungen Mäusen weitgehend ausreichte. Wurde BDNF in Perizyten eliminiert, wuchsen die Lungenkapillaren schlecht, Endothelzellen teilten sich weniger und die Lufträume wurden ebenfalls vergrößert. Folgende Experimente zeigten, dass BDNF aus Perizyten seinen Rezeptor auf Lungenendothelzellen aktiviert und so die Ausdehnung des Gefäßnetzes antreibt, die für eine normale Alveolenbildung nötig ist.
Andere Regeln für das Gehirnwachstum
Die gleichen Perizyten-Signale waren nicht überall wichtig. Im Gehirn produzierten Perizyten wenig bis kein HGF und BDNF, und das Ausschalten dieser Moleküle in muralen Zellen verursachte keine erkennbaren Veränderungen in der Gefäßdichte, der Barriereintegrität oder dem Verhalten benachbarter Nervenzellen. Stattdessen setzten Gehirnperizyten auf ein anderes Signal, ein Protein namens Nodal. Wenn die Nodal-Produktion spezifisch in diesen Perizyten nach der Geburt blockiert wurde, dehnten sich Hirnkapillaren nicht normal aus, und es trat eine subtile Undichtigkeit von Blutbestandteilen ins Hirngewebe auf. Zellkulturtests mit isolierten Maus-Hirnendothelzellen zeigten, dass Nodal deren Wachstum und Bewegung direkt über einen bekannten Signalweg fördern kann, was seine Rolle als wachstumsförderndes Signal für die Mikrogefäße des Gehirns stützt.
Das Gleichgewicht der Gehirnstützzellen bewahren
Der Verlust von Perizyten-abgeleitetem Nodal hatte eine weitere auffällige Wirkung: Er brachte zentrale Gehirnstützzellen in einen Stresszustand. Astrozyten, die sternförmigen Zellen, die Gefäße umhüllen und zur Aufrechterhaltung der Blut-Hirn-Schranke beitragen, wurden hypertroph und zeigten höhere Werte von Markern, die mit reaktiven Antworten auf Verletzung assoziiert sind. Mikroglia, die residenten Immunzellen des Gehirns, nahmen aktiviertere Formen an und schalteten Gene ein, die mit Entzündungen verbunden sind. Einzelzell-RNA-Sequenzierung bestätigte, dass Mikroglia ohne Nodal zu einem proinflammatorischeren Profil wechselten und Astrozyten eine molekulare Signatur der Reaktivität zeigten. In Zellkulturen aktivierte das Hinzufügen von Nodal an isolierte Astrozyten und Mikroglia denselben intrazellulären Signalweg und dämpfte mehrere Aktivierungsmarker, was darauf hindeutet, dass Perizyten-abhängiges Nodal normalerweise hilft, diese Stützzellen und das Hirnumfeld ruhiger und schützender zu halten.
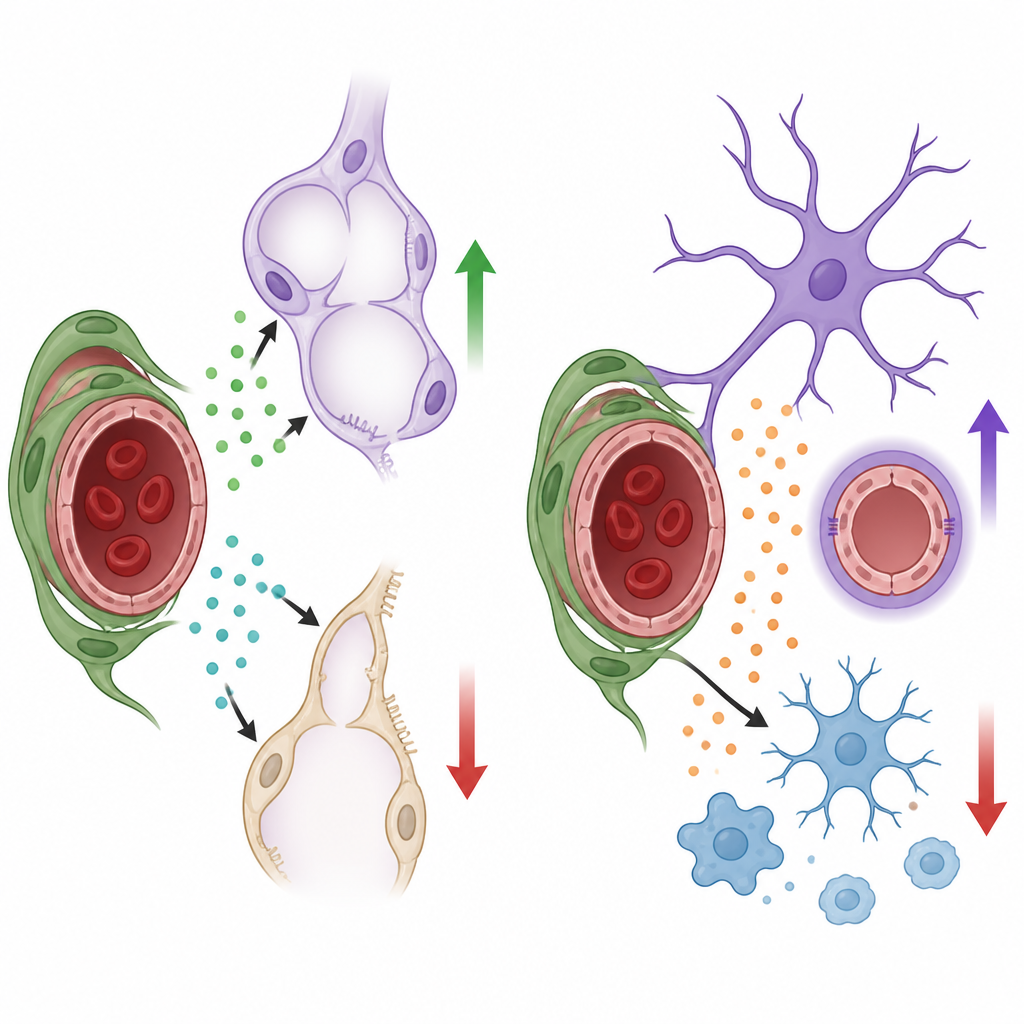
Was das für die Organgesundheit bedeutet
Insgesamt zeigen die Befunde, dass Perizyten organspezifische „Vokabulare“ von Wachstumsfaktoren nutzen, um die Entwicklung zu steuern: in der Lunge fördern sie die Bildung von Alveolen und Gefäßen durch HGF und BDNF, während sie im Gehirn das Gefäßwachstum unterstützen und entzündliche Reaktionen über Nodal einschränken. Perizyten wirken demnach nicht als passive strukturelle Stützen, sondern als lokale Signalknoten, die das Verhalten von Blutgefäßen und die Reaktionen angrenzender Zellen an die Bedürfnisse des jeweiligen Organs anpassen. Das Verständnis dieser verborgenen Gespräche könnte künftige Strategien informieren, um die Lungenreifung bei Frühgeborenen zu unterstützen, die Hirnbarriere bei Erkrankungen zu schützen oder Entzündungen bei neurologischen Störungen feiner zu steuern, ohne den lebenswichtigen Blutfluss zu stören.
Zitation: Rasouli, S.J., Kruse, K., Diéguez-Hurtado, R. et al. Pericytes are organ-specific regulators of tissue morphogenesis. Nat Commun 17, 4229 (2026). https://doi.org/10.1038/s41467-026-71643-1
Schlüsselwörter: Perizyten, Lungenentwicklung, Hirnvasculatur, angiokrine Signalgebung, Neuroinflammation