Clear Sky Science · pl
Pericyty są regulatorem morfogenezy tkanek specyficznym dla narządu
Jak komórki wspierające dyskretnie kształtują rosnące narządy
Każdy narząd w ciele jest opleciony drobnymi naczyniami krwionośnymi dostarczającymi tlen i składniki odżywcze. Jednak te naczynia robią więcej niż tylko przewodzą krew. Badanie ujawnia, jak rzadziej znana grupa komórek podporowych otaczających naczynia włosowate, zwana pericytami, wysyła lokalne sygnały chemiczne, które pomagają płucom i mózgowi budować odpowiednie struktury w miarę dojrzewania po porodzie.
Ukryci pomocnicy wzdłuż naczyń krwionośnych
Naczynia krwionośne wyściełają komórki śródbłonka, które nie tylko tworzą rurki dla przepływu krwi, lecz także wydzielają sygnały kierujące pobliskimi komórkami podczas wzrostu i naprawy narządów. Pericyty siedzą blisko przylegając do małych naczyń i są znane z utrzymywania stabilności ścian naczyń. Do tej pory ich szersza rola w kształtowaniu całych tkanek była niejasna. Korzystając z zaawansowanych narzędzi genetycznych u myszy, badacze selektywnie wyłączyli konkretne molekuły sygnałowe produkowane przez pericyty, a następnie śledzili, jak zmienia się rozwój płuc i mózgu. Ich praca pokazuje, że pericyty nie są uniwersalnymi pomocnikami — zamiast tego działają w sposób specyficzny dla danego narządu i komunikują się z różnymi sąsiednimi komórkami w każdej tkance.
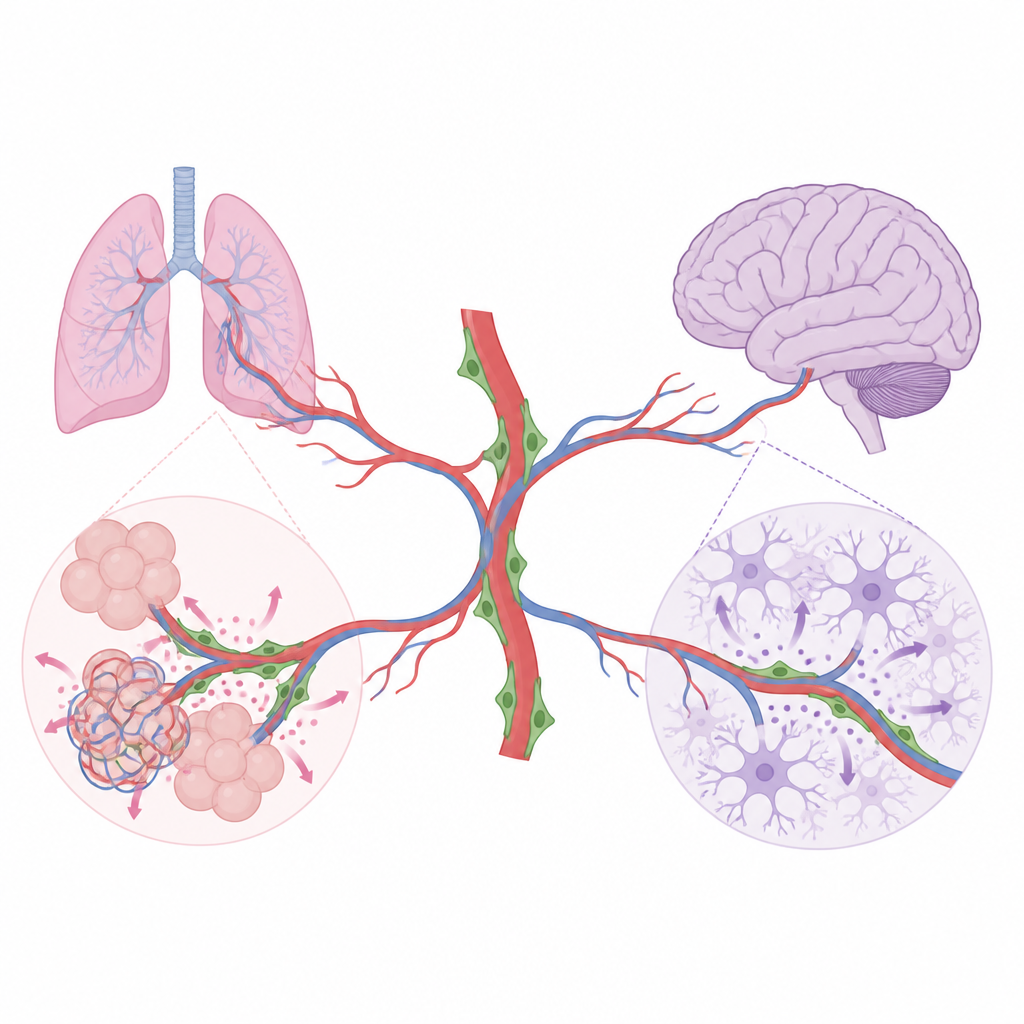
Wiadomości pericytów, które budują zdrowe płuca
W rozwijającym się płucu pęcherzyki muszą tworzyć się w dużej liczbie i być ściśle splecione z kapilarami, aby wymiana gazowa działała wydajnie. Zespół odkrył, że pericyty płucne produkują dwa ważne czynniki wzrostu, HGF i BDNF. Gdy HGF został usunięty jedynie z pericytów, mały „macierzysty-like” typ 2 komórek pęcherzykowych wyściełających pęcherzyki namnażał się słabiej i wytwarzał mniej dojrzałych komórek wyściełających powierzchnię. Płuca wykazywały większe, uproszczone przestrzenie powietrzne i mniejszą objętość ogólną, mimo że podstawowe oddychanie pozostawało u młodych myszy wystarczające. Gdy BDNF został usunięty z pericytów, naczynia włosowate płuc rozwijały się słabo, komórki śródbłonka dzieliły się mniej, a przestrzenie powietrzne znów się powiększyły. Dalsze eksperymenty wykazały, że BDNF pochodzący od pericytów aktywuje swój receptor partnerski na śródbłonku płuc, pomagając napędzać ekspansję sieci naczyniowej niezbędnej do prawidłowego formowania pęcherzyków.
Inne zasady wzrostu mózgu
Te same sygnały pericytów nie miały znaczenia wszędzie. W mózgu pericyty produkowały niewiele lub wcale HGF i BDNF, a wyłączenie tych molekuł w komórkach muralnych nie powodowało wykrywalnych zmian gęstości naczyń, szczelności bariery ani zachowania pobliskich komórek wspierających neurony. Zamiast tego pericyty mózgowe polegały na innym sygnale — białku zwanym Nodal. Gdy produkcja Nodalu została zablokowana specyficznie w tych pericytach po urodzeniu, naczynia włosowate mózgu nie rozwinęły się prawidłowo, a pojawiło się subtelne przeciekanie składników krwi do tkanki mózgowej. Badania laboratoryjne na hodowanych komórkach śródbłonka mózgowego myszy wykazały, że Nodal może bezpośrednio zwiększać ich wzrost i ruch poprzez dobrze znaną ścieżkę sygnałową, wspierając jego rolę jako czynnika pro-wzrostowego dla mikronaczyń mózgu.
Utrzymanie równowagi komórek wspierających mózg
Utrata Nodalu pochodzącego od pericytów wywołała jeszcze jeden uderzający efekt: popchnęła kluczowe komórki wspierające mózg w stan stresu. Astrocyty, komórki w kształcie gwiazdy, które otaczają naczynia i pomagają utrzymać barierę krew–mózg, stały się hipertroficzne i wykazywały wyższy poziom markerów związanych z reaktywną odpowiedzią na uszkodzenie. Mikroglej, rezydujące immunokomórki mózgu, przyjął bardziej aktywowane kształty i włączyl geny związane z zapaleniem. Sekwencjonowanie RNA pojedynczych komórek potwierdziło, że bez Nodalu mikroglej przesunął się w kierunku bardziej prozapalnego profilu, a astrocyty wykazywały molekularny sygnaturę reaktywności. W hodowli, dodanie Nodalu do izolowanych astrocytów i mikrogleju aktywowało ten sam wewnętrzny przełącznik sygnałowy i ograniczało kilka markerów aktywacji, co sugeruje, że Nodal pochodzący od pericytów normalnie pomaga utrzymać te komórki wspierające i środowisko mózgu w spokojniejszym, bardziej ochronnym stanie.
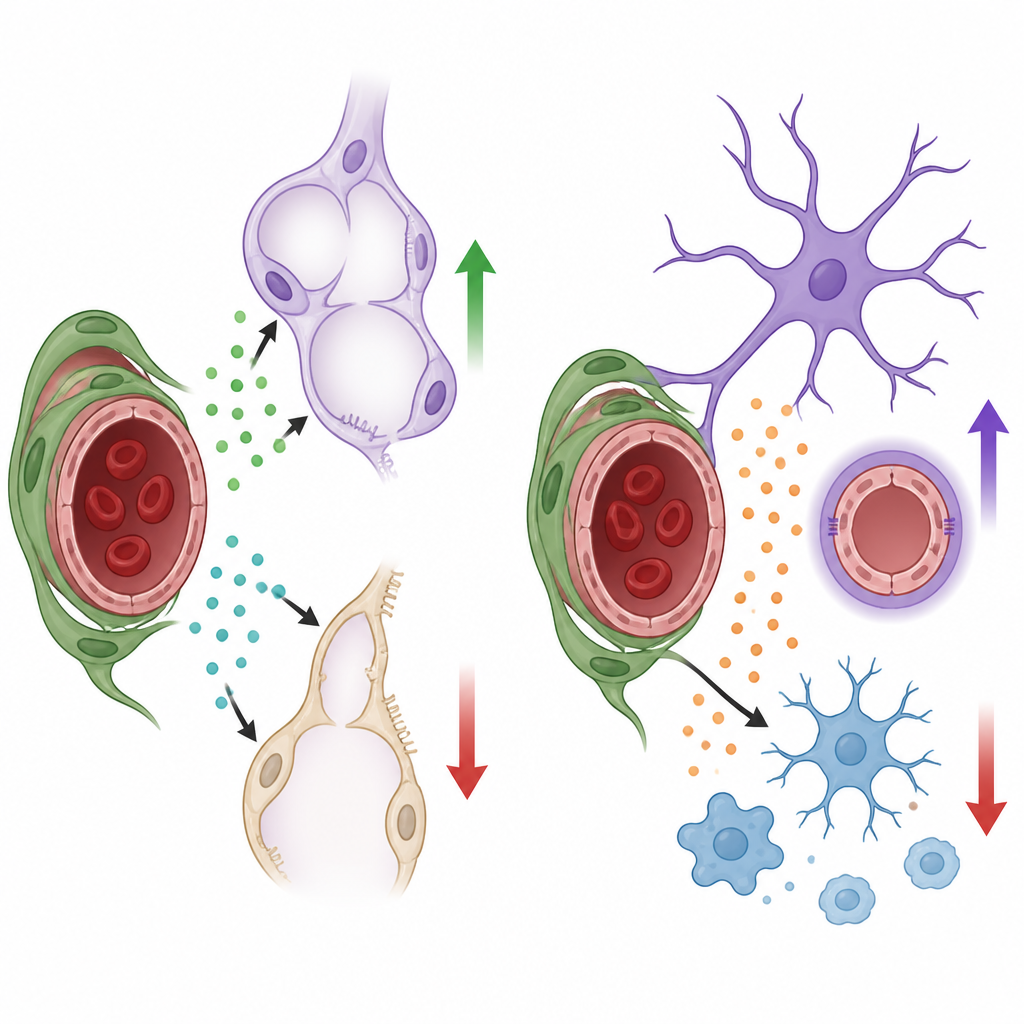
Co to oznacza dla zdrowia narządów
Wspólnie wyniki pokazują, że pericyty używają specyficznych dla narządu „słowników” czynników wzrostu do kierowania rozwojem: w płucach promują formowanie pęcherzyków i naczyń przez HGF i BDNF, podczas gdy w mózgu sprzyjają wzrostowi naczyń i tłumią reakcje zapalne poprzez Nodal. Zamiast działać jako bierne wzmocnienia strukturalne, pericyty funkcjonują jako lokalne węzły sygnałowe, które dopasowują zachowanie naczyń i odpowiedzi pobliskich komórek do potrzeb danego narządu. Zrozumienie tych ukrytych rozmów może naprowadzić przyszłe strategie wspierania dojrzewania płuc u wcześniaków, ochrony bariery mózgowej w chorobach lub precyzyjnego modulowania zapalenia w zaburzeniach neurologicznych bez zakłócania istotnego przepływu krwi.
Cytowanie: Rasouli, S.J., Kruse, K., Diéguez-Hurtado, R. et al. Pericytes are organ-specific regulators of tissue morphogenesis. Nat Commun 17, 4229 (2026). https://doi.org/10.1038/s41467-026-71643-1
Słowa kluczowe: pericyty, rozwój płuc, naczynia mózgowe, sygnalizacja angiokrynowa, neurozapalność