Clear Sky Science · fr
Les péricytes, régulateurs spécifiques à chaque organe de la morphogenèse tissulaire
Comment des cellules de soutien façonnent discrètement les organes en croissance
Chaque organe du corps est parcouru de minuscules vaisseaux sanguins qui apportent oxygène et nutriments. Mais ces vaisseaux font plus que transporter le sang. Cette étude révèle comment un groupe moins connu de cellules de soutien enroulées autour des capillaires, appelées péricytes, envoie des signaux chimiques locaux qui aident les poumons et le cerveau à construire les structures appropriées lors de leur maturation après la naissance.
Les aides cachées le long des vaisseaux sanguins
Les vaisseaux sont tapissés par des cellules endothéliales qui non seulement forment des conduits pour le flux sanguin, mais libèrent aussi des signaux guidant les cellules voisines pendant la croissance et la réparation des organes. Les péricytes sont étroitement attachés aux petits vaisseaux et sont connus pour stabiliser la paroi vasculaire. Jusqu’à présent, leur rôle plus large dans la formation des tissus restait flou. À l’aide d’outils génétiques avancés chez la souris, les chercheurs ont désactivé sélectivement des molécules de signalisation produites par les péricytes, puis suivi comment le développement pulmonaire et cérébral évoluait. Leur travail montre que les péricytes ne sont pas de simples aides génériques ; ils agissent de façon spécifique à chaque organe et dialoguent avec différents voisins cellulaires selon le tissu.
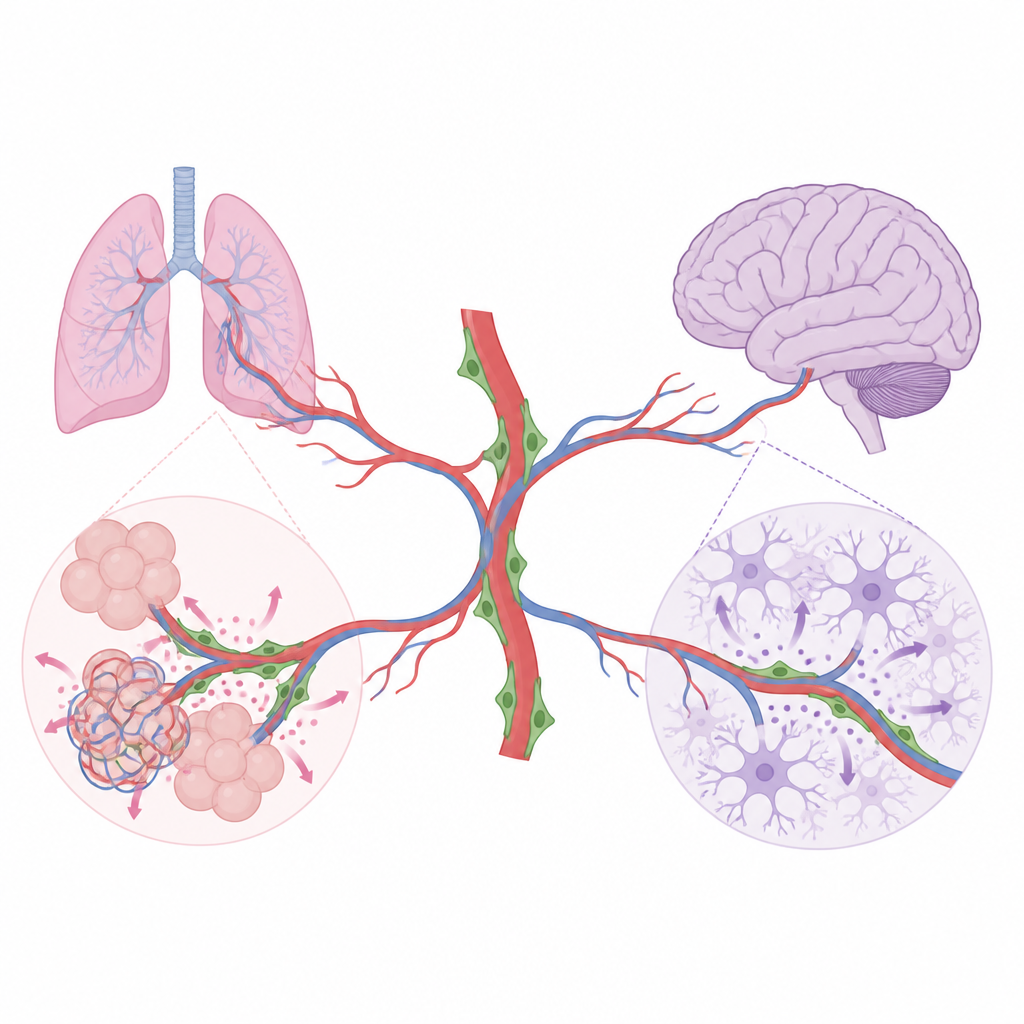
Les messages des péricytes qui construisent des poumons sains
Dans le poumon en développement, les alvéoles doivent se former en grand nombre et s’entrelacer étroitement avec les capillaires pour que les échanges gazeux fonctionnent efficacement. L’équipe a découvert que les péricytes pulmonaires produisent deux facteurs de croissance importants, HGF et BDNF. Lorsque HGF a été supprimé uniquement dans les péricytes, les petites cellules de type 2 alveolaires « souches » qui tapissent les alvéoles se sont moins multipliées et ont produit moins de cellules matures de surface. Les poumons présentaient des espaces aériens plus larges et simplifiés et un volume global réduit, même si la respiration de base restait adéquate chez les jeunes souris. Lorsque le BDNF a été retiré des péricytes, les capillaires pulmonaires se développaient mal, les cellules endothéliales se divisaient moins, et les espaces aériens s’élargissaient de nouveau. Des expériences complémentaires ont montré que le BDNF issu des péricytes active son récepteur partenaire sur les cellules endothéliales pulmonaires, contribuant à l’expansion du réseau vasculaire nécessaire à la formation normale des alvéoles.
Des règles différentes pour la croissance cérébrale
Les mêmes signaux péricytaires n’étaient pas pertinents partout. Dans le cerveau, les péricytes produisaient peu ou pas de HGF et de BDNF, et l’inactivation de ces molécules dans les cellules murales n’entraînait aucun changement détectable de la densité vasculaire, de l’étanchéité de la barrière ou du comportement des cellules gliales voisines. À la place, les péricytes cérébraux s’appuyaient sur un signal différent, une protéine appelée Nodal. Quand la production de Nodal a été bloquée spécifiquement dans ces péricytes après la naissance, les capillaires cérébraux n’ont pas pu s’étendre normalement et une fuite subtile de composants sanguins dans le tissu cérébral est apparue. Des essais en culture avec des cellules endothéliales cérébrales de souris ont montré que Nodal pouvait directement stimuler leur croissance et leur migration via une voie de signalisation bien connue, confirmant son rôle de signal pro-croissance pour les microvaisseaux du cerveau.
Maintenir l’équilibre des cellules de soutien cérébrales
La perte de Nodal dérivé des péricytes avait un autre effet marquant : elle poussait des cellules support clés du cerveau vers un état de stress. Les astrocytes, ces cellules en étoile qui enveloppent les vaisseaux et aident à maintenir la barrière hémato-encéphalique, devenaient hypertrophiés et exprimaient des niveaux plus élevés de marqueurs associés à des réponses réactives aux blessures. Les microglies, les cellules immunitaires résidentes du cerveau, adoptaient des morphologies plus activées et activaient des gènes liés à l’inflammation. Le séquençage ARN unicellulaire a confirmé que, sans Nodal, les microglies basculaient vers un profil plus pro-inflammatoire et que les astrocytes présentaient une signature moléculaire de réactivité. En culture, l’ajout de Nodal à des astrocytes et microglies isolés activait le même interrupteur de signalisation interne et atténuait plusieurs marqueurs d’activation, ce qui suggère que Nodal dérivé des péricytes aide normalement à maintenir ces cellules de soutien et l’environnement cérébral dans un état plus calme et protecteur.
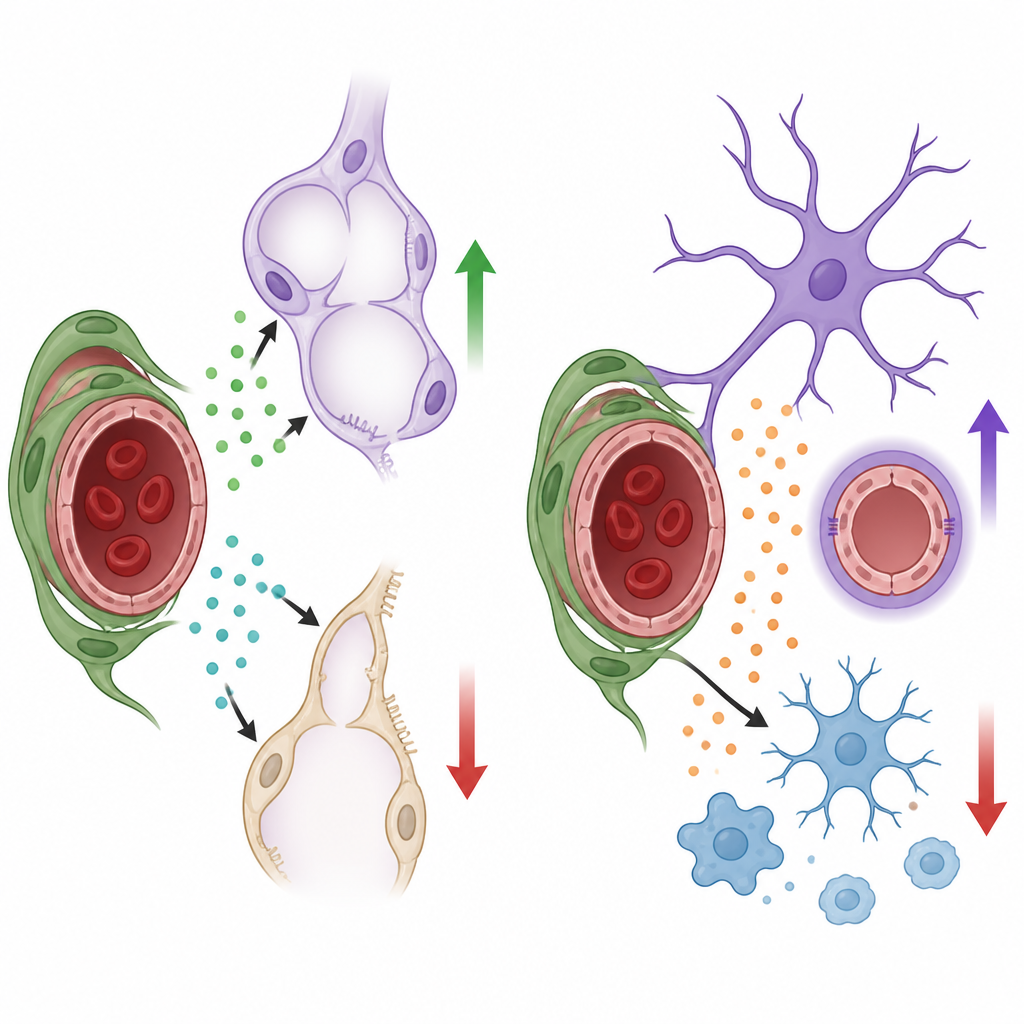
Ce que cela signifie pour la santé des organes
Ensemble, ces résultats montrent que les péricytes utilisent des « vocabulaires » spécifiques à chaque organe de facteurs de croissance pour orienter le développement : dans les poumons, ils favorisent la formation des alvéoles et des vaisseaux via HGF et BDNF, tandis que dans le cerveau ils soutiennent la croissance vasculaire et limitent les réactions inflammatoires via Nodal. Plutôt que d’agir comme de simples supports structurels, les péricytes fonctionnent comme des centres locaux de signalisation qui adaptent le comportement des vaisseaux et les réponses des cellules voisines aux besoins de chaque organe. Comprendre ces conversations cachées pourrait inspirer des stratégies futures pour soutenir la maturation pulmonaire chez les prématurés, protéger la barrière cérébrale dans les maladies ou moduler l’inflammation dans les troubles neurologiques sans perturber le flux sanguin vital.
Citation: Rasouli, S.J., Kruse, K., Diéguez-Hurtado, R. et al. Pericytes are organ-specific regulators of tissue morphogenesis. Nat Commun 17, 4229 (2026). https://doi.org/10.1038/s41467-026-71643-1
Mots-clés: péricytes, développement pulmonaire, vasculature cérébrale, signalisation angiocrine, neuroinflammation