Clear Sky Science · zh
单个核苷酸的增强子突变压倒染色体性别并驱动 XX 雄性发育
微小改变,深远后果
我们通常认为生物学性别写在染色体上:XX 为雌性,XY 为雄性。这项研究为这个叙述带来了一个令人惊讶的转折。研究人员表明,仅在一段调控关键基因的 DNA 中改变一个“字母”就能在小鼠中压倒染色体性别。通过这一微小调整,携带两条 X 染色体的动物会发育出雄性生殖器官,即便它们缺少传统上形成睾丸所需的 Y 染色体。
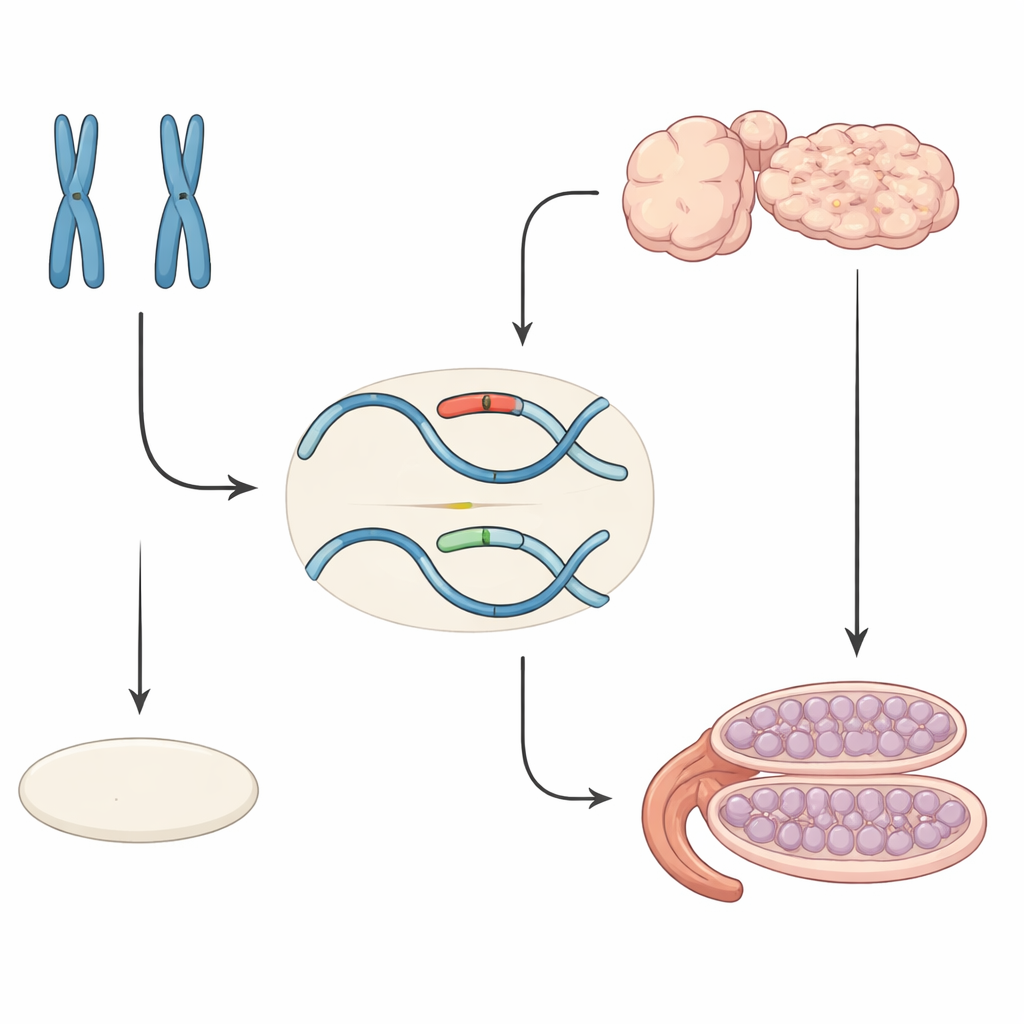
胎内性别通常如何决定
在哺乳动物中,性别由几个阶段决定。起初,胚胎具有未分化的性腺,既可成为睾丸也可成为卵巢。在 XY 胚胎中,位于 Y 染色体上的基因 Sry 激活另一个基因 Sox9,后者驱动细胞朝睾丸方向分化。在 XX 胚胎中缺乏 Sry,一组“促雌性”因子抑制 Sox9 的表达,从而允许卵巢发育。Sox9 的水平像一个分子阈值:如果在适当时间上升到足够高,就会启动睾丸发育;如果保持较低,则进行卵巢发育。
远离基因的隐藏开关
该团队此前鉴定出一段短的 DNA 元件,称为 Enh13,位于距离 Sox9 基因超过五十万个碱基的位置。尽管距离遥远,Enh13 在发育中的睾丸中作为一个强有力的开启开关来激活 Sox9。在小鼠或人类中删除 Enh13 会如此显著降低 Sox9 的活性,以至于 XY 个体可能发育成卵巢而非睾丸。有趣的是,一些有性别发育差异的 XX 人携带包含人类版本 Enh13 的小片段重复,提示额外拷贝可能不当激活 Sox9,促使 XX 性腺走向睾丸命运。
一字母编辑将 XX 性腺翻转为睾丸
在这项研究中,研究人员在小鼠的 Enh13 内进行了极其细微的改动:在 SOX9 蛋白可以结合的一小段序列中,分别引入了三碱基缺失或一碱基插入。携带两份这种被改变增强子拷贝的 XX 小鼠发育为雄性。成体时,它们在外观和内部结构上呈雄性,具有睾丸而非卵巢,尽管这些睾丸体积小且不育,因为缺少 Y 染色体连带的精子生成所需基因。对胚胎的检查显示,XX 性腺最初形成了卵巢和睾丸组织的拼贴——“卵睾混合体”(ovotestis)——随后随着发育进程最终变为睾丸。
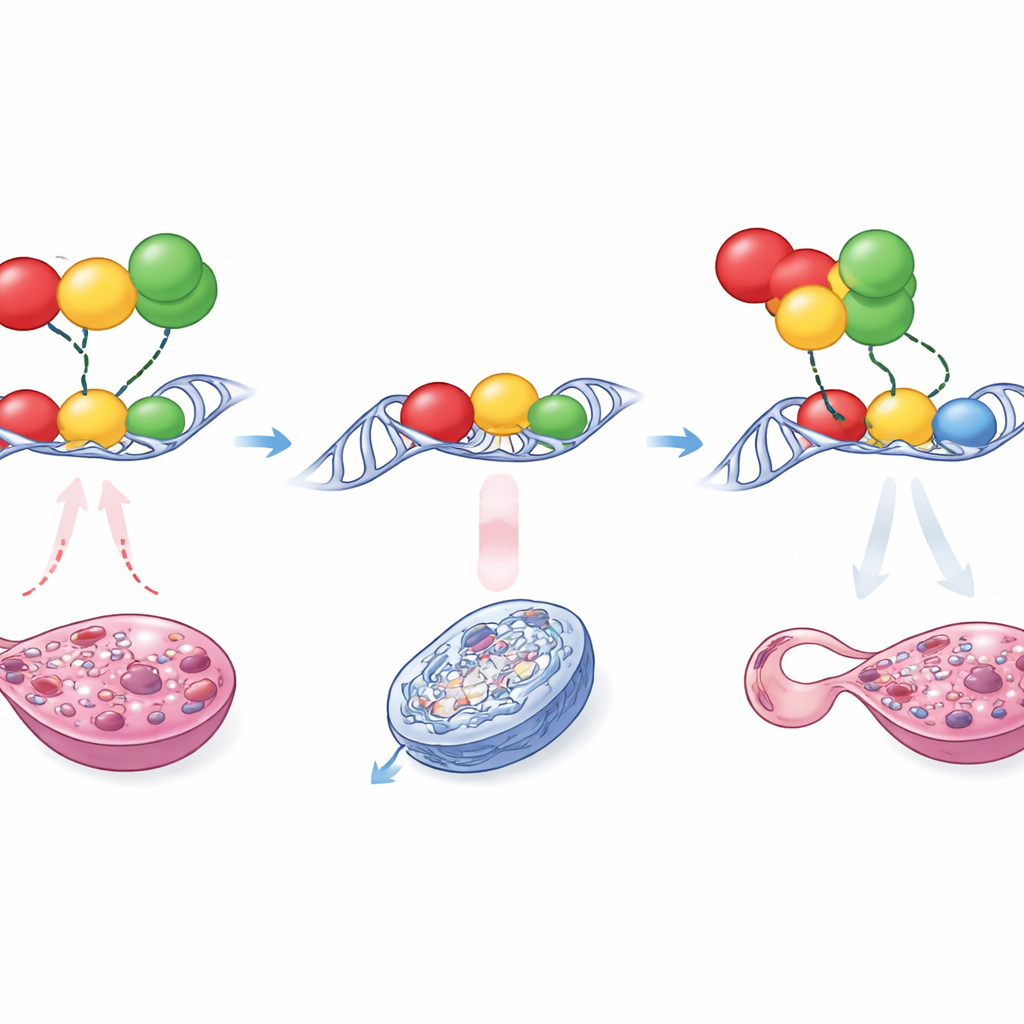
在微小 DNA 片段上的拉锯战
如此细微的改变如何导致如此显著的结果?详尽的分子检测表明,突变并非单纯使 SOX9 结合更强。相反,Enh13 作为一个拥挤的停靠位点,供多种蛋白质结合,这些蛋白质有的推动睾丸命运,有的维持卵巢状态。其中包括在早期性腺中活跃的 RUNX1、NR5A1 和 GATA4。在正常的增强子中,它们结合位点的排列与间距允许“促雌性”影响,特别是 RUNX1 与其他因子协同,抑制 Enh13 在 XX 胚胎中的活性,从而使 Sox9 保持在临界阈值以下。小的插入或缺失微妙地改变了这个结合簇的间距和局部结构。结果,RUNX1 无法再施加相同程度的抑制,而在某个突变体中出现了一个新的位点,使 GATA4 能以更有激活性的构型结合。这些结构上的变化使得增强子在没有 Sry 的情况下也能过度活化,推动 Sox9 表达略微升高,足以让 SOX9 开始自我增强,从而将性腺锁定到睾丸发育路径上。
这对性发育与疾病意味着什么
这项工作表明,Enh13 不仅是睾丸的“开”开关,也是卵巢因子常用来沉默 Sox9 的关键位点。换言之,同一个微小的 DNA 元件可以根据结合的蛋白质不同,既启动也抑制睾丸发育。研究证明,即便在非编码 DNA(不编码蛋白质的区域)中一个字母的改变也能彻底翻转动物的性别命运。这对理解无法解释的人类性别发育差异病例具有重要意义,并说明一个更广泛的原理:增强子内蛋白质停靠位点的三维排列与相对间距,可能与位点本身的存在一样关键。间距的细微变化能重布调控蛋白质的协同方式,将一个平衡的基因开关转变为驱动发育改变的强力因素。
引用: Abberbock, E., Ridnik, M., Stévant, I. et al. A single-nucleotide enhancer mutation overrides chromosomal sex to drive XX male development. Nat Commun 17, 3186 (2026). https://doi.org/10.1038/s41467-026-71328-9
关键词: 性别决定, Sox9, 增强子, 性腺发育, XX 雄性性别逆转