Clear Sky Science · de
Eine einzelner Nukleotid-Verstärker-Mutation überstimmt chromosomales Geschlecht und erzeugt XX-männliche Entwicklung
Eine winzige Änderung mit großen Folgen
Unser biologisches Geschlecht wird üblicherweise in unseren Chromosomen verankert gesehen: XX für Weibchen und XY für Männchen. Diese Studie offenbart eine überraschende Wendung dieser Geschichte. Die Forschenden zeigen, dass die Veränderung nur eines einzigen „Buchstabens“ in einer DNA-Sequenz, die ein Schlüsseltgen reguliert, das chromosomale Geschlecht bei Mäusen außer Kraft setzen kann. Mit dieser winzigen Modifikation entwickeln Tiere mit zwei X-Chromosomen männliche Fortpflanzungsorgane, obwohl ihnen das Y-Chromosom fehlt, das traditionell für die Hodenbildung benötigt wird.
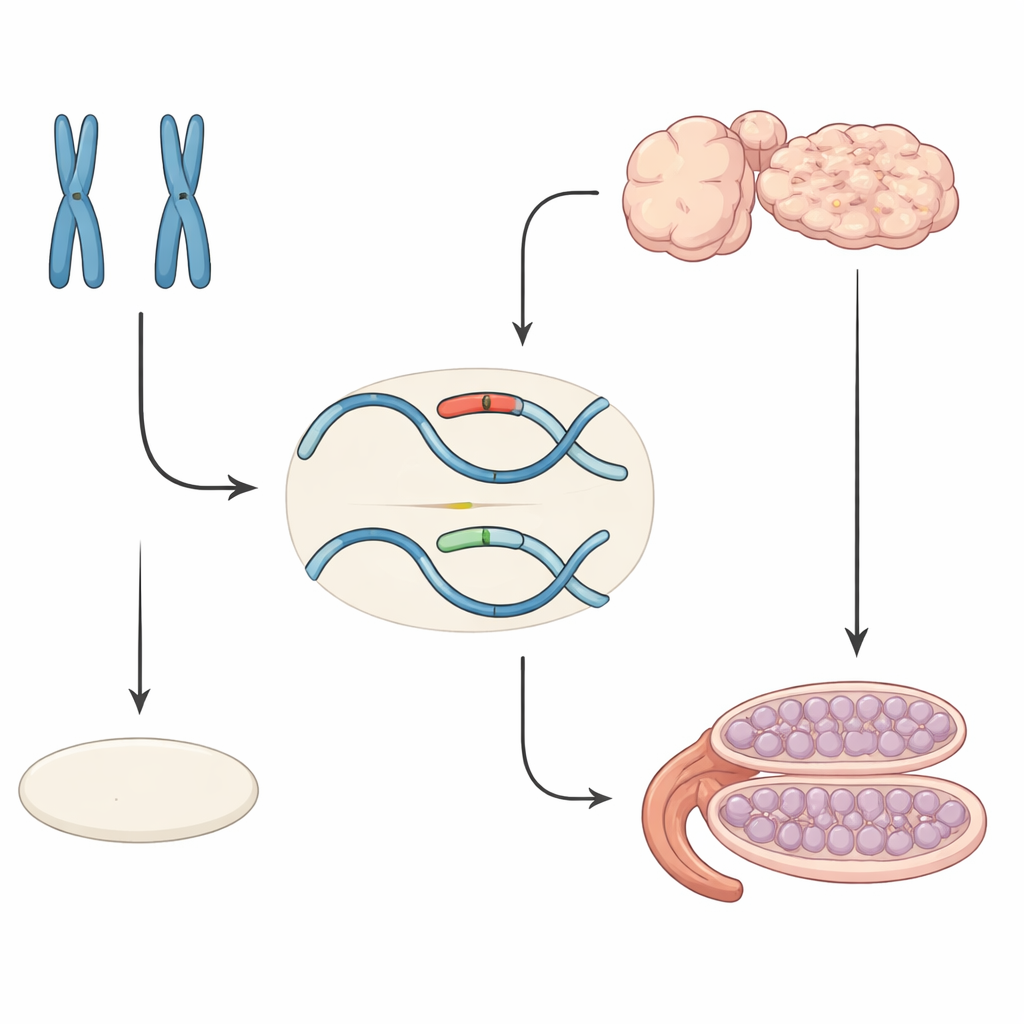
Wie das Geschlecht normalerweise vor der Geburt entschieden wird
Bei Säugetieren erfolgt die Geschlechtsbestimmung in mehreren Schritten. Zunächst besitzen Embryonen undifferenzierte Gonaden, die sich zu Hoden oder Eierstöcken entwickeln können. In XY-Embryonen schaltet ein Gen auf dem Y-Chromosom, genannt Sry, ein anderes Gen, Sox9, an, das die Zellen in Richtung Hodenbildung lenkt. In XX-Embryonen fehlt Sry und eine Gruppe von „pro-weiblichen“ Faktoren hält Sox9 ausgeschaltet, sodass sich Eierstöcke entwickeln. Der Gehalt an Sox9 wirkt wie eine molekulare Schwelle: Steigt er zur richtigen Zeit hoch genug, wird die Hodenentwicklung ausgelöst; bleibt er niedrig, schreitet die Ovarentwicklung voran.
Der verborgene Schalter weit entfernt vom Gen
Das Team hatte zuvor ein kurzes DNA-Element identifiziert, Enh13 genannt, das mehr als eine halbe Million DNA-Basen vom Sox9-Gen entfernt liegt. Trotz der Distanz wirkt Enh13 als starke An-Schaltstelle für Sox9 in sich entwickelnden Hoden. Das Entfernen von Enh13 in Mäusen oder Menschen reduziert die Sox9-Aktivität so stark, dass XY-Individuen statt Hoden Eierstöcke entwickeln können. Auffällig ist, dass einige XX-Personen mit Differences of Sex Development kleine Duplikationen tragen, die die menschliche Version von Enh13 umfassen, was nahelegt, dass zusätzliche Kopien Sox9 unpassend aktivieren und XX-Gonaden in Richtung Hoden-Schicksal schieben könnten.
Ein-Buchstaben-Änderungen, die XX-Gonaden in Hoden verwandeln
In dieser Studie erzeugten die Forschenden extrem subtile Änderungen innerhalb von Enh13 in Mäusen: entweder eine Dreibasendeletion oder eine Ein-Basen-Insertion innerhalb einer kurzen Sequenz, an die das SOX9-Protein binden kann. XX-Mäuse, die zwei Kopien dieser veränderten Enhancer erbten, entwickelten sich als Männchen. Als Erwachsene erschienen sie äußerlich und innerlich männlich, mit Hoden statt Eierstöcken, obwohl die Hoden klein und unfruchtbar waren, weil ihnen y‑chromosomale Gene zur Spermienproduktion fehlten. Bei der Untersuchung von Embryonen fanden die Wissenschaftler, dass XX-Gonaden zunächst ein Mosaik aus ovariellen und hodenähnlichen Geweben – ein „Ovotestis“ – bildeten, bevor sie sich im Verlauf der Entwicklung schließlich zu Hoden ausformten.
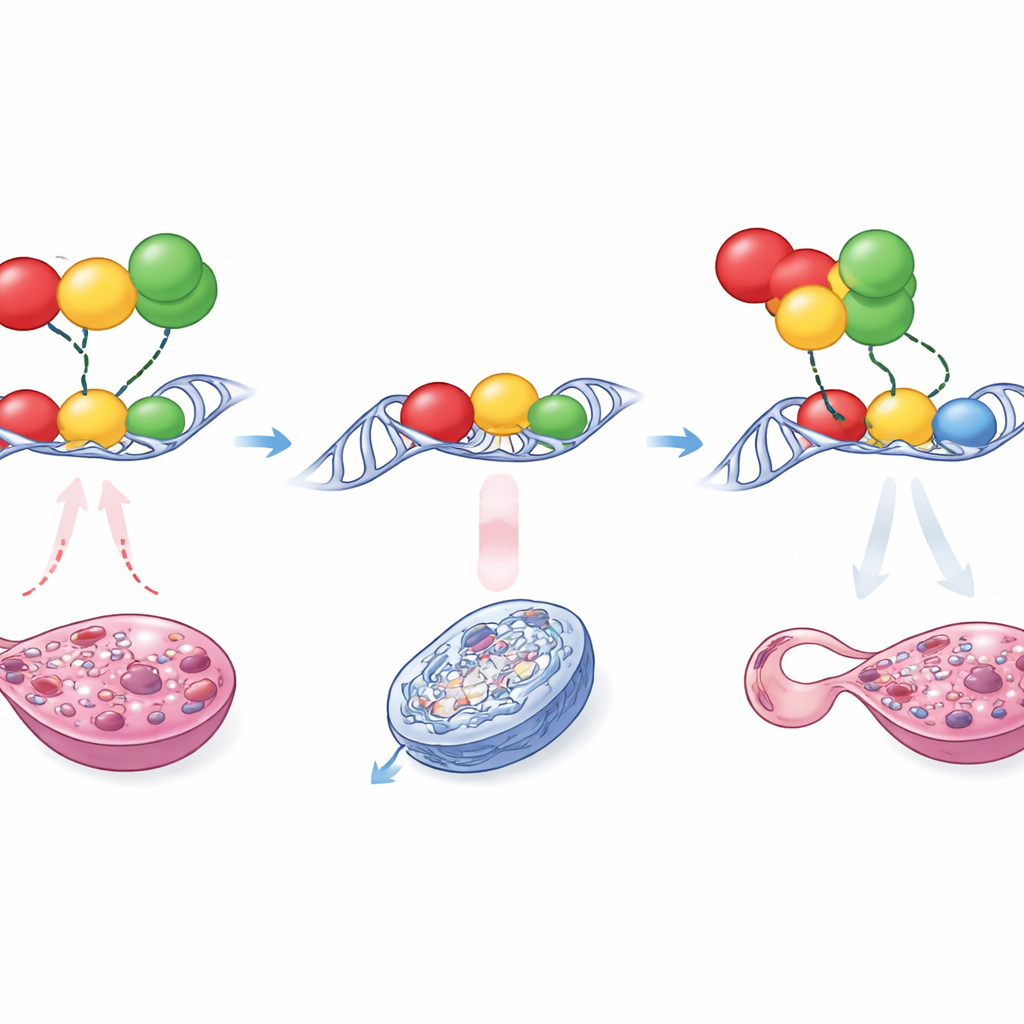
Ein Tauziehen auf einem winzigen DNA-Streifen
Wie kann eine so feine Änderung ein derart dramatisches Ergebnis bewirken? Detaillierte molekulare Tests zeigten, dass die Mutationen nicht einfach dazu führten, dass SOX9 stärker bindet. Vielmehr fungiert Enh13 als dicht besetzte Andockstelle für mehrere Proteine, die entweder in Richtung Hoden-Schicksal drücken oder das System im ovariellen Zustand halten. Dazu gehören RUNX1, NR5A1 und GATA4, Faktoren, die in der frühen Gonade aktiv sind. Im normalen Enhancer erlauben Anordnung und Abstände ihrer Bindungsstellen den „pro-weiblichen“ Einflüssen, insbesondere RUNX1 in Partnerschaft mit anderen, die Aktivität von Enh13 in XX-Embryonen zu dämpfen und Sox9 unter der kritischen Schwelle zu halten. Die kleine Insertion oder Deletion verändert subtil die Abstände und die lokale Struktur dieses Bindungsclusters. Infolgedessen kann RUNX1 nicht mehr dieselbe Repression ausüben, und in einem Mutanten erscheint eine neue Stelle, die GATA4 in einer stärker aktivierenden Konfiguration binden lässt. Diese strukturellen Verschiebungen lassen den Enhancer auch ohne Sry überaktiv werden und heben die Sox9-Expression gerade hoch genug, damit SOX9 seine eigene Produktion zu verstärken beginnt und die Gonade auf den Hodenweg festlegt.
Warum das für Geschlechtsentwicklung und Krankheit wichtig ist
Diese Arbeit zeigt, dass Enh13 nicht nur ein „An“-Schalter für Hoden ist, sondern auch eine Schlüssellokalität, an der ovarielle Faktoren Sox9 normalerweise stummschalten. Anders gesagt kann dasselbe winzige DNA-Element je nach gebundenen Proteinen entweder die Hodenentwicklung starten oder verhindern. Die Studie demonstriert, dass bereits eine Ein-Buchstaben-Änderung in nichtkodierender DNA – Regionen, die keine Proteine kodieren – das sexuelle Schicksal eines Tieres vollständig umkippen kann. Das hat wichtige Folgen für das Verständnis unerklärter Fälle menschlicher Differences of Sex Development und illustriert ein allgemeineres Prinzip: Die dreidimensionale Anordnung von Protein-Andockstellen innerhalb von Enhancern kann ebenso entscheidend sein wie das Vorhandensein der Stellen selbst. Geringfügige Verschiebungen in den Abständen können die Kooperation regulatorischer Proteine neu verdrahten und einen ausgeglichenen genetischen Schalter in einen starken Treiber der Entwicklungsveränderung verwandeln.
Zitation: Abberbock, E., Ridnik, M., Stévant, I. et al. A single-nucleotide enhancer mutation overrides chromosomal sex to drive XX male development. Nat Commun 17, 3186 (2026). https://doi.org/10.1038/s41467-026-71328-9
Schlüsselwörter: Geschlechtsbestimmung, Sox9, Enhancer, gonadale Entwicklung, XX-männliche Geschlechtsumkehr