Clear Sky Science · fr
Une mutation d’un seul nucléotide dans un amplificateur outrepassant le sexe chromosomique pour produire des mâles XX
Un minuscule changement aux grandes conséquences
On pense généralement que notre sexe biologique est inscrit dans nos chromosomes : XX pour les femelles et XY pour les mâles. Cette étude révèle un retournement surprenant de cette histoire. Les chercheurs montrent que modifier d’une seule « lettre » dans un tronçon d’ADN qui régule un gène clé peut outrepasser le sexe chromosomique chez la souris. Avec cette infime modification, des animaux portant deux chromosomes X développent des organes reproducteurs mâles, bien qu’ils n’aient pas le chromosome Y traditionnellement requis pour la formation des testicules.
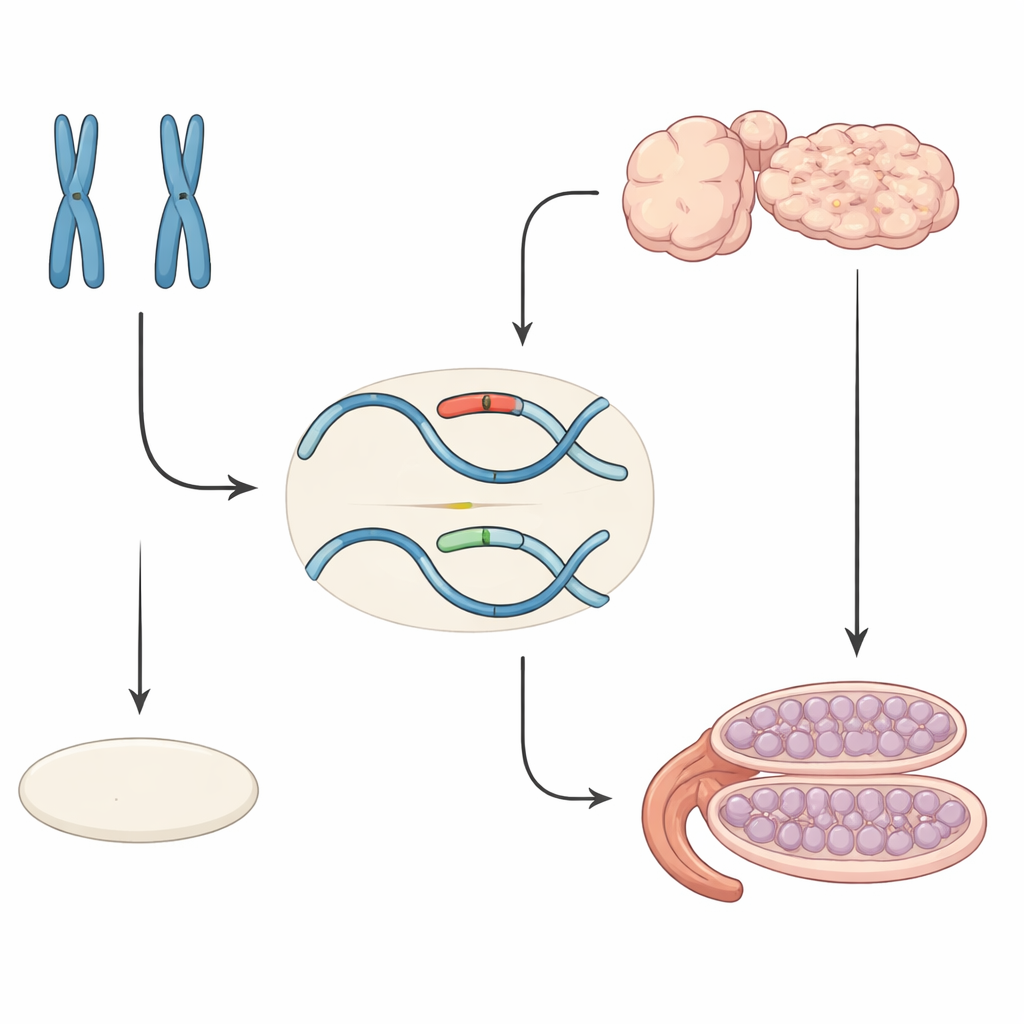
Comment le sexe se décide normalement avant la naissance
Chez les mammifères, le sexe se détermine en plusieurs étapes. Au départ, les embryons possèdent des gonades indifférenciées qui peuvent devenir soit des testicules soit des ovaires. Chez les embryons XY, un gène porté par le chromosome Y appelé Sry active un autre gène, Sox9, qui oriente les cellules vers la formation des testicules. Chez les embryons XX, Sry est absent et un ensemble de facteurs « pro-femelle » maintient Sox9 éteint, permettant le développement des ovaires. Le niveau de Sox9 fonctionne comme un seuil moléculaire : s’il monte suffisamment et au bon moment, le développement testiculaire se met en route ; s’il reste bas, le développement ovarien progresse.
Le commutateur caché loin du gène
L’équipe a auparavant identifié un court élément d’ADN, nommé Enh13, situé à plus d’un demi-million de lettres d’ADN du gène Sox9. Bien que distant, Enh13 fonctionne comme un puissant bouton marche pour Sox9 dans les testicules en développement. La suppression d’Enh13 chez la souris ou chez l’humain réduit l’activité de Sox9 de manière si prononcée que des individus XY peuvent développer des ovaires au lieu de testicules. De manière intrigante, certaines personnes XX présentant des variations du développement sexuel portent de petites duplications incluant la version humaine d’Enh13, ce qui suggère que des copies supplémentaires pourraient activer inappropriément Sox9 et orienter les gonades XX vers un destin testiculaire.
Des modifications d’une seule lettre qui transforment les gonades XX en testicules
Dans cette étude, les chercheurs ont introduit des modifications extrêmement subtiles à l’intérieur d’Enh13 chez la souris : soit une suppression de trois lettres, soit une insertion d’une lettre au sein d’une courte séquence où la protéine SOX9 peut se lier. Les souris XX ayant hérité de deux copies de ces amplificateurs altérés se sont développées comme des mâles. À l’âge adulte, elles présentaient un aspect externe et interne masculin, avec des testicules au lieu d’ovaires, bien que ces testicules fussent petits et infertiles car ils ne contenaient pas les gènes liés au Y nécessaires à la production de spermatozoïdes. Lorsqu’ils ont examiné les embryons, les scientifiques ont constaté que les gonades XX formaient d’abord une mosaïque de tissus ovarien et testiculaire — un « ovotestis » — avant de se résoudre finalement en testicules à mesure que le développement progressait.
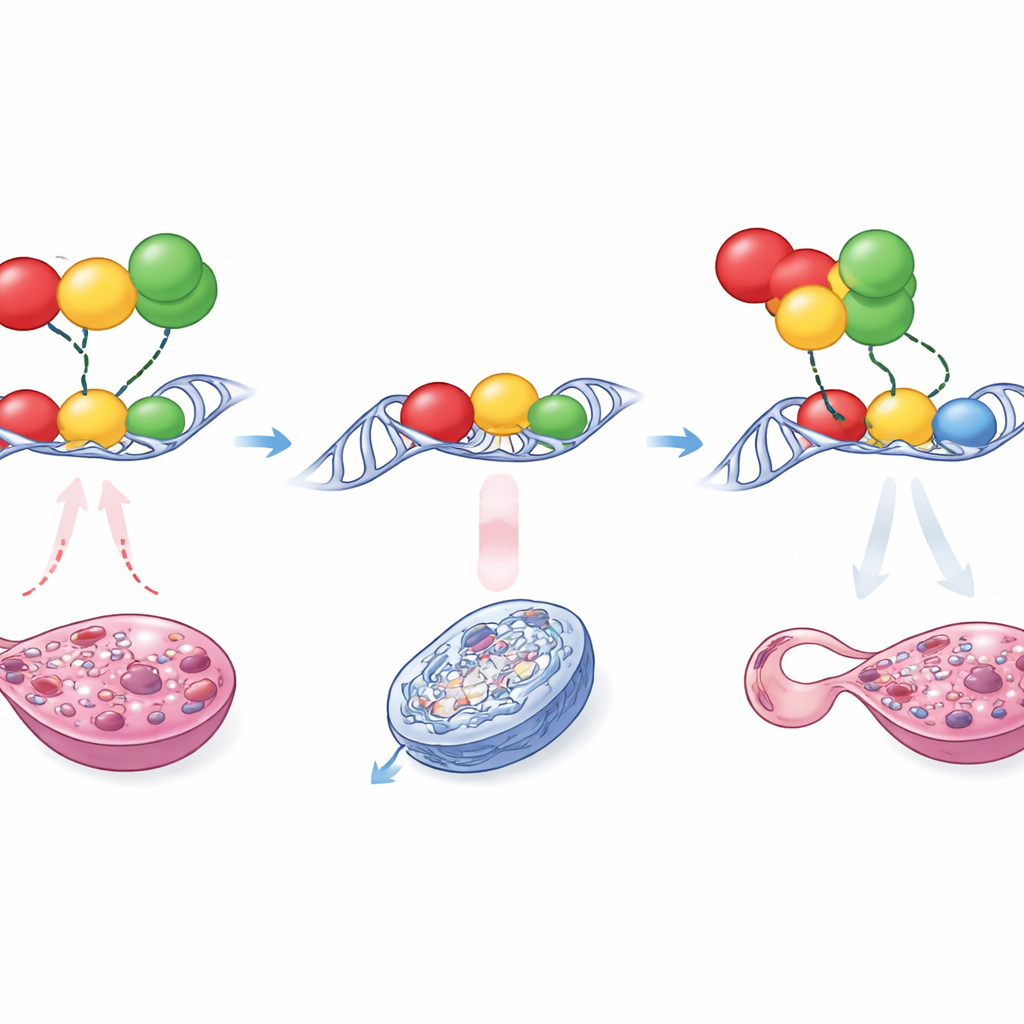
Une lutte d’influence sur une minuscule bande d’ADN
Comment un changement aussi délicat peut-il provoquer un résultat aussi spectaculaire ? Des tests moléculaires détaillés ont montré que les mutations ne rendaient pas simplement SOX9 plus affiné pour se lier. Au lieu de cela, Enh13 sert de site d’amarrage très encombré pour plusieurs protéines qui poussent soit vers un destin testiculaire soit vers un état ovarien. Parmi elles figurent RUNX1, NR5A1 et GATA4, des facteurs actifs dans la gonade précoce. Dans l’amplificateur normal, l’agencement et l’espacement de leurs sites de liaison permettent aux influences « pro-femelle », en particulier RUNX1 en partenariat avec d’autres, d’atténuer l’activité d’Enh13 chez les embryons XX et de maintenir Sox9 en dessous du seuil critique. La petite insertion ou suppression modifie subtilement l’espacement et la structure locale de ce groupe de sites de liaison. En conséquence, RUNX1 ne peut plus imposer le même niveau de répression, et dans une des mutations un nouveau site apparaît qui permet à GATA4 de se lier dans une configuration plus activatrice. Ces changements structuraux font que l’amplificateur devient hyperactif même en l’absence de Sry, élevant l’expression de Sox9 juste assez pour que SOX9 commence à amplifier sa propre production, verrouillant la gonade sur la voie testiculaire.
Pourquoi c’est important pour le développement sexuel et la maladie
Ce travail montre qu’Enh13 n’est pas seulement un bouton « marche » pour les testicules mais aussi un site clé où les facteurs ovariens silencent normalement Sox9. Autrement dit, le même minuscule élément d’ADN peut soit déclencher soit arrêter le développement testiculaire selon les protéines qui y sont liées. L’étude démontre qu’un changement d’une seule « lettre » dans l’ADN non codant — des régions qui n’encodent pas de protéines — peut complètement inverser le destin sexuel d’un animal. Cela a des implications importantes pour la compréhension de cas inexpliqués de différences du développement sexuel humain et illustre un principe plus large : l’agencement tridimensionnel des sites d’ancrage protéiques au sein des amplificateurs peut être tout aussi crucial que la présence des sites eux-mêmes. De légers décalages d’espacement peuvent reconfigurer la coopération des protéines régulatrices, transformant un interrupteur génétique équilibré en un puissant moteur de changement développemental.
Citation: Abberbock, E., Ridnik, M., Stévant, I. et al. A single-nucleotide enhancer mutation overrides chromosomal sex to drive XX male development. Nat Commun 17, 3186 (2026). https://doi.org/10.1038/s41467-026-71328-9
Mots-clés: détermination du sexe, Sox9, amplificateurs, développement gonadique, inversion du sexe mâle XX