Clear Sky Science · pt
Uma mutação de um único nucleotídeo em potenciador anula o sexo cromossômico para promover desenvolvimento masculino em XX
Uma mudança minúscula com grandes consequências
Geralmente pensamos que nosso sexo biológico está escrito nos cromossomos: XX para fêmeas e XY para machos. Este estudo revela uma reviravolta surpreendente nessa história. Os pesquisadores mostram que alterar apenas uma “letra” em um trecho de DNA que regula um gene-chave pode anular o sexo cromossômico em camundongos. Com esse ajuste minúsculo, animais com dois cromossomos X desenvolvem órgãos reprodutivos masculinos, mesmo sem o cromossomo Y tradicionalmente necessário para a formação de testículos.
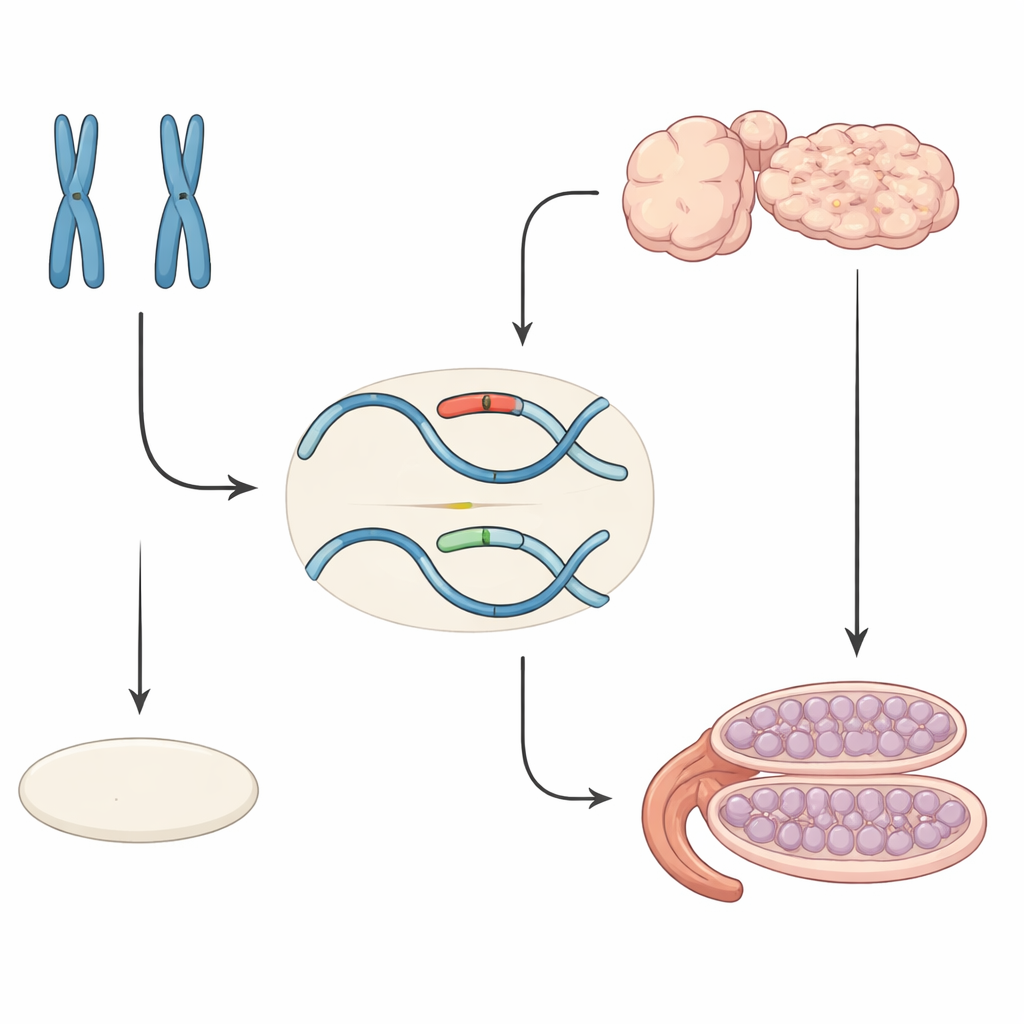
Como o sexo normalmente é decidido antes do nascimento
Em mamíferos, a determinação sexual ocorre em várias etapas. A princípio, os embriões possuem gônadas indiferenciadas que podem se tornar testes ou ovários. Em embriões XY, um gene no cromossomo Y chamado Sry ativa outro gene, Sox9, que direciona as células para formar testículos. Em embriões XX, Sry está ausente e um conjunto de fatores “pró-femininos” mantém Sox9 desligado, permitindo o desenvolvimento dos ovários. O nível de Sox9 funciona como um limiar molecular: se subir o bastante no momento certo, o desenvolvimento do testículo é desencadeado; se permanecer baixo, segue-se o desenvolvimento ovariano.
O interruptor escondido longe do gene
O grupo identificou anteriormente um curto elemento de DNA, chamado Enh13, situado a mais de meio milhão de bases do gene Sox9. Embora distante, Enh13 funciona como um poderoso interruptor de ativação para Sox9 em testículos em desenvolvimento. Deletar Enh13 em camundongos ou humanos reduz a atividade de Sox9 de forma tão acentuada que indivíduos XY podem desenvolver ovários em vez de testículos. Intrigantemente, algumas pessoas XX com diferenças no desenvolvimento sexual carregam pequenas duplicações que incluem a versão humana de Enh13, o que sugere que cópias extras podem ativar Sox9 de modo inadequado e empurrar as gônadas XX rumo ao destino testicular.
Edições de uma letra que transformam gônadas XX em testículos
Neste estudo, os pesquisadores introduziram mudanças extremamente sutis dentro de Enh13 em camundongos: ou uma deleção de três letras ou uma inserção de uma letra dentro de uma curta sequência onde a proteína SOX9 pode se ligar. Camundongos XX que herdaram duas cópias desses potenciadores alterados se desenvolveram como machos. Em adultos, apresentavam aparência externa e interna masculina, com testículos em vez de ovários, embora os testículos fossem pequenos e inférteis porque careciam de genes ligados ao Y necessários para a produção de espermatozoides. Ao examinar embriões, os cientistas descobriram que as gônadas XX inicialmente formavam um mosaico de tecido ovariano e testicular — um “ovotesto” — antes de finalmente se resolverem em testículos conforme o desenvolvimento avançava.
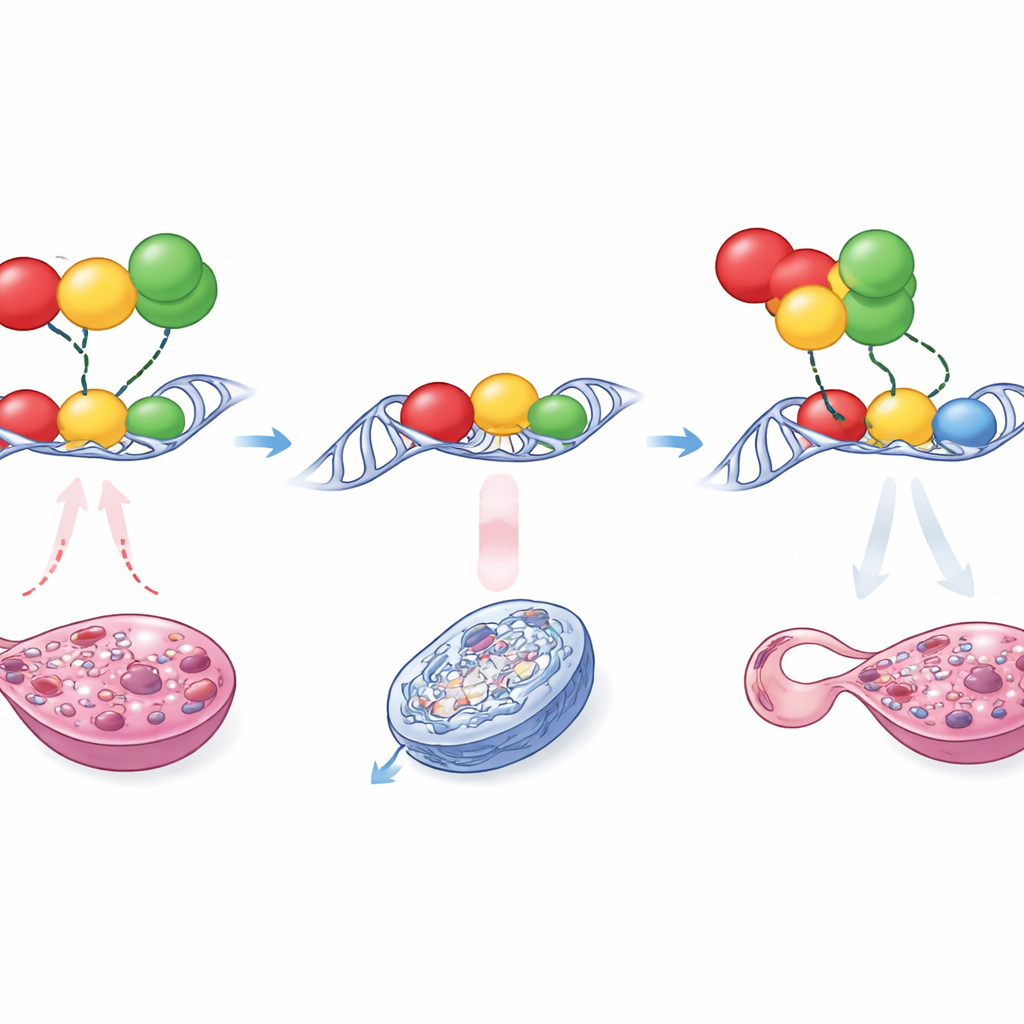
Uma disputa em uma faixa minúscula de DNA
Como uma alteração tão delicada pode causar um resultado tão dramático? Testes moleculares detalhados mostraram que as mutações não simplesmente fizeram a SOX9 ligar-se com mais afinidade. Em vez disso, Enh13 funciona como um local de acoplamento lotado para várias proteínas que ou empurram para um destino testicular ou mantêm o sistema em um estado ovariano. Entre elas estão RUNX1, NR5A1 e GATA4, fatores ativos na gônada precoce. No potenciador normal, o arranjo e o espaçamento dos seus sítios de ligação permitem que as influências “pró-femininas”, especialmente RUNX1 em parceria com outros, atenuem a atividade de Enh13 em embriões XX e mantenham Sox9 abaixo do limiar crítico. A pequena inserção ou deleção altera sutilmente o espaçamento e a estrutura local desse aglomerado de sítios de ligação. Como resultado, RUNX1 não consegue mais impor o mesmo nível de repressão, e em um dos mutantes surge um novo sítio que permite à GATA4 ligar-se numa configuração mais ativadora. Essas mudanças estruturais permitem que o potenciador fique hiperativo mesmo sem Sry, impulsionando a expressão de Sox9 o suficiente para que SOX9 comece a aumentar sua própria produção, travando a gônada no caminho testicular.
Por que isso importa para desenvolvimento sexual e doenças
Este trabalho mostra que Enh13 não é apenas um interruptor “liga” para testículos, mas também um sítio-chave onde fatores ovarianos silenciam normalmente Sox9. Em outras palavras, o mesmo pequeno elemento de DNA pode iniciar ou impedir o desenvolvimento testicular dependendo de quais proteínas estão ligadas. O estudo demonstra que mesmo uma mudança de uma letra em DNA não codificante — regiões que não codificam proteínas — pode inverter completamente o destino sexual de um animal. Isso tem implicações importantes para entender casos inexplicados de diferenças do desenvolvimento sexual humano e ilustra um princípio mais amplo: o arranjo tridimensional dos sítios de acoplamento de proteínas dentro de potenciadores pode ser tão crucial quanto a presença dos próprios sítios. Pequenas variações no espaçamento podem reconfigurar como proteínas reguladoras cooperam, transformando um interruptor genético em equilíbrio num potente motor de mudança desenvolvimental.
Citação: Abberbock, E., Ridnik, M., Stévant, I. et al. A single-nucleotide enhancer mutation overrides chromosomal sex to drive XX male development. Nat Commun 17, 3186 (2026). https://doi.org/10.1038/s41467-026-71328-9
Palavras-chave: determinação sexual, Sox9, potenciadores, desenvolvimento gonadal, inversão sexual masculino em XX