Clear Sky Science · es
Una mutación de un solo nucleótido en un potenciador anula el sexo cromosómico para provocar el desarrollo masculino en XX
Un pequeño cambio con grandes consecuencias
Normalmente se considera que nuestro sexo biológico está escrito en los cromosomas: XX para las hembras y XY para los machos. Este estudio revela un giro sorprendente de esa historia. Los investigadores muestran que alterar una sola “letra” en un tramo de ADN que regula un gen clave puede anular el sexo cromosómico en ratones. Con este mínimo ajuste, animales que portan dos cromosomas X desarrollan órganos reproductores masculinos, aunque carecen del cromosoma Y que tradicionalmente se considera necesario para la formación de los testículos.
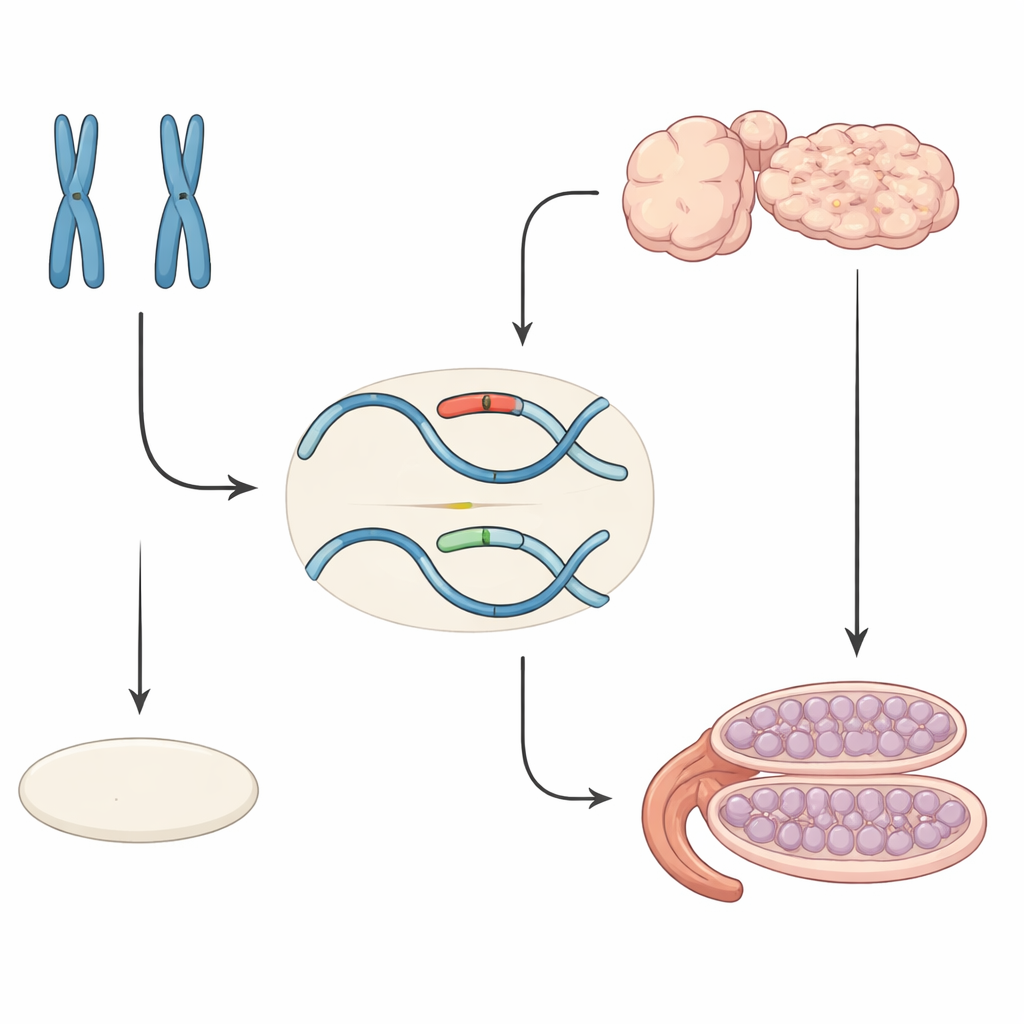
Cómo se decide normalmente el sexo antes del nacimiento
En los mamíferos, el sexo se determina en varias etapas. Al principio, los embriones poseen gónadas indiferenciadas que pueden convertirse en testículos u ovarios. En los embriones XY, un gen en el cromosoma Y llamado Sry activa otro gen, Sox9, que impulsa a las células hacia la formación de testículos. En los embriones XX, Sry está ausente y un conjunto de factores “pro‑femeninos” mantiene a Sox9 apagado, permitiendo que se desarrollen ovarios. El nivel de Sox9 actúa como un umbral molecular: si sube lo suficiente en el momento adecuado, se pone en marcha el desarrollo testicular; si se mantiene bajo, progresa el desarrollo ovárico.
El interruptor oculto lejos del gen
El equipo identificó previamente un elemento corto de ADN, llamado Enh13, situado a más de medio millón de bases del gen Sox9. Aunque lejano, Enh13 funciona como un potente interruptor de encendido para Sox9 en los testículos en desarrollo. Eliminar Enh13 en ratones o humanos reduce la actividad de Sox9 de manera tan drástica que individuos XY pueden desarrollar ovarios en lugar de testículos. Intrigantemente, algunas personas XX con diferencias en el desarrollo sexual presentan pequeñas duplicaciones que incluyen la versión humana de Enh13, lo que sugiere que copias adicionales podrían activar inapropiadamente a Sox9 y empujar las gónadas XX hacia un destino testicular.
Ediciones de una sola letra que convierten gónadas XX en testículos
En este estudio, los investigadores introdujeron cambios extremadamente sutiles dentro de Enh13 en ratones: bien una deleción de tres letras o una inserción de una letra dentro de una secuencia corta donde puede unirse la proteína SOX9. Los ratones XX que heredaron dos copias de estos potenciadores alterados se desarrollaron como machos. En adultos, tenían apariencia externa e interna masculina, con testículos en lugar de ovarios, aunque los testículos eran pequeños e infértiles porque les faltaban genes ligados al Y necesarios para la producción de esperma. Al examinar los embriones, los científicos encontraron que las gónadas XX formaban inicialmente un mosaico de tejido ovárico y testicular—un “ovotestículo”—antes de resolverse finalmente en testículos a medida que avanzaba el desarrollo.
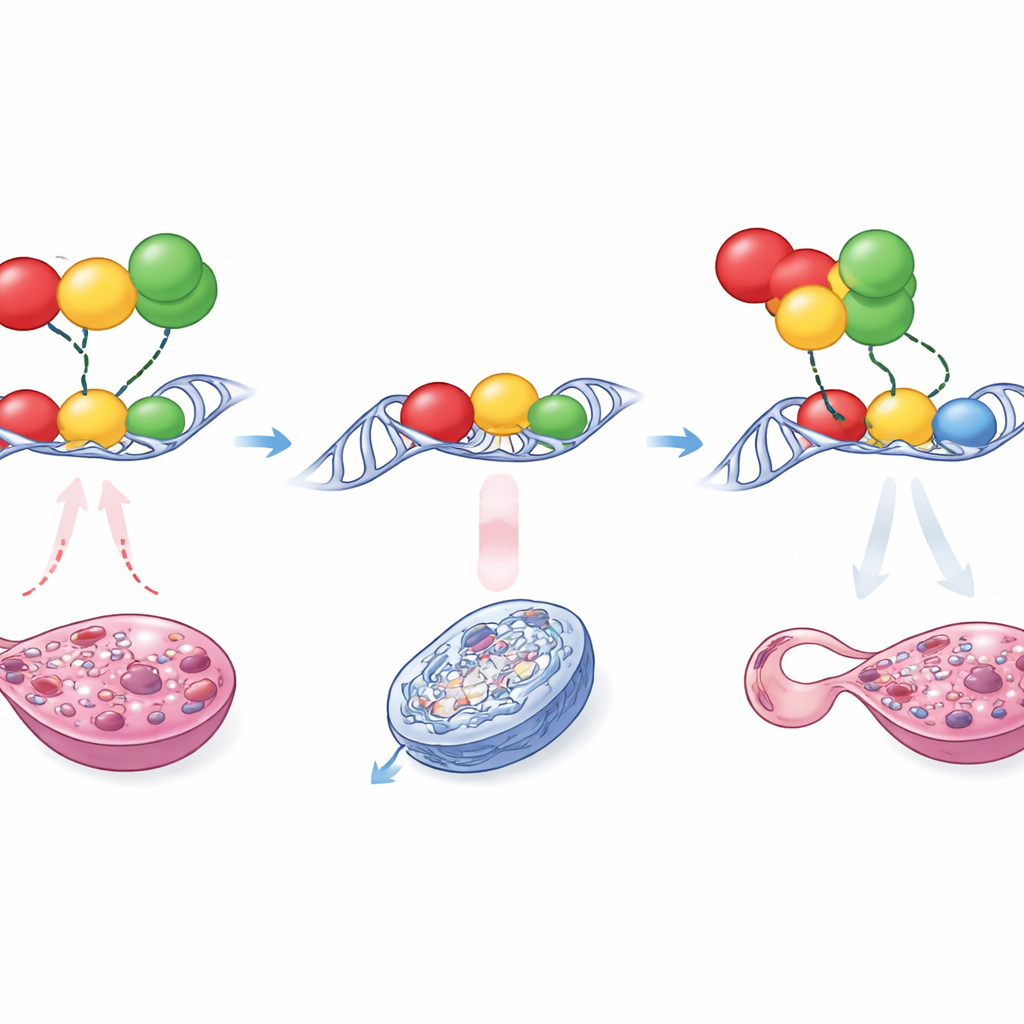
Un tira y afloja en una franja minúscula de ADN
¿Cómo puede un cambio tan delicado causar un resultado tan drástico? Pruebas moleculares detalladas mostraron que las mutaciones no hicieron simplemente que SOX9 se uniera con más fuerza. En su lugar, Enh13 actúa como un sitio de acoplamiento concurrido para varias proteínas que, bien empujan hacia un destino testicular o bien mantienen el sistema en un estado ovárico. Entre ellas se encuentran RUNX1, NR5A1 y GATA4, factores activos en la gónada temprana. En el potenciador normal, la disposición y el espaciamiento de sus sitios de unión permiten influencias “pro‑femeninas”, especialmente RUNX1 en asociación con otros, que atemperan la actividad de Enh13 en embriones XX y mantienen a Sox9 por debajo del umbral crítico. La pequeña inserción o deleción cambia sutilmente el espaciamiento y la estructura local de este cúmulo de sitios de unión. Como resultado, RUNX1 ya no puede imponer el mismo nivel de represión, y en uno de los mutantes aparece un nuevo sitio que permite a GATA4 unirse en una configuración más activadora. Estos cambios estructurales permiten que el potenciador se vuelva hiperactivo incluso sin Sry, impulsando la expresión de Sox9 lo bastante como para que SOX9 comience a potenciar su propia producción, bloqueando a la gónada en la vía testicular.
Por qué esto importa para el desarrollo sexual y la enfermedad
Este trabajo muestra que Enh13 no es solo un interruptor de encendido para los testículos, sino también un sitio clave donde los factores ováricos normalmente silencian a Sox9. En otras palabras, ese mismo elemento diminuto de ADN puede iniciar o detener el desarrollo testicular según qué proteínas estén unidas. El estudio demuestra que incluso un cambio de una sola letra en el ADN no codificante—regiones que no codifican proteínas—puede invertir por completo el destino sexual de un animal. Esto tiene implicaciones importantes para comprender casos no explicados de diferencias en el desarrollo sexual humano e ilustra un principio más amplio: la disposición tridimensional de los sitios de acoplamiento de proteínas dentro de los potenciadores puede ser tan crucial como la presencia de los propios sitios. Pequeños desplazamientos en el espaciamiento pueden reconectar cómo cooperan las proteínas reguladoras, convirtiendo un interruptor genético equilibrado en un potente motor de cambio del desarrollo.
Cita: Abberbock, E., Ridnik, M., Stévant, I. et al. A single-nucleotide enhancer mutation overrides chromosomal sex to drive XX male development. Nat Commun 17, 3186 (2026). https://doi.org/10.1038/s41467-026-71328-9
Palabras clave: determinación sexual, Sox9, potenciadores, desarrollo gonadal, inversión sexual masculino XX