Clear Sky Science · zh
可逆的 DNA 凝聚驱动天然转化
细菌如何“借用”DNA
当细菌从周围环境中拾取游离 DNA 时,抗生素耐药性可能会扩散,这种技巧被称为天然转化。这项研究揭示了单一蛋白如何帮助将进入的 DNA 拉过某些细菌的坚硬外层屏障,采用一种微妙的推拉方式,而非强力马达式推动。理解这种微观拔河机制,有助于未来制定减缓耐药基因传播的策略。
通向新基因的分子门
许多细菌能够天然地从环境中摄取 DNA 片段,并将有用基因并入自身染色体。为此,DNA 必须穿过细胞壁并到达细胞内部。在具有厚细胞壁的革兰氏阳性细菌中,膜蛋白 ComEA 位于细胞壁与内膜之间的空间,那里它会抓住进入的 DNA。到目前为止,科学家知道 ComEA 对该过程至关重要,但尚不清楚它如何实际促使 DNA 向内移动。
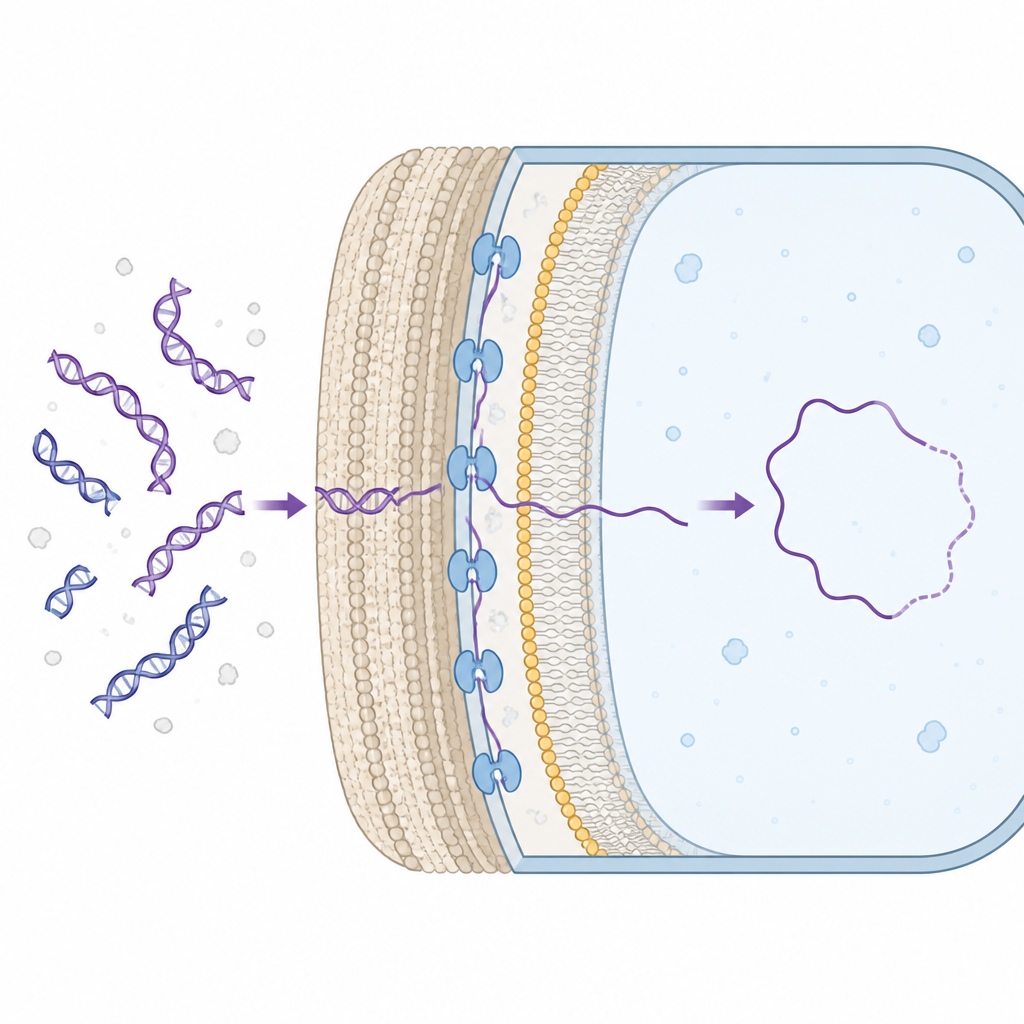
一次测量一条分子的温和 DNA 拖拽
研究人员使用单分子光镊技术,将单条 DNA 用激光光束夹在两个微小微珠之间。通过添加纯化的 ComEA 并牵拉 DNA,他们能够观察到 ComEA 分子何时将链上相距较远的部分连接起来,形成小环。当更多这样的桥接形成时,整体 DNA 长度有效减少,显示出 ComEA 在凝聚 DNA。打破这些桥接会导致 DNA 长度的突变跳跃,使团队能够计算出被环绕的 DNA 量以及产生的机械力。他们发现 ComEA 能产生非常小的、亚皮牛顿级的牵引力,足以偏向 DNA 向内移动,但远弱于典型分子马达产生的力。
两态开关:先凝聚,后松驰
电子显微镜为科学家提供了将 DNA 与 ComEA 混合时的快照。在适度的蛋白水平下,他们观察到 DNA 形成环状和部分压缩,符合桥接相互作用的特征。随着 ComEA 浓度进一步增加,这些环消失,尽管 DNA 表面被更多蛋白覆盖。额外测量显示,在高覆盖度下,ComEA 仍沿 DNA 形成组装体,但以非桥接方式存在,稳定伸展的 DNA 而非将其环化。在这种拥挤状态下,DNA 变得去凝聚,不再受到牵拉力,这揭示了由局部 ComEA 含量控制的内在开关。
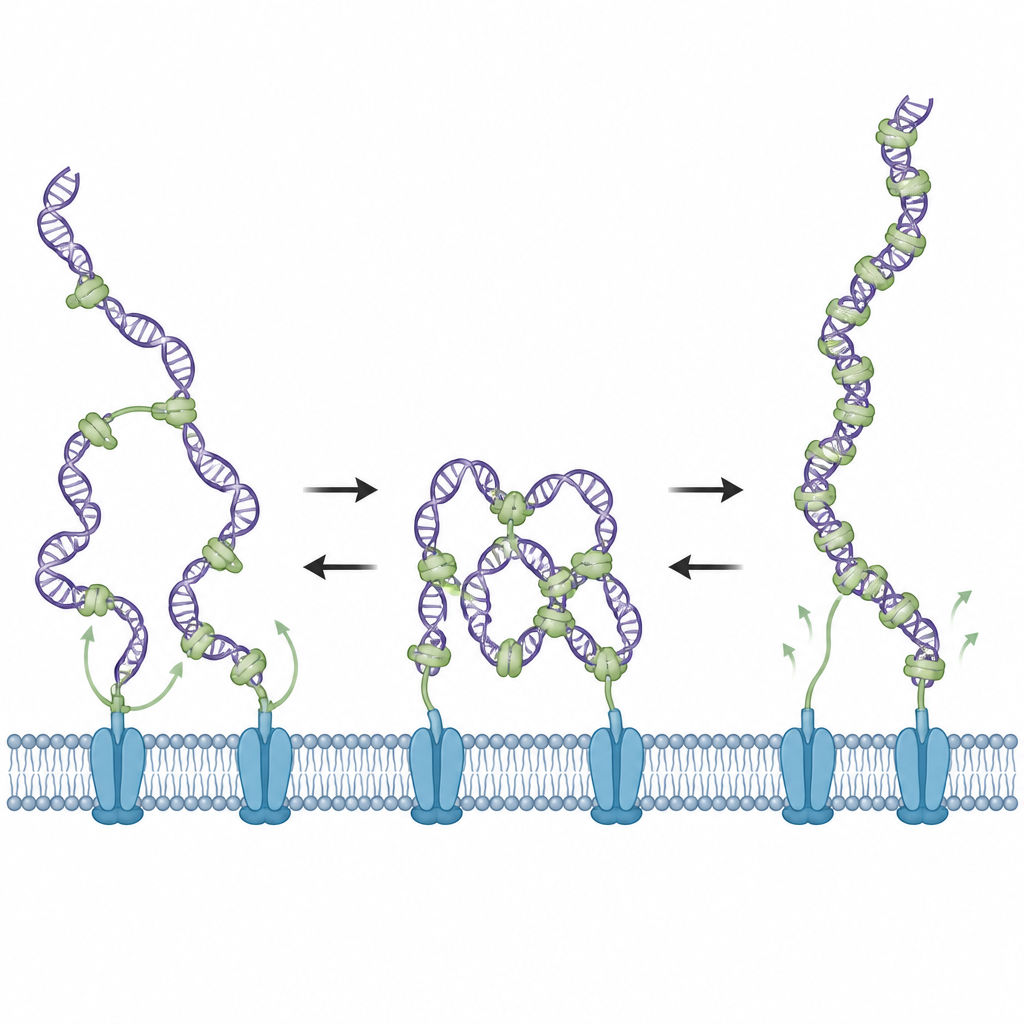
改造蛋白的柔性连接段
ComEA 含有一段柔性连接区,将其抓握 DNA 的部分与允许其与其他 ComEA 分子聚集的部分连接起来。团队缩短或延长了这一连接段,以测试其对行为的影响。短连接突变体更倾向于处于放松的非桥接状态,无法产生凝聚力,而长连接突变体即使在高蛋白水平下也倾向于持续桥接并产生牵引力。两类突变体都能结合 DNA,但在转化真正的枯草芽孢杆菌(Bacillus subtilis)细胞时效果都很差,这表明成功的 DNA 摄取需要 ComEA 起初能够凝聚 DNA,随后又能释放让其放松。
这与抗生素耐药为何相关
综合起来,这些结果支持了革兰氏阳性细菌拉入外源 DNA 的两步模型。在摄取早期,稀疏结合的 ComEA 蛋白桥接 DNA 的分离片段,温和地凝聚并将链拉过厚实的细胞壁朝膜方向移动。随着更多 ComEA 在同一 DNA 上积累,它切换到非桥接模式,停止牵拉并允许 DNA 去凝聚,从而更易于其他转运蛋白将单链 DNA 输送入细胞内部。这种可逆的凝聚提供了足够的定向偏置以推动 DNA,而不会阻碍随后的转运步骤,有助于解释细菌如何高效获取可能包含抗生素耐药性的全新基因。
引用: Santiago, J.I., Ahmed, I., Hahn, J. et al. Reversible DNA condensation drives natural transformation. Nat Commun 17, 4242 (2026). https://doi.org/10.1038/s41467-026-70559-0
关键词: 天然转化, DNA 摄取, ComEA, 抗生素耐药, 细菌细胞壁