Clear Sky Science · sv
Reversibel DNA-kondensation driver naturlig transformation
Hur bakterier lånar DNA
Antibiotikaresistens kan spridas när bakterier plockar upp fritt DNA från omgivningen, ett trick känt som naturlig transformation. Denna studie visar hur ett enda protein hjälper till att föra inkommande DNA över den tuffa yttre barriären hos vissa bakterier, genom en subtil drag-och-släpp-rutin snarare än en kraftfull motor. Att förstå detta mikroskopiska dragkamp kan ge insikter för framtida strategier att bromsa spridningen av resistensgener.
En molekylär dörr för nya gener
Många bakterier kan naturligt ta upp DNA-fragment från sin omgivning och lägga användbara gener till sitt eget genom. För att detta ska ske måste DNA passera cellväggen och nå cellens inre. Hos Grampositiva bakterier, som har en tjock cellvägg, sitter ett membranbundet protein kallat ComEA i utrymmet mellan väggen och innermembranet, där det fångar upp inkommande DNA. Hittills visste forskarna att ComEA är nödvändigt för denna process, men de förstod inte hur det faktiskt bidrog till att föra DNA inåt.
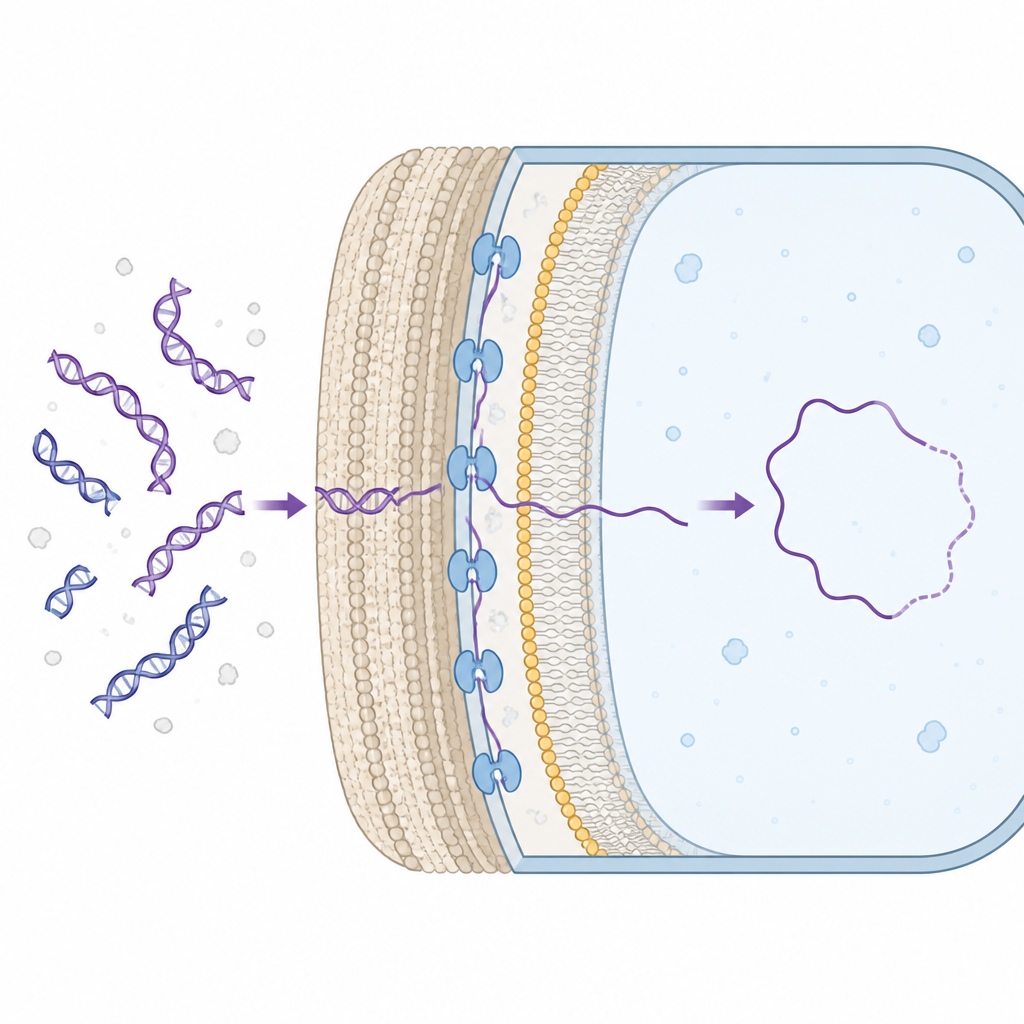
Varsamma DNA-drag mätta en molekyl åt gången
Forskarna använde enkelmolekylära optiska pincetter, en teknik som håller en enskild DNA-bit mellan två mikroskopiska kulor med laserljus. Genom att tillsätta renat ComEA och dra i DNA:t kunde de se när ComEA-molekyler kopplade samman avlägsna delar av strängen och bildade små slingor. När fler av dessa bryggor bildades krympte den totala DNA-längden effektivt, vilket visade att ComEA kondenserade det. Brott i dessa bryggor orsakade plötsliga hopp i DNA-längd, vilket gjorde det möjligt för teamet att beräkna hur mycket DNA som slingats och hur mycket mekanisk kraft som genererades. De fann att ComEA kan dra med mycket små, sub-pikonewton-krafter — tillräckligt för att ge en riktad rörelse inåt men långt svagare än krafterna från klassiska molekylära motorer.
En tvålägesbrytare: kondensera, sedan slappna av
Elektronmikroskopi gav forskarna ögonblicksbilder av hur DNA såg ut när det blandades med ComEA. Vid måttliga proteinnivåer såg de slingor och partiell kompaktering av DNA, i linje med bryggande interaktioner. När koncentrationen av ComEA ökade ytterligare försvann dessa slingor, även om DNA-ytan blev mer tätt täckt med protein. Ytterligare mätningar visade att vid hög beläggning bildar ComEA fortfarande sammankomster längs DNA men nu på ett icke-bryggande sätt som stabiliserar utsträckt DNA i stället för att loopa det. I detta trånga tillstånd blir DNA:t dekoncentrerat och upplever inte längre dragkrafter, vilket avslöjar en inbyggd växel kontrollerad av hur mycket ComEA som finns lokalt.
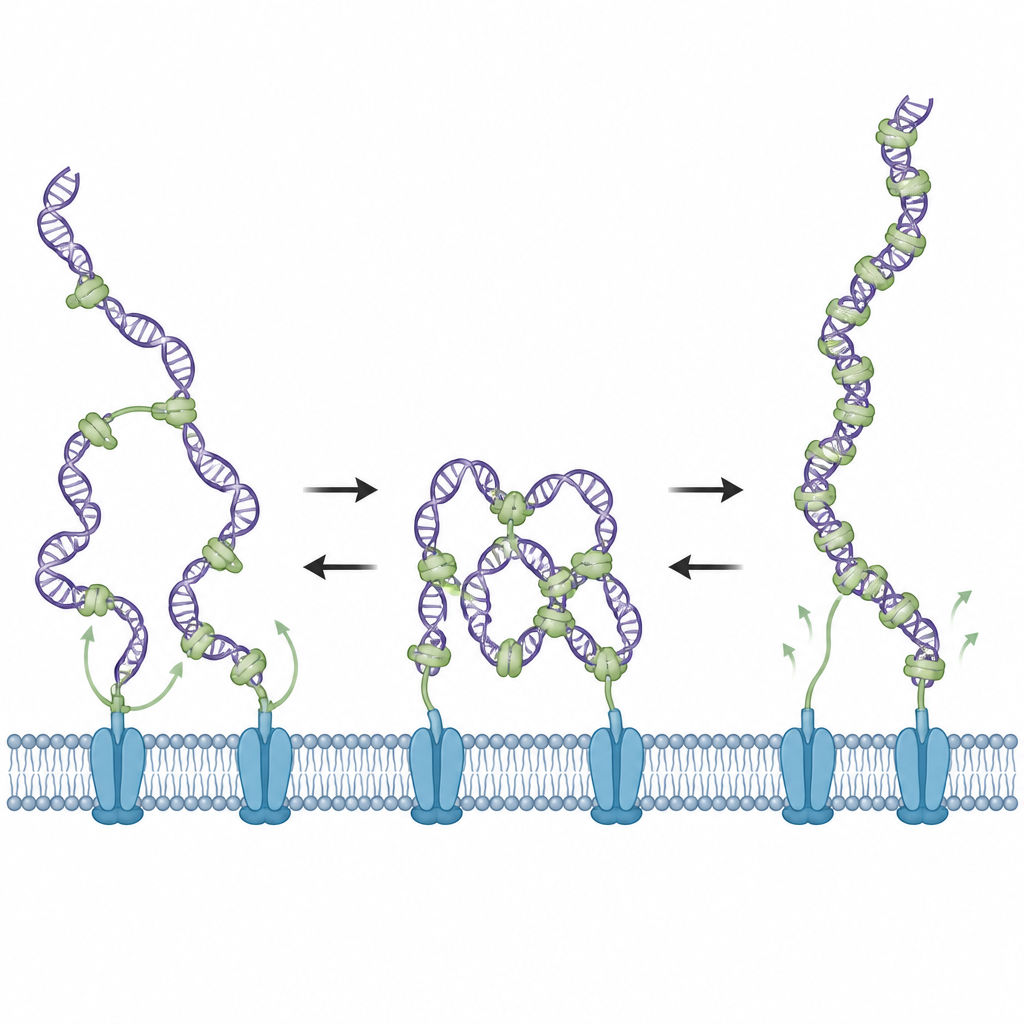
Ingenjörskap av proteinets flexibla länk
ComEA innehåller en flexibel länk som kopplar dess DNA-gripande del till den del som möjliggör klustring med andra ComEA-molekyler. Teamet förkortade eller förlängde denna länk för att testa hur det påverkade beteendet. Kortlänksmutanter gynnade det avslappnade, icke-bryggande tillståndet och lyckades inte generera kondensationskrafter, medan långlänksmutanter gynnade bestående bryggning och kraftgenerering även vid höga proteinnivåer. Båda typerna av mutanter bundet DNA, men de var var och en dåliga på att transformera verkliga Bacillus subtilis-celler, vilket visar att framgångsrikt DNA-upptag kräver att ComEA både kan kondensera DNA initialt och senare låta det slappna av.
Varför detta spelar roll för antibiotikaresistens
Tillsammans stöder resultaten en tvåstegsmodell för hur Grampositiva bakterier drar in främmande DNA. Tidigt i upptaget bryggar glest bundna ComEA-proteiner separata DNA-sträckor, kondenserar varsamt och drar tråden genom den tjocka cellväggen mot membranet. När mer ComEA ackumuleras på samma DNA växlar det till ett icke-bryggande läge som stoppar dragandet och tillåter DNA att dekoncenteras, vilket gör det lättare för andra transportproteiner att mata in en enkelsträngat DNA i cellens inre. Denna reversibla kondensation ger precis tillräcklig riktningsbias för att förflytta DNA utan att störa efterföljande transportsteg, och hjälper till att förklara hur bakterier effektivt förvärvar nya gener som kan innefatta antibiotikaresistens.
Citering: Santiago, J.I., Ahmed, I., Hahn, J. et al. Reversible DNA condensation drives natural transformation. Nat Commun 17, 4242 (2026). https://doi.org/10.1038/s41467-026-70559-0
Nyckelord: naturlig transformation, DNA-upptag, ComEA, antibiotikaresistens, bakterievägg