Clear Sky Science · de
Reversible DNA-Kondensation treibt natürliche Transformation an
Wie Bakterien DNA ausleihen
Antibiotikaresistenz kann sich ausbreiten, wenn Bakterien lose DNA aus ihrer Umgebung aufnehmen – ein Vorgang, der als natürliche Transformation bekannt ist. Diese Studie zeigt, wie ein einzelnes Protein dabei hilft, eingehende DNA über die robuste Außenbarriere bestimmter Bakterien zu ziehen, indem es eher eine subtile Schub‑Zug‑Routine als einen starken Motor einsetzt. Das Verständnis dieses mikroskopischen Tauziehens könnte helfen, künftige Strategien zur Verlangsamung der Ausbreitung von Resistenzgenen zu entwickeln.
Ein molekularer Durchgang für neue Gene
Viele Bakterien können natürlich DNA‑Fragmente aus ihrer Umwelt aufnehmen und nützliche Gene in ihr eigenes Chromosom einbauen. Dazu muss die DNA die Zellwand überwinden und ins Zellinnere gelangen. Bei Gram‑positiven Bakterien, die eine dicke Zellwand besitzen, sitzt ein Membranprotein namens ComEA im Raum zwischen Wand und innerer Membran und fängt dort eintreffende DNA ein. Bislang war bekannt, dass ComEA für diesen Prozess essenziell ist, aber es war unklar, wie es die DNA tatsächlich nach innen bewegt.
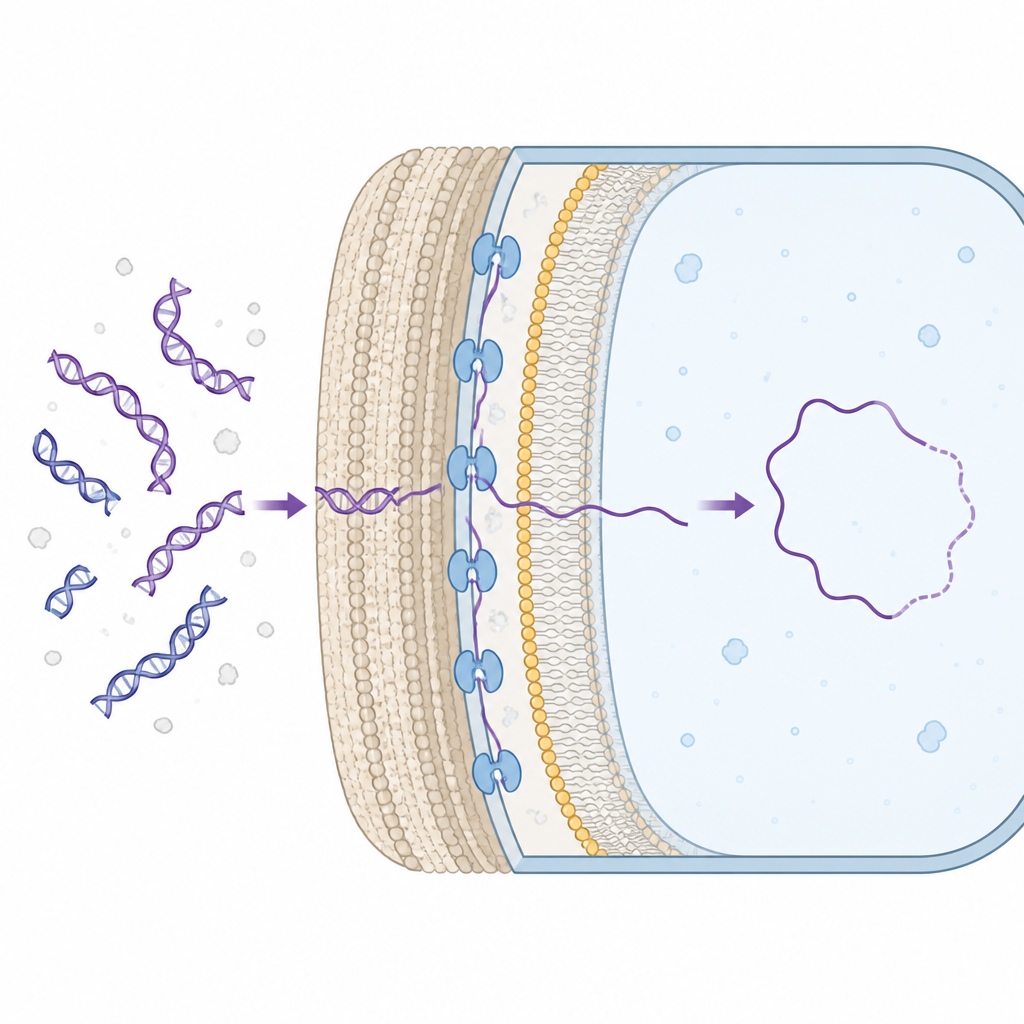
Sanfte DNA‑Züge, einzelmolekülweise gemessen
Die Forschenden nutzten Einzelmolekül‑Optische Pinzetten, eine Methode, bei der ein einzelnes DNA‑Stück zwischen zwei winzigen Kügelchen mithilfe von Laserlicht gehalten wird. Durch Zugabe von gereinigtem ComEA und gleichzeitiges Ziehen an der DNA konnten sie beobachten, wann ComEA Moleküle entfernte Bereiche des Strangs miteinander verband und so kleine Schleifen bildete. Mit zunehmender Brückenbildung verkürzte sich die effektive Länge der DNA, was zeigte, dass ComEA sie kondensierte. Das Aufbrechen dieser Brücken verursachte sprunghafte Längenänderungen, mit denen das Team berechnete, wie viel DNA verschlungen worden war und welche mechanischen Kräfte entstanden. Sie stellten fest, dass ComEA mit sehr kleinen, sub‑piconewtonschen Kräften zieht — genug, um die Bewegung der DNA nach innen zu beeinflussen, aber deutlich schwächer als die Kräfte klassischer molekularer Motoren.
Ein Zwei‑Modi‑Schalter: Kondensieren, dann Entspannen
Elektronenmikroskopische Aufnahmen lieferten Schnappschüsse der DNA, gemischt mit ComEA. Bei moderaten Proteinmengen sahen die Forschenden Schleifen und teilweise Kompaktierung der DNA, konsistent mit überbrückenden Wechselwirkungen. Mit steigender ComEA‑Konzentration verschwanden diese Schleifen, obwohl die DNA‑Oberfläche dichter mit Protein bedeckt war. Weitere Messungen zeigten, dass ComEA bei hoher Belegung weiterhin Assemblies entlang der DNA bildet, nun aber in einer nicht‑überbrückenden Weise, die gestreckte DNA stabilisiert statt sie zu schleifen. In diesem überfüllten Zustand wird die DNA dekompakter und erfährt keine ziehenden Kräfte mehr — ein eingebauter Schalter, der von der lokalen ComEA‑Dichte gesteuert wird.
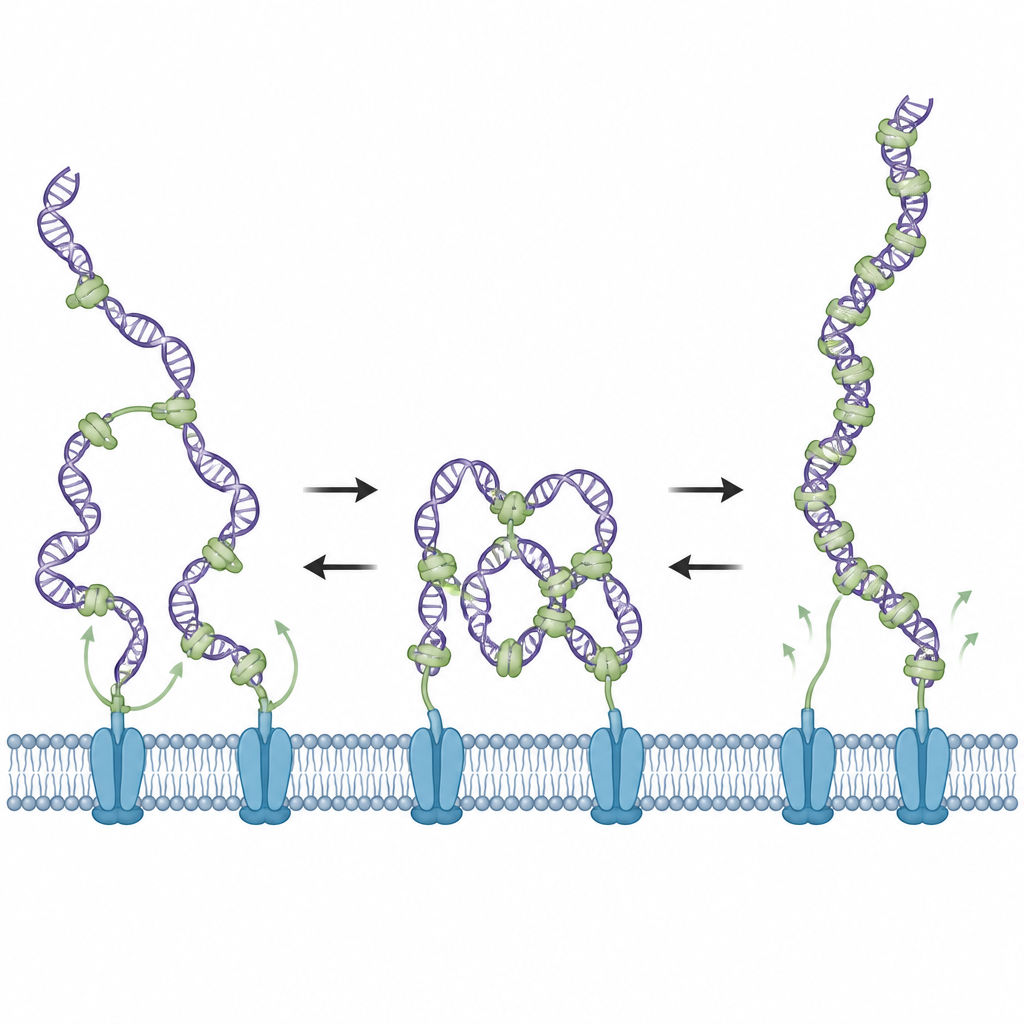
Das flexible Verbindungsstück des Proteins ingenieurmäßig verändern
ComEA besitzt ein flexibles Linker‑Segment, das seinen DNA‑greifenden Teil mit dem Bereich verbindet, der das Zusammenlagern mit anderen ComEA‑Molekülen ermöglicht. Das Team verkürzte bzw. verlängerte dieses Linker‑Segment, um dessen Wirkung zu testen. Kurzlinker‑Mutanten bevorzugten den entspannten, nicht‑überbrückenden Zustand und erzeugten keine Kondensationskräfte, während Langlinker‑Mutanten anhaltende Brückenbildung und Kraftentwicklung sogar bei hohen Proteinmengen begünstigten. Beide Mutantentypen banden DNA, waren jedoch jeweils schlecht darin, echte Bacillus subtilis‑Zellen zu transformieren, was zeigt, dass erfolgreiche DNA‑Aufnahme erfordert, dass ComEA zunächst kondensieren und später wieder entspannen kann.
Warum das für Antibiotikaresistenz wichtig ist
Die Ergebnisse sprechen zusammen für ein zweistufiges Modell, wie Gram‑positive Bakterien fremde DNA einziehen. Zu Beginn der Aufnahme überbrücken dünn verteilte ComEA‑Proteine getrennte DNA‑Abschnitte, kondensieren sie sanft und ziehen den Strang durch die dicke Zellwand in Richtung Membran. Wenn mehr ComEA an derselben DNA akkumuliert, schaltet es in einen nicht‑überbrückenden Modus um, der das Ziehen stoppt und der DNA erlaubt, sich wieder zu dekompaktieren, wodurch es für andere Transportproteine leichter wird, einen einzelnen DNA‑Strang ins Zellinnere zu führen. Diese reversible Kondensation liefert gerade genug richtungsgebende Vorspannung, um DNA zu bewegen, ohne dem späteren Transportschritt entgegenzuwirken, und erklärt, wie Bakterien effizient neue Gene erwerben können, darunter solche, die Antibiotikaresistenz vermitteln.
Zitation: Santiago, J.I., Ahmed, I., Hahn, J. et al. Reversible DNA condensation drives natural transformation. Nat Commun 17, 4242 (2026). https://doi.org/10.1038/s41467-026-70559-0
Schlüsselwörter: natürliche Transformation, DNA‑Aufnahme, ComEA, Antibiotikaresistenz, bakterielle Zellwand