Clear Sky Science · it
La condensazione reversibile del DNA guida la trasformazione naturale
Come i batteri prendono in prestito il DNA
La resistenza agli antibiotici può diffondersi quando i batteri raccolgono frammenti di DNA liberi nell’ambiente, un meccanismo noto come trasformazione naturale. Questo studio mostra come una singola proteina aiuti a tirare il DNA entrante attraverso la barriera esterna robusta di alcuni batteri, usando una routine sottile di spinta–trazione invece di un motore potente. Comprendere questa trazione microscopica potrebbe aiutare a sviluppare strategie per rallentare la diffusione dei geni di resistenza.
Un portale molecolare per nuovi geni
Molti batteri possono naturalmente acquisire frammenti di DNA dall’ambiente e integrare geni utili nel proprio cromosoma. Per farlo, il DNA deve attraversare la parete cellulare e raggiungere l’interno della cellula. Nei batteri Gram-positivi, che hanno una parete spessa, una proteina di membrana chiamata ComEA si trova nello spazio tra la parete e la membrana interna, dove afferra il DNA in arrivo. Finora si sapeva che ComEA era essenziale per questo processo, ma non si capiva come aiutasse concretamente il DNA a muoversi verso l’interno.
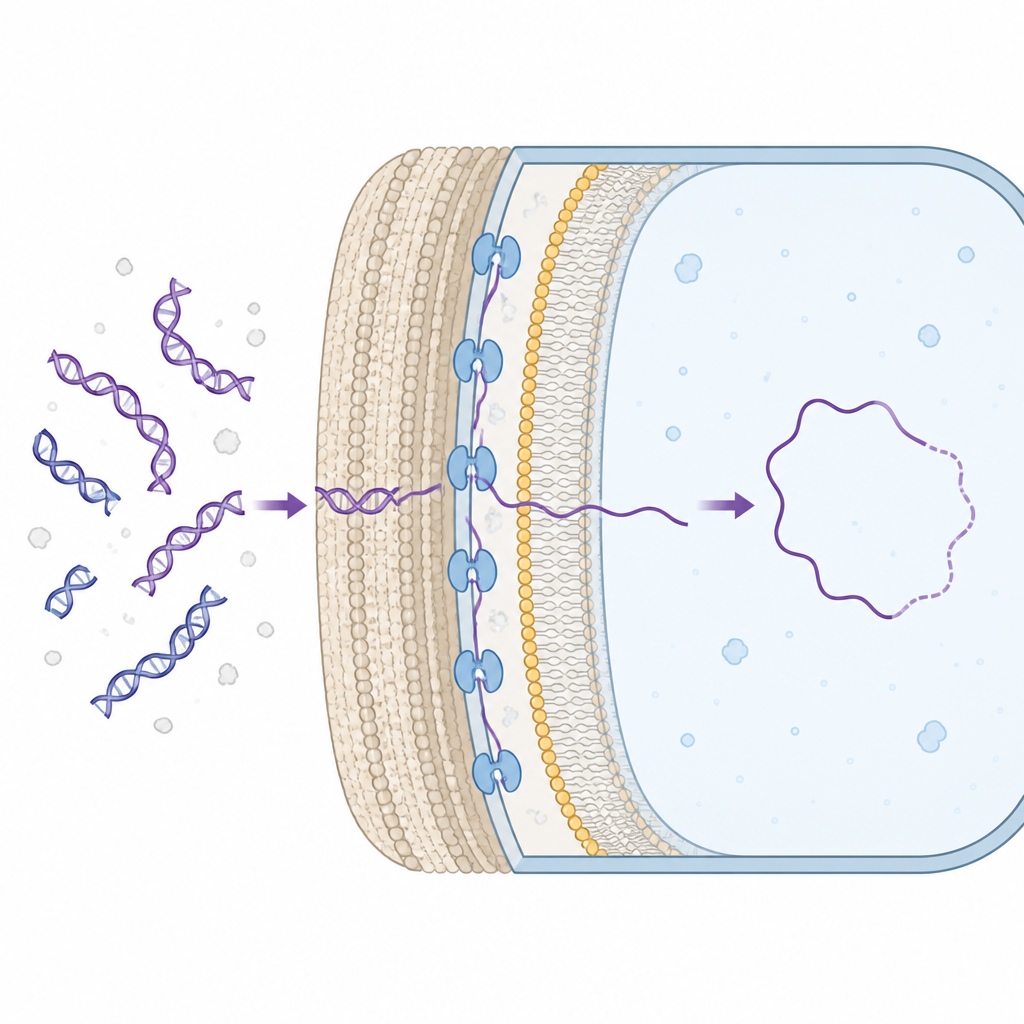
Tirate gentili sul DNA misurate una molecola alla volta
I ricercatori hanno usato le pinzette ottiche a singola molecola, una tecnica che tiene un singolo filamento di DNA tra due minuscoli perni usando la luce laser. Aggiungendo ComEA purificata e tirando sul DNA, hanno potuto osservare quando molecole di ComEA collegavano parti distanti del filamento tra loro, formando piccoli anelli. Man mano che si formavano più di questi ponti, la lunghezza complessiva del DNA si riduceva, mostrando che ComEA lo condensava. La rottura di questi ponti causava salti improvvisi nella lunghezza del DNA, permettendo al team di calcolare quanto DNA fosse stato anellato e quanta forza meccanica fosse stata generata. Hanno scoperto che ComEA può tirare con forze molto piccole, sotto il piconewton, sufficienti a indirizzare il movimento del DNA verso l’interno ma molto più deboli delle forze prodotte dai classici motori molecolari.
Un interruttore a due modalità: condensa, poi rilassa
La microscopia elettronica ha fornito agli scienziati istantanee dell’aspetto del DNA mescolato con ComEA. A livelli modesti di proteina si osservavano anelli e una compattazione parziale del DNA, coerenti con interazioni di bridging. All’aumentare della concentrazione di ComEA, questi anelli scomparivano, anche se la superficie del DNA risultava più spessa per la copertura proteica. Misure aggiuntive hanno mostrato che ad alta copertura ComEA forma comunque assemblaggi lungo il DNA ma in modo non ponte, stabilizzando il DNA teso anziché anellarlo. In questo stato affollato il DNA si decondensa e non subisce più forze di trazione, rivelando un interruttore intrinseco controllato dalla quantità locale di ComEA presente.
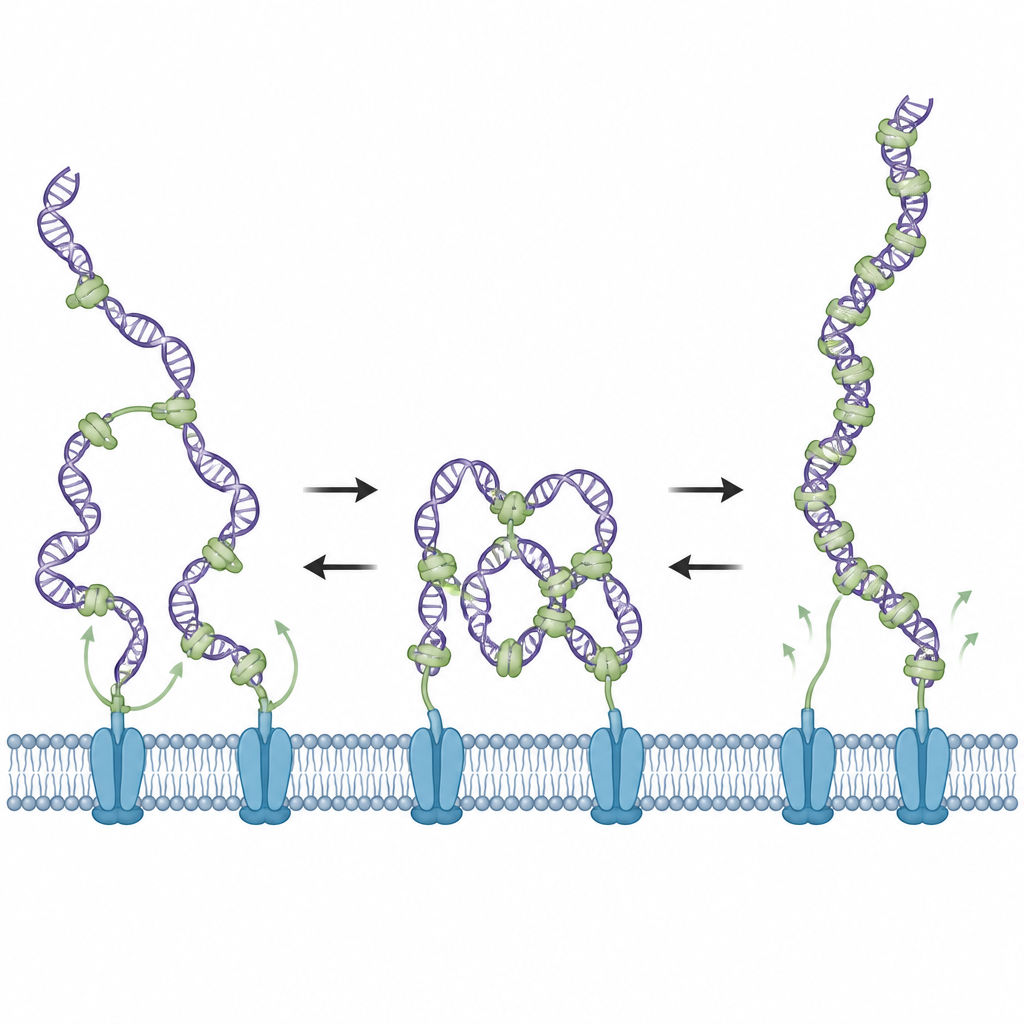
Progettare il link flessibile della proteina
ComEA contiene un link flessibile che collega la sua porzione che afferra il DNA alla parte che le permette di aggregarsi con altre molecole di ComEA. Il gruppo ha accorciato o allungato questo link per testarne l’effetto sul comportamento. I mutanti con link più corti favorivano lo stato rilassato e non ponte e non riuscivano a generare forze di condensazione, mentre i mutanti con link più lunghi tendevano a mantenere ponti persistenti e a generare forza anche a livelli proteici elevati. Entrambi i tipi di mutanti si legavano al DNA, ma si dimostrarono inefficaci nel trasformare cellule reali di Bacillus subtilis, dimostrando che l’acquisizione riuscita del DNA richiede che ComEA possa sia condensare il DNA inizialmente sia poi lasciarlo rilassare.
Perché questo è importante per la resistenza agli antibiotici
Nel complesso, i risultati supportano un modello a due fasi per come i batteri Gram-positivi richiamano DNA estraneo. All’inizio dell’assorbimento, proteine ComEA scarsamente legate fanno da ponte tra tratti separati di DNA, condensandolo dolcemente e tirando il filamento attraverso la spessa parete verso la membrana. Man mano che più ComEA si accumula sullo stesso DNA, la proteina passa a una modalità non ponte che interrompe la trazione e permette al DNA di decondensarsi, facilitando il lavoro di altre proteine di trasporto che possono instradare un singolo filamento nell’interno della cellula. Questa condensazione reversibile fornisce il bias direzionale necessario per muovere il DNA senza ostacolare il successivo passaggio di trasporto, aiutando a spiegare come i batteri acquisiscono efficacemente nuovi geni che possono includere la resistenza agli antibiotici.
Citazione: Santiago, J.I., Ahmed, I., Hahn, J. et al. Reversible DNA condensation drives natural transformation. Nat Commun 17, 4242 (2026). https://doi.org/10.1038/s41467-026-70559-0
Parole chiave: trasformazione naturale, acquisizione del DNA, ComEA, resistenza agli antibiotici, parete cellulare batterica