Clear Sky Science · pt
Condensação reversível de DNA impulsiona a transformação natural
Como as bactérias pegam emprestado DNA
A resistência a antibióticos pode se espalhar quando bactérias capturam fragmentos de DNA soltos do ambiente, um truque conhecido como transformação natural. Este estudo revela como uma única proteína ajuda a puxar o DNA que chega através da barreira externa resistente de certas bactérias, usando uma rotina sutil de empurrar–puxar em vez de um motor poderoso. Entender essa disputa microscópica pode orientar estratégias futuras para desacelerar a disseminação de genes de resistência.
Uma passagem molecular para novos genes
Muitas bactérias podem naturalmente captar fragmentos de DNA do ambiente e incorporar genes úteis aos seus próprios cromossomos. Para isso, o DNA precisa atravessar a parede celular e alcançar o interior da célula. Em bactérias Gram-positivas, que têm parede celular espessa, uma proteína de membrana chamada ComEA localiza-se no espaço entre a parede e a membrana interna, onde agarra o DNA que chega. Até agora, os cientistas sabiam que o ComEA era essencial para esse processo, mas não compreendiam como ele ajudava efetivamente a mover o DNA para o interior.
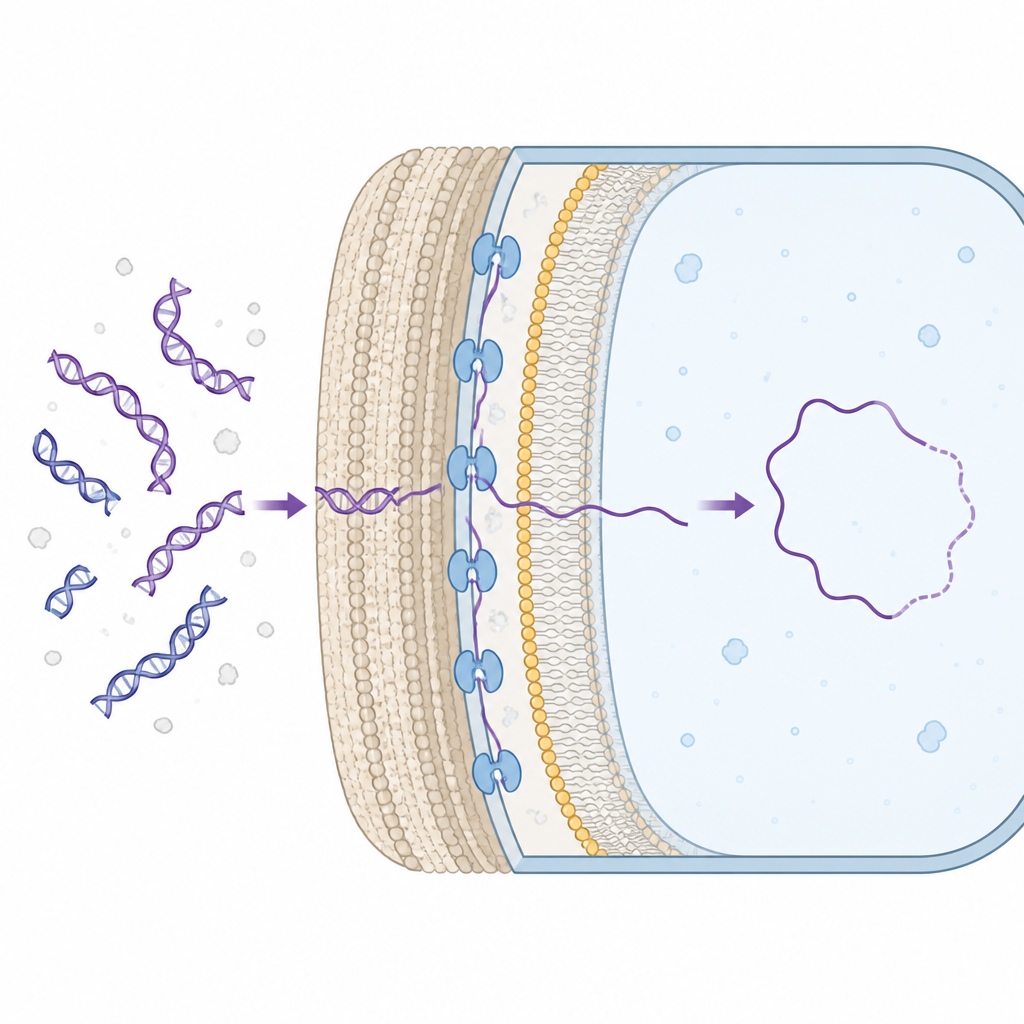
Puxões suaves no DNA medidos molécula a molécula
Os pesquisadores usaram pinças ópticas em nível de molécula única, uma técnica que prende um único filamento de DNA entre duas microesferas usando luz laser. Ao adicionar ComEA purificado e puxar o DNA, eles puderam ver quando moléculas de ComEA conectavam partes distantes da fita, formando pequenos laços. À medida que mais dessas pontes se formavam, o comprimento efetivo do DNA encolhia, mostrando que o ComEA o estava condensando. A quebra dessas pontes causava saltos repentinos no comprimento do DNA, permitindo à equipe calcular quanto DNA havia sido emaranhado e que força mecânica foi gerada. Eles descobriram que o ComEA pode puxar com forças muito pequenas, sub-piconewton, suficientes para direcionar o movimento do DNA para dentro, mas muito mais fracas que as forças produzidas por motores moleculares clássicos.
Um interruptor em dois modos: condensar, depois relaxar
A microscopia eletrônica forneceu instantâneos da aparência do DNA misturado com ComEA. Em níveis moderados de proteína, observaram-se laços e compactação parcial do DNA, consistentes com interações de ponte. À medida que a concentração de ComEA aumentou ainda mais, esses laços desapareceram, embora a superfície do DNA ficasse mais densamente revestida por proteína. Medidas adicionais mostraram que, em alta cobertura, o ComEA ainda forma agregados ao longo do DNA, mas agora de maneira que não faz pontes, estabilizando o DNA estendido em vez de formá-lo em laços. Nesse estado congestionado, o DNA se decondensa e não experimenta mais forças de tração, revelando um interruptor embutido controlado pela quantidade de ComEA presente localmente.
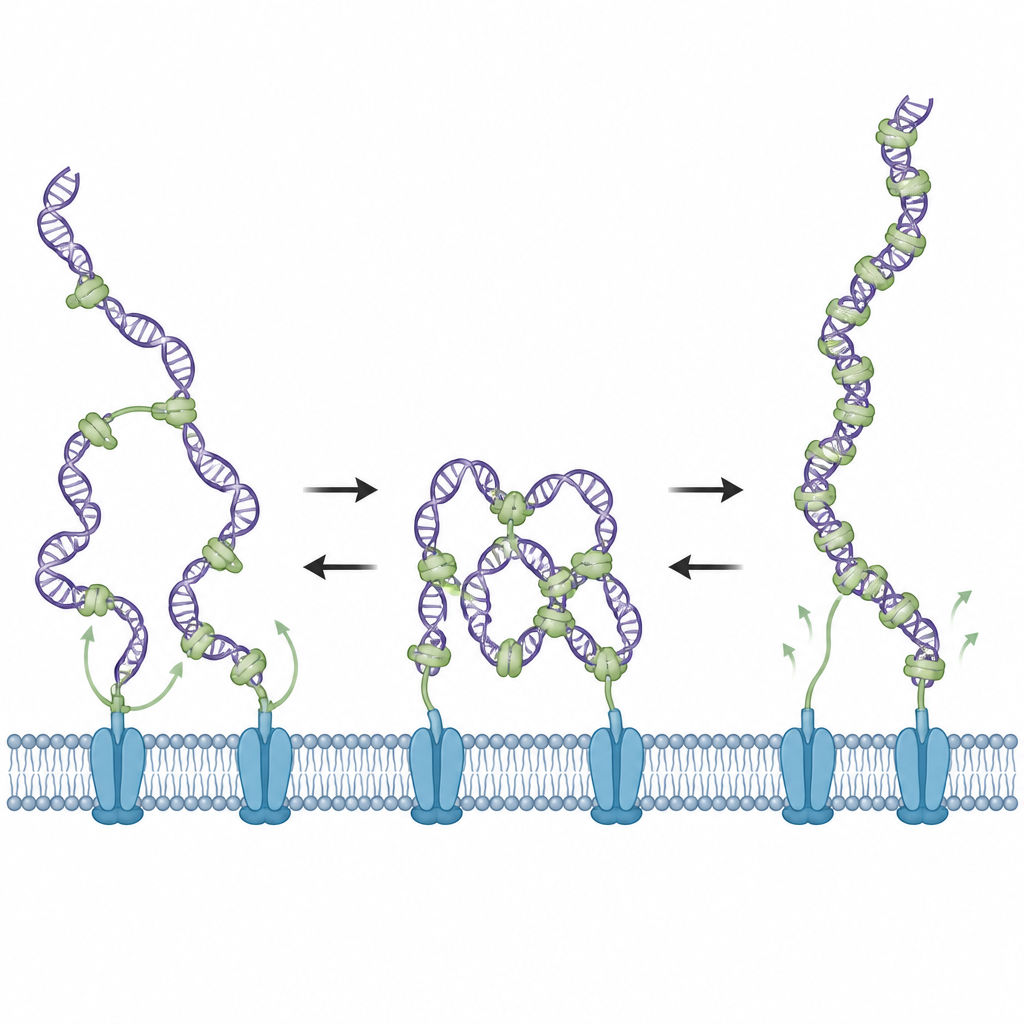
Engenharia do elo flexível da proteína
O ComEA contém um elo flexível que conecta sua porção que prende o DNA à parte que permite seu agrupamento com outras moléculas de ComEA. A equipe encurtou ou alongou esse elo para testar como isso afetava o comportamento. Mutantes com elo curto favoreceram o estado relaxado e não pontilhante, e falharam em gerar forças de condensação, enquanto mutantes com elo longo favoreceram pontes persistentes e geração de força mesmo em altos níveis de proteína. Ambos os tipos de mutantes ligavam o DNA, mas foram ineficientes em transformar células reais de Bacillus subtilis, mostrando que a captação bem-sucedida de DNA requer que o ComEA seja capaz tanto de condensar o DNA inicialmente quanto de permitir que ele se relaxe depois.
Por que isso importa para a resistência a antibióticos
Em conjunto, os resultados sustentam um modelo em duas etapas de como bactérias Gram-positivas puxam DNA estrangeiro. No início da captação, moléculas de ComEA escassamente ligadas fazem pontes entre trechos separados de DNA, condensando-o suavemente e atraindo a fita através da espessa parede celular em direção à membrana. À medida que mais ComEA se acumula no mesmo DNA, ele muda para um modo não pontilhante que interrompe a tração e permite que o DNA se decondense, facilitando que outras proteínas de transporte alimentem uma única fita de DNA para o interior da célula. Essa condensação reversível fornece um viés direcional suficiente para mover o DNA sem atrapalhar a etapa de transporte posterior, ajudando a explicar como as bactérias adquirem eficientemente novos genes que podem incluir resistência a antibióticos.
Citação: Santiago, J.I., Ahmed, I., Hahn, J. et al. Reversible DNA condensation drives natural transformation. Nat Commun 17, 4242 (2026). https://doi.org/10.1038/s41467-026-70559-0
Palavras-chave: transformação natural, captação de DNA, ComEA, resistência a antibióticos, parede celular bacteriana