Clear Sky Science · pl
Odwracalna kondensacja DNA napędza naturalną transformację
Jak bakterie pożyczają DNA
Oporność na antybiotyki może się rozprzestrzeniać, gdy bakterie przechwytują luźne DNA z otoczenia — proces znany jako naturalna transformacja. To badanie pokazuje, jak pojedyncze białko pomaga przeciągnąć napływające DNA przez trudną zewnętrzną barierę niektórych bakterii, stosując subtelny manewr pchania i ciągnięcia zamiast silnego silnika. Zrozumienie tego mikroskopijnego przeciągania liny może pomóc w opracowaniu strategii spowalniających rozprzestrzenianie się genów oporności.
Molekularna brama dla nowych genów
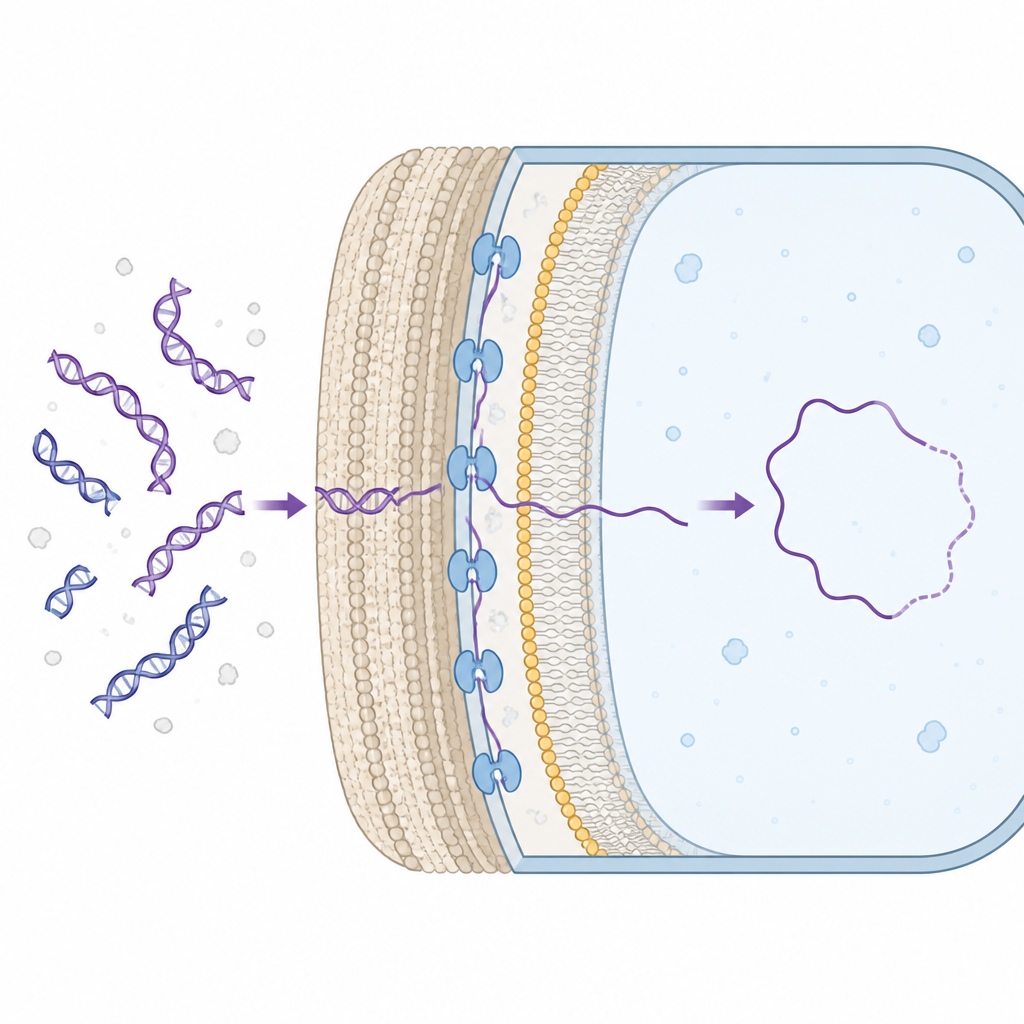
Wiele bakterii potrafi naturalnie pobierać fragmenty DNA ze środowiska i włączać użyteczne geny do własnego chromosomu. Aby to zrobić, DNA musi przekroczyć ścianę komórkową i dotrzeć do wnętrza komórki. U bakterii Gram-dodatnich, które mają grubą ścianę komórkową, białko błonowe zwane ComEA znajduje się w przestrzeni między ścianą a błoną wewnętrzną, gdzie chwyta napływające DNA. Do tej pory naukowcy wiedzieli, że ComEA jest niezbędne w tym procesie, ale nie rozumieli, w jaki sposób faktycznie pomaga przemieszczać DNA do wnętrza.
Delikatne pociągnięcia DNA mierzone pojedynczą cząsteczką
Naukowcy użyli optycznych pęset pojedynczych cząsteczek — techniki, która utrzymuje pojedynczy fragment DNA między dwiema maleńkimi kuleczkami za pomocą światła lasera. Dodając oczyszczone ComEA i napinając DNA, mogli zaobserwować, kiedy cząsteczki ComEA łączyły odległe fragmenty nici, tworząc małe pętle. W miarę powstawania kolejnych takich mostków, efektywna długość DNA malała, co pokazywało, że ComEA je kondensuje. Zerwanie tych mostków powodowało nagłe skoki długości DNA, co pozwoliło zespołowi obliczyć, ile DNA zostało pętlowane i jaką siłę mechaniczną wygenerowano. Odkryli, że ComEA może ciągnąć z bardzo małymi, subpikonewtonowymi siłami — wystarczającymi, by faworyzować ruch DNA do wnętrza, ale znacznie słabszymi niż siły wytwarzane przez klasyczne molekularne silniki.
Przełącznik w dwóch trybach: kondensuj, potem rozluźnij
Mikroskopia elektronowa dostarczyła naukowcom migawek wyglądu DNA zmieszanego z ComEA. Przy umiarkowanych stężeniach białka zaobserwowano pętle i częściową kompakcję DNA, zgodne z interakcjami mostkującymi. W miarę wzrostu stężenia ComEA pętle znikały, mimo że powierzchnia DNA była coraz bardziej pokryta białkiem. Dalsze pomiary wykazały, że przy wysokim pokryciu ComEA nadal tworzy zespoły wzdłuż DNA, ale teraz w trybie niemostkującym, który stabilizuje rozciągnięte DNA zamiast go pętlować. W tym zagęszczonym stanie DNA ulega dekondensacji i przestaje doświadczać sił ciągnących, odkrywając wbudowany przełącznik kontrolowany lokalną ilością ComEA.
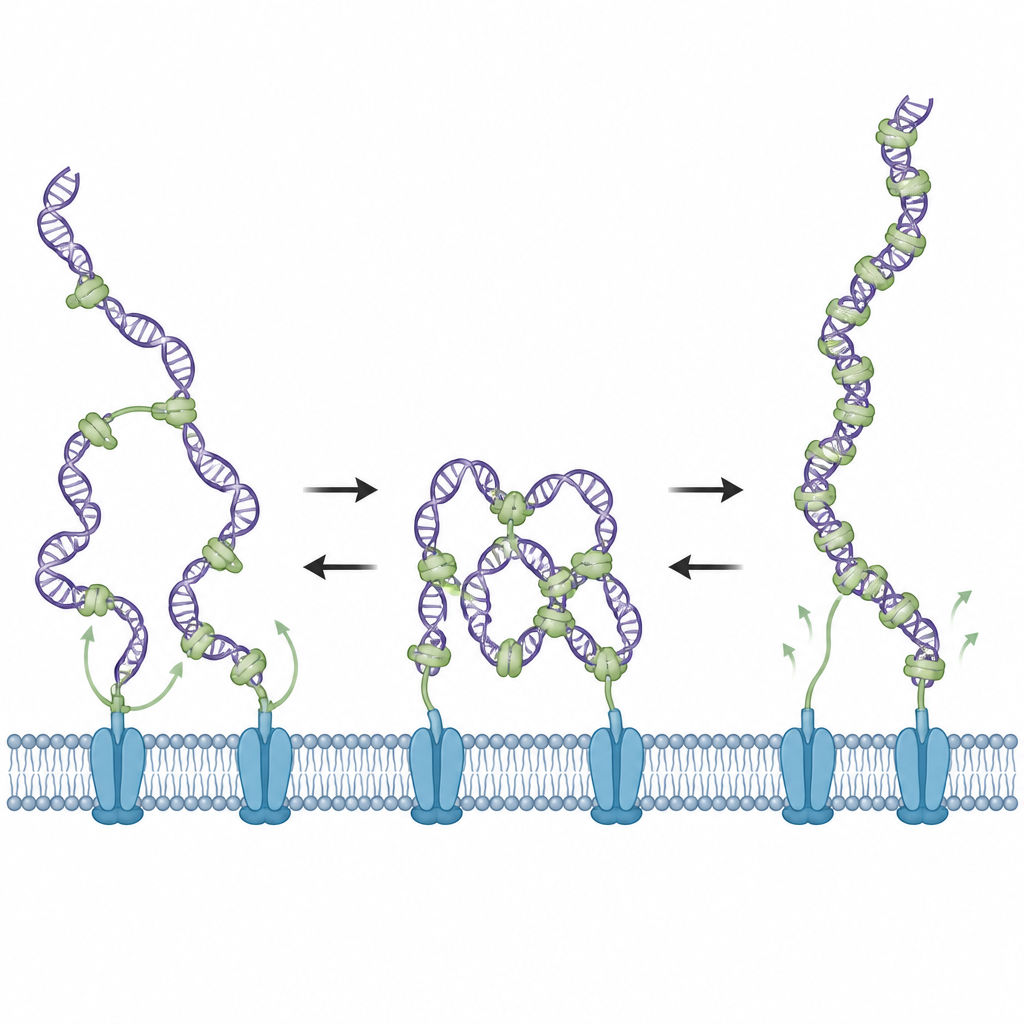
Inżynieria elastycznego łącznika białka
ComEA zawiera elastyczny łącznik, który łączy część chwytającą DNA z fragmentem pozwalającym mu agregować z innymi cząsteczkami ComEA. Zespół skrócił lub wydłużył ten łącznik, aby sprawdzić, jak wpływa to na zachowanie białka. Mutanty ze skróconym łącznikiem sprzyjały zrelaksowanemu, niemostkującemu stanowi i nie generowały sił kondensacyjnych, podczas gdy mutanty z długim łącznikiem utrzymywały trwałe mostkowanie i generowanie sił nawet przy wysokich stężeniach białka. Oba typy mutantów wiązały DNA, lecz były słabe w transformacji rzeczywistych komórek Bacillus subtilis, co pokazuje, że skuteczne pobieranie DNA wymaga od ComEA zdolności zarówno do początkowej kondensacji DNA, jak i do późniejszego jego rozluźnienia.
Dlaczego to ma znaczenie dla oporności na antybiotyki
Podsumowując, wyniki wspierają dwustopniowy model tego, jak bakterie Gram-dodatnie wciągają obce DNA. Na wczesnym etapie pobierania rzadko związane cząsteczki ComEA mostkują oddzielne odcinki DNA, delikatnie kondensując i przesuwając nić przez grubą ścianę komórkową w kierunku błony. W miarę gromadzenia się większej ilości ComEA na tym samym fragmencie DNA przełącza się on w tryb niemostkujący, który przerywa ciągnięcie i pozwala DNA się rozluźnić, ułatwiając innym białkom transportowym wprowadzenie pojedynczej nici do wnętrza komórki. Ta odwracalna kondensacja zapewnia wystarczające ukierunkowanie ruchu DNA bez utrudniania kolejnego etapu transportu, pomagając wyjaśnić, jak bakterie efektywnie nabywają nowe geny, w tym te odpowiedzialne za oporność na antybiotyki.
Cytowanie: Santiago, J.I., Ahmed, I., Hahn, J. et al. Reversible DNA condensation drives natural transformation. Nat Commun 17, 4242 (2026). https://doi.org/10.1038/s41467-026-70559-0
Słowa kluczowe: naturalna transformacja, pobieranie DNA, ComEA, oporność na antybiotyki, ściana komórkowa bakterii