Clear Sky Science · zh
猕猴皮层与疾病相关基因的顺式调控元件单细胞空间图谱
为何这张脑图重要
许多脑部疾病——从精神分裂症到阿尔茨海默病——具有家族遗传倾向,但增加风险的DNA变化常位于不编码蛋白质的基因组区域,功能难以解释。本研究通过绘制一张详尽图谱,展示了数百万个微小DNA开关在猕猴皮层中不同细胞类型和位置的运作方式,来攻克这一难题。将这些开关与细胞身份及人类疾病风险相联系,研究为理解为什么某些脑细胞与区域在精神和神经退行性疾病中尤其脆弱提供了新的视角。
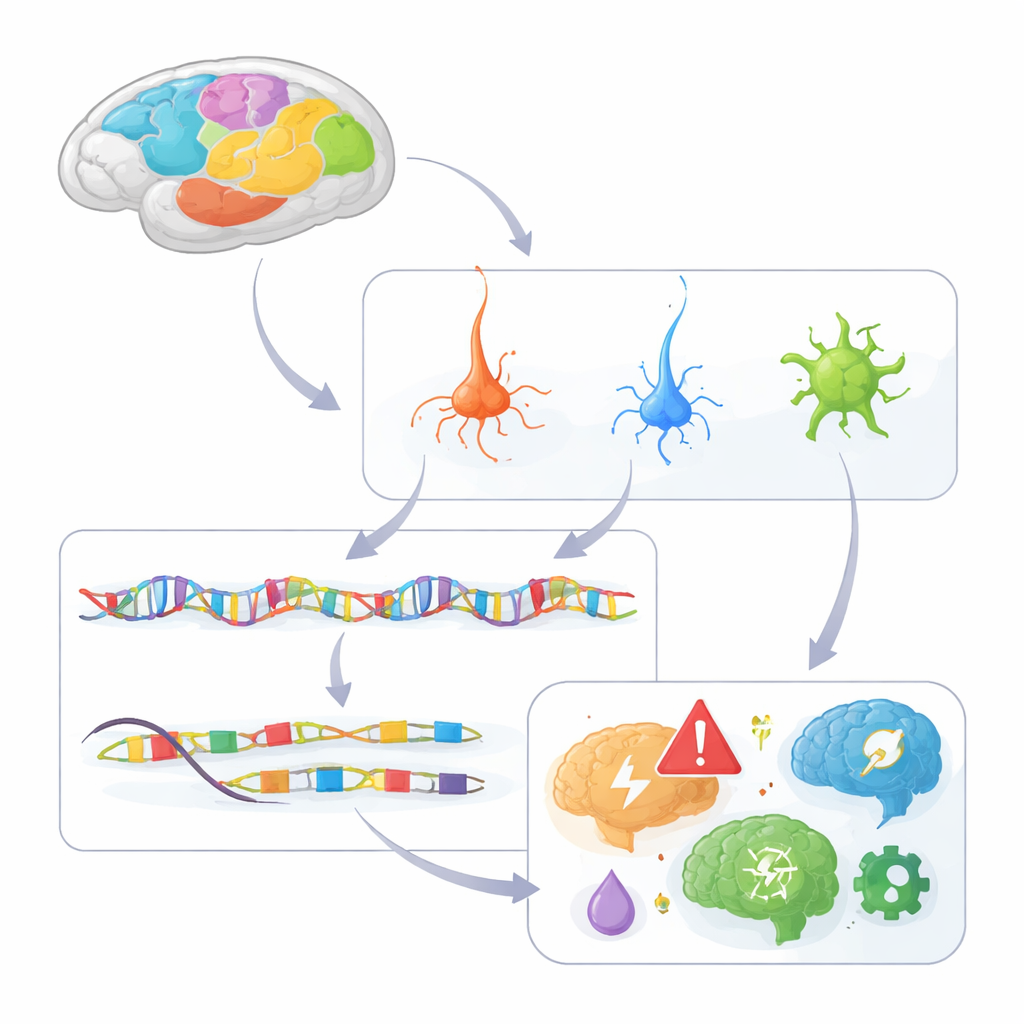
构建灵长类皮层的细胞水平图谱
研究者分析了来自猕猴皮层142个区域约160万个单个细胞核的染色质可及性——即DNA的开放或关闭状态。开放的DNA区段标记顺式调控元件,作为控制邻近基因的“开/关”开关。借助一种基于微滴的单细胞核ATAC-seq方法,他们将细胞分为230种不同类型,涵盖兴奋性谷氨酸能神经元、抑制性GABA能神经元以及多种支持细胞,如星形胶质细胞、少突胶质细胞和小胶质细胞。他们鉴定出超过60万个候选调控元件,并将许多元件与特定靶基因关联起来,构建了皮层调控连线图的初稿。
分层与区域性的基因控制模式
通过将这一DNA开关图与高分辨率的基因表达空间图结合,团队能够观察不同调控元件在六层皮层与各叶区内的活跃分布。许多开关显示出显著的层和区域偏好。例如,与上层神经元标志基因相关的元件主要在第2层和第3层活跃,而另一些则限于更深层。某些开关仅在初级视觉皮层(V1)高度活跃,这有助解释为何某些神经元类型与基因程序在该区域独特。研究还揭示了进化上更古老的嗅球皮层(piriform cortex)与新皮层之间的对比:在胶质细胞与深层神经元中分别活跃着不同的开关,指向塑造这些结构的不同调控程序。
关键神经元类型中的灵长类创新
将猕猴数据与人类和小鼠皮层的类似图谱比较,作者发现某些神经元亚类仅存在于灵长类,尤其是第4层的部分谷氨酸能神经元和一种特殊的抑制性细胞群体,称为LAMP5/LHX6中间神经元。这些细胞携带许多在人类和猕猴中开放但在小鼠中不开放的调控元件,其中一些似乎伴随可移动的转座元件出现——这些移动DNA序列可促成新的基因开关。灵长类特有的开关调控与突触功能、神经发育和神经元通信相关的基因,表明较近期的调控变化可能推动了灵长类皮层回路的多样化,尤其涉及与复杂感知和认知相关的那些层次。
支持细胞与可塑性背后的连线
该图谱也阐明了非神经元细胞的特征。少突胶质细胞前体与成熟少突胶质细胞在皮层层级上呈现相反的丰度分布:高阶区域具有更多前体细胞和更少成熟的髓鞘形成细胞,暗示这些区域在调整连线方面具有更大的灵活性。它们的调控元件反映了这一梯度,并在与突触和视觉系统相关的灵长类偏向开关中富集。星形胶质细胞分为集中于顶层的层间细胞和分布于更深层的原浆细胞,各自受不同开关和转录因子的控制。这些模式表明,不仅是神经元,支持、绝缘和重塑它们的细胞也受区域特异性调控程序调节,可能影响学习能力和对损伤的易感性。
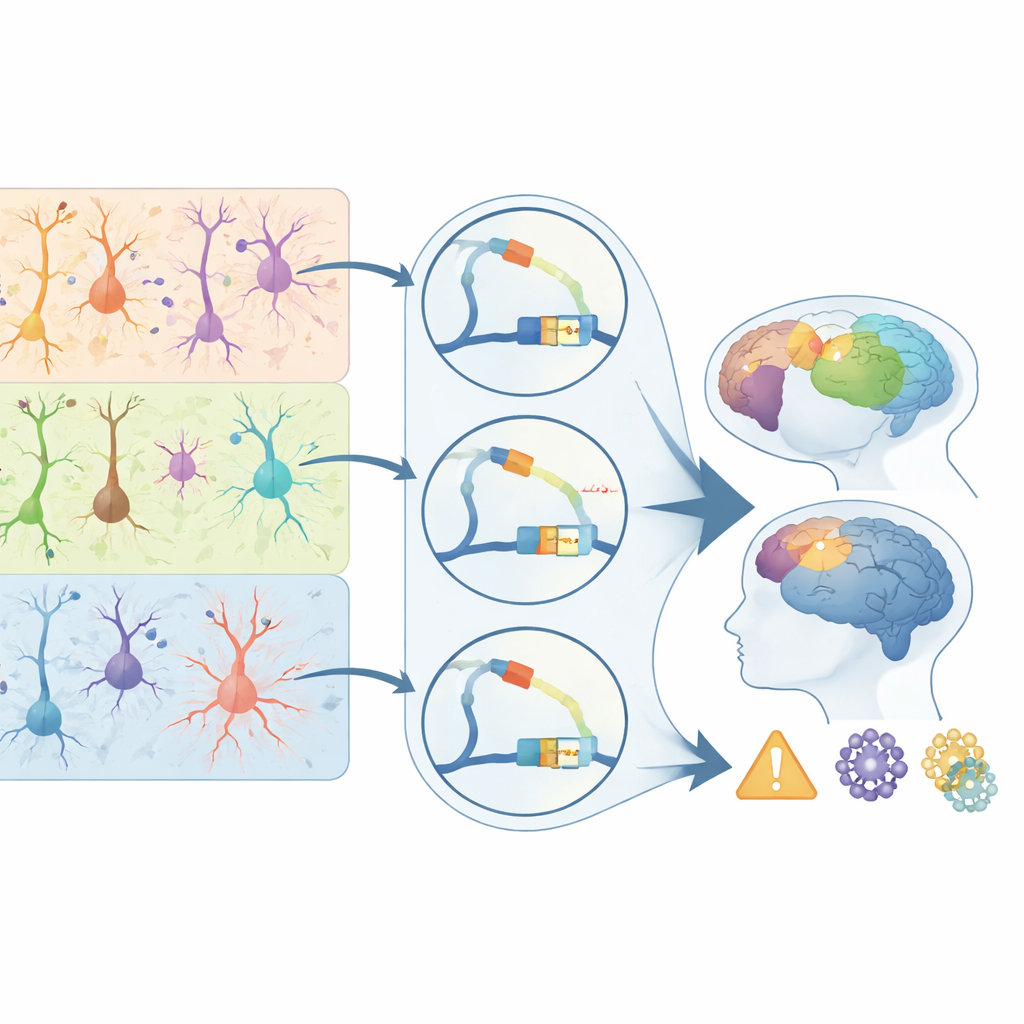
将DNA开关与脑疾病风险相连
为了把他们的灵长类图谱与人类健康联系起来,作者将其与28种与大脑相关的疾病和性状的遗传研究叠加分析。他们发现,疾病相关变体不成比例地集中在特定细胞类型活跃的调控元件中。精神分裂症和双相情感障碍的风险变体聚集在上层兴奋性神经元使用的开关中;癫痫的信号在某些抑制性细胞中富集;阿尔茨海默病的风险变体显著集中在小胶质细胞的调控元件中。许多这些与疾病相关的开关具有灵长类偏向,尤其是在精神分裂症相关的第4层神经元中和阿尔茨海默病相关的小胶质细胞中,它们靶向已知影响突触、免疫反应和蛋白质清除的基因。对普通读者而言,核心信息是疾病风险往往不是通过直接破坏蛋白质发挥作用,而是通过微妙地重塑基因在特定细胞何时何地被激活。本研究提供了一幅在灵长类皮层中这些控制点的里程碑式图谱,澄清了为何某些细胞类型和区域成为疾病热点,并为未来旨在修正大脑调控代码(而非蛋白质本身)的治疗策略提供了指南。
引用: Meng, J., Chen, C., Zhu, Z. et al. Single-cell spatial map of cis-regulatory elements for disease-related genes in the macaque cortex. Nat Commun 17, 4041 (2026). https://doi.org/10.1038/s41467-026-70497-x
关键词: 单细胞表观基因组学, 灵长类皮层, 基因调控, 脑部疾病, 顺式调控元件