Clear Sky Science · fr
Carte spatiale unicellulaire des éléments cis-régulateurs pour les gènes liés aux maladies dans le cortex du macaque
Pourquoi cette carte cérébrale est importante
De nombreuses maladies cérébrales, de la schizophrénie à la maladie d’Alzheimer, sont familiales — mais les variations d’ADN qui augmentent le risque se trouvent souvent dans des régions mystérieuses du génome qui ne codent pas pour des protéines. Cette étude relève ce défi en créant une carte détaillée de la façon dont des millions de petits interrupteurs d’ADN fonctionnent selon les types cellulaires et les emplacements dans le cortex de macaques, nos proches parents primates. En reliant ces interrupteurs à l’identité cellulaire et au risque de maladie humaine, le travail offre une nouvelle fenêtre pour comprendre pourquoi certaines cellules et régions cérébrales sont particulièrement vulnérables dans les troubles psychiatriques et neurodégénératifs.
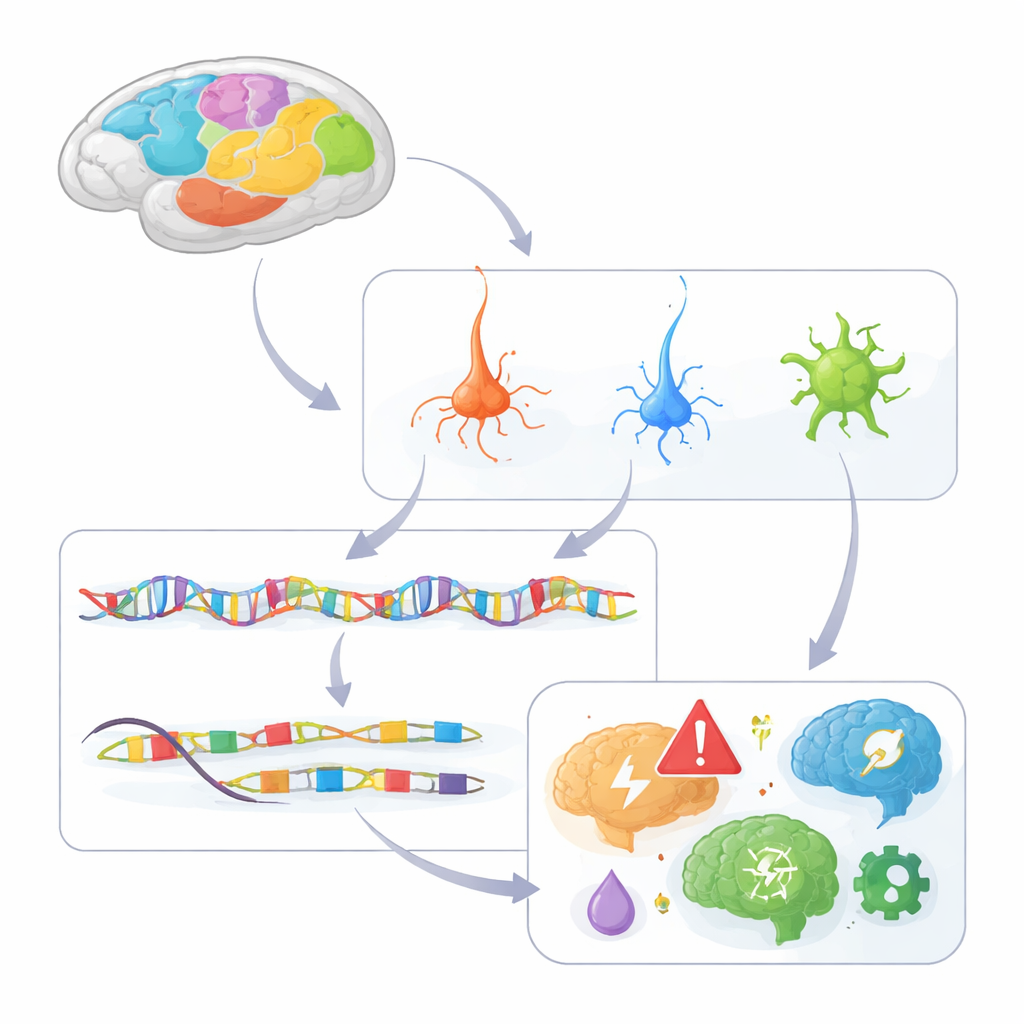
Construire un atlas cellulaire du cortex de primate
Les chercheurs ont analysé l’accessibilité de la chromatine — c’est‑à‑dire à quel point l’ADN est ouvert ou fermé — dans environ 1,6 million de noyaux individuels prélevés dans 142 régions du cortex de macaque. Les régions d’ADN ouvertes marquent les éléments cis-régulateurs, les interrupteurs « marche/arrêt » qui contrôlent les gènes voisins. À l’aide d’une méthode en gouttelettes appelée single-nucleus ATAC-seq, ils ont regroupé les cellules en 230 types distincts, couvrant les neurones glutamatergiques excitateurs, les neurones GABAergiques inhibitifs et divers cellules de soutien telles que les astrocytes, oligodendrocytes et microglies. Ils ont identifié plus de 600 000 éléments régulateurs candidats et lié beaucoup d’entre eux à des gènes cibles spécifiques, élaborant un premier brouillon du schéma de câblage régulateur du cortex.
Schémas superposés de contrôle génique selon la couche et la région
En combinant cet atlas des interrupteurs d’ADN avec une carte spatiale à haute résolution de l’activité génique, l’équipe a pu voir où, au sein des six couches corticales et des différents lobes, différents éléments régulateurs sont actifs. De nombreux interrupteurs présentent de fortes préférences de couche et de région. Par exemple, des éléments associés à des gènes marquant les neurones des couches supérieures étaient principalement actifs dans les couches 2 et 3, tandis que d’autres étaient confinés aux couches profondes. Certains interrupteurs étaient fortement actifs uniquement dans le cortex visuel primaire (V1), ce qui aide à expliquer pourquoi certains types neuronaux et programmes géniques sont propres à cette région. L’étude a aussi mis en évidence des contrastes entre le cortex piriforme, plus ancien sur le plan évolutif, et le néocortex, avec des ensembles d’interrupteurs différents actifs dans les cellules gliales par rapport aux neurones des couches profondes, suggérant des programmes régulateurs distincts qui façonnent ces architectures.
Innovations propres aux primates dans des types neuronaux clés
En comparant les données du macaque avec des cartes similaires du cortex humain et de la souris, les auteurs ont identifié des sous‑classes neuronales présentes uniquement chez les primates, notamment certains neurones glutamatergiques de la couche 4 et un groupe spécialisé de cellules inhibitrices appelées interneurones LAMP5/LHX6. Ces cellules portaient de nombreux éléments régulateurs ouverts chez l’homme et le macaque mais pas chez la souris, et certains de ces éléments semblent être apparus en lien avec des éléments transposables — des séquences d’ADN mobiles qui peuvent contribuer à la création de nouveaux interrupteurs géniques. Les interrupteurs propres aux primates régulent des gènes impliqués dans la fonction synaptique, le développement neuronal et la communication neuronale, suggérant que des changements régulateurs relativement récents ont contribué à diversifier les circuits corticaux propres aux primates, en particulier dans les couches associées à la perception et à la cognition complexes.
Cellules de soutien et le câblage derrière la plasticité
La carte éclaire également les cellules non neuronales. Les cellules progénitrices des oligodendrocytes et les oligodendrocytes matures montraient des abondances opposées le long de la hiérarchie corticale : les régions de niveau supérieur contenaient plus de précurseurs et moins de cellules matures myélinisantes, ce qui suggère une plus grande flexibilité pour ajuster le câblage à ces endroits. Leurs éléments régulateurs suivaient ce gradient et étaient enrichis en interrupteurs biaisés chez les primates associés aux gènes de la synapse et du système visuel. Les astrocytes se répartissaient en cellules interlaminaires concentrées dans la couche supérieure et en cellules protoplasmiques distribuées dans les couches profondes, chacune contrôlée par des ensembles distincts d’interrupteurs et de facteurs de transcription. Ces motifs indiquent que non seulement les neurones, mais aussi les cellules qui les nourrissent, les isolent et les remodelent, sont réglés par des programmes régulateurs spécifiques aux régions, susceptibles d’influencer la capacité d’apprentissage et la vulnérabilité aux dommages.
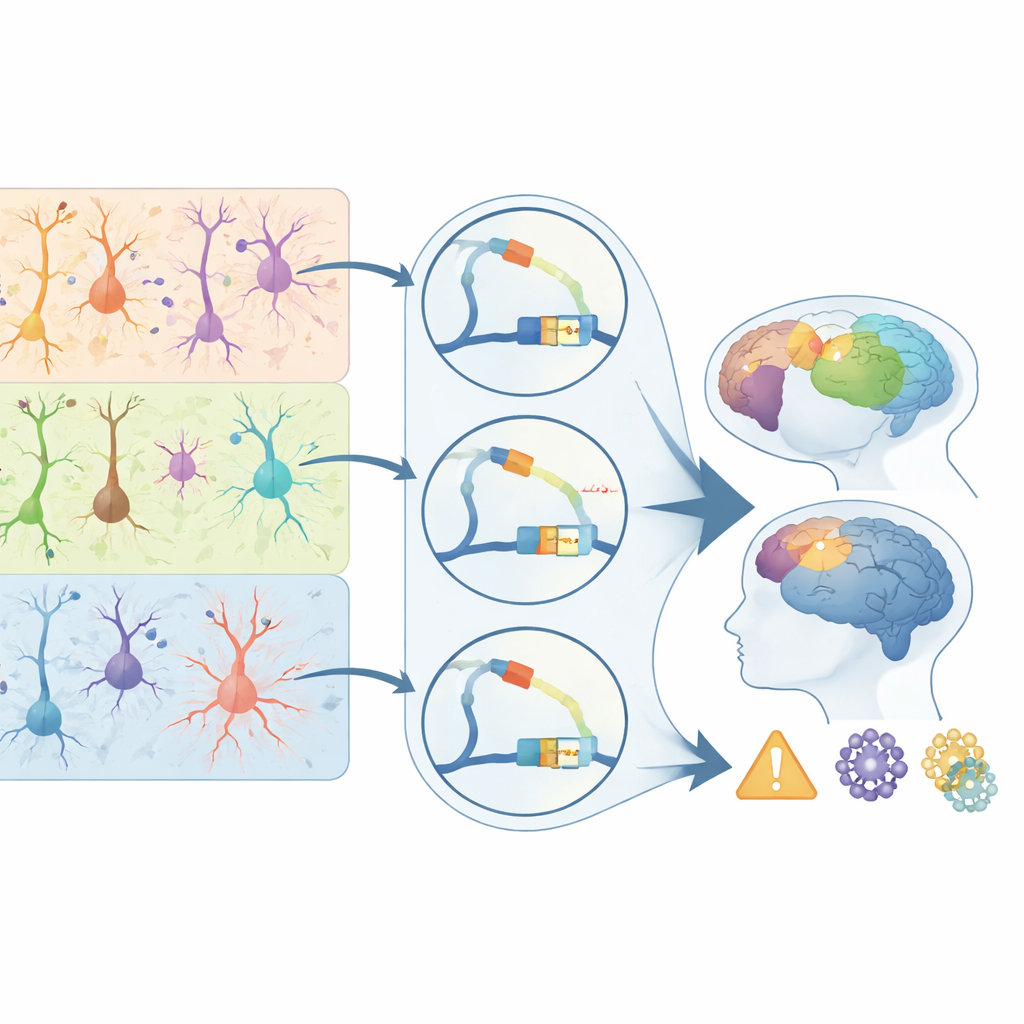
Relier les interrupteurs d’ADN au risque de maladies cérébrales
Pour faire le lien entre leur atlas de primate et la santé humaine, les auteurs l’ont superposé aux études génétiques de 28 troubles et traits liés au cerveau. Ils ont découvert que les variants associés aux maladies se trouvent de manière disproportionnée dans des éléments régulateurs actifs dans des types cellulaires spécifiques. Les variants de risque pour la schizophrénie et le trouble bipolaire se regroupent dans des interrupteurs utilisés par les neurones excitateurs des couches supérieures ; les signaux liés à l’épilepsie sont enrichis dans certains neurones inhibiteurs ; et les variants de risque pour la maladie d’Alzheimer se concentrent de façon frappante dans les éléments régulateurs des microglies. Nombre de ces interrupteurs associés aux maladies sont biaisés chez les primates, notamment dans les neurones de la couche 4 pour la schizophrénie et dans les microglies pour Alzheimer, et ils ciblent des gènes connus pour influencer les synapses, les réponses immunitaires et l’élimination des protéines. Pour le lecteur non spécialiste, le message principal est que le risque de maladie n’agit souvent pas en endommageant directement les protéines, mais en réécrivant subtilement quand et où les gènes s’expriment dans des cellules particulières. Cette étude fournit une carte de référence de ces points de contrôle régulateurs dans le cortex des primates, clarifiant pourquoi certains types cellulaires et régions sont des points chauds de maladies et offrant une boussole pour des thérapies futures visant à corriger le code régulateur du cerveau plutôt que ses composants protéiques.
Citation: Meng, J., Chen, C., Zhu, Z. et al. Single-cell spatial map of cis-regulatory elements for disease-related genes in the macaque cortex. Nat Commun 17, 4041 (2026). https://doi.org/10.1038/s41467-026-70497-x
Mots-clés: épigénomique unicellulaire, cortex de primate, régulation génique, troubles cérébraux, éléments cis-régulateurs