Clear Sky Science · ja
マカク皮質における疾病関連遺伝子のシス調節要素の単一細胞空間マップ
この脳地図が重要な理由
統合失調症からアルツハイマー病まで、多くの脳疾患は家族内で起こりやすい一方で、リスクを高めるDNA変化はタンパク質をコードしない不明瞭なゲノム領域に存在することが多い。本研究は、この謎に取り組み、マカク(ヒトに近い霊長類)の皮質全域にわたる異なる細胞型と場所で数百万の小さなDNAスイッチがどのように働くかを詳細に描いた地図を作成した。これらのスイッチを細胞の同一性やヒトの疾患リスクと結びつけることで、なぜ特定の脳細胞や領域が精神疾患や神経変性疾患で特に脆弱になるのかについて新たな見通しを提供する。
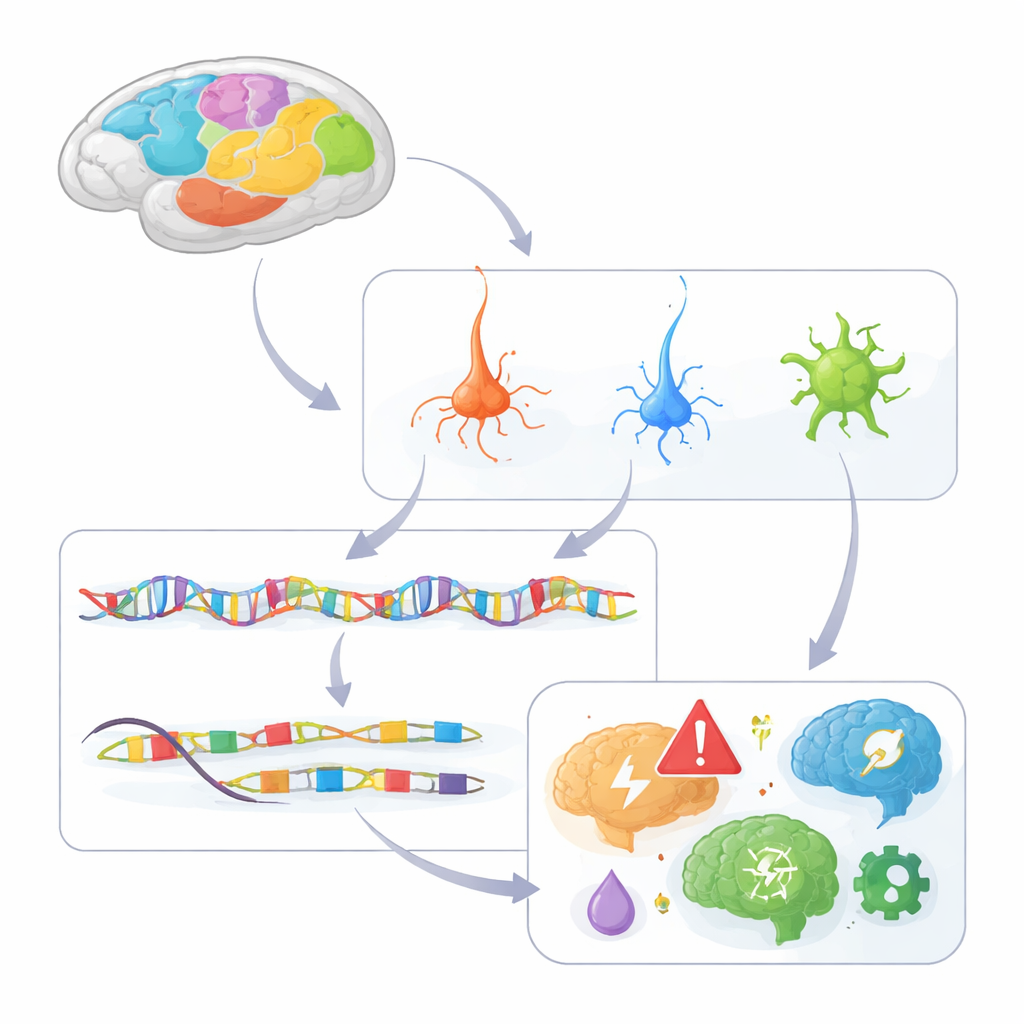
霊長類皮質の細胞レベルアトラスの構築
研究者らは、マカク皮質の142領域から採取した約160万個の個々の核におけるクロマチン開放性、すなわちDNAがどれだけ開いているかを解析した。開いたDNA領域はシス調節要素、つまり近接する遺伝子をオン・オフするスイッチを示す。シングルニュクレウスATAC-seqと呼ばれるドロップレット法を用いて、細胞を230の異なる型に分類し、興奮性グルタミン作動性ニューロン、抑制性GABA作動性ニューロン、アストロサイト、オリゴデンドロサイト、ミクログリアなどの支持細胞を網羅した。60万を超える候補調節要素を同定し、それらの多くを特定の標的遺伝子に結びつけ、皮質の調節配線図の第一稿を構築した。
層別・領域別の遺伝子制御パターン
このDNAスイッチの地図を高解像度の遺伝子発現の空間地図と組み合わせることで、6つの皮質層や複数の葉におけるどこで異なる調節要素が活性化しているかを可視化できた。多くのスイッチは層や領域に強い嗜好を示した。例えば、上層ニューロンを標識する遺伝子に結びつく要素は主に第2層と第3層で活性化され、一方で他の要素はより深い層に限定されていた。一次視覚野(V1)でのみ高く活性化するスイッチもあり、なぜ一部のニューロン型や遺伝子プログラムがこの領域に特有なのかを説明する手がかりとなる。さらに、進化的に古い鼻腔皮質(piriform cortex)と新皮質(neocortex)の対照も明らかになり、グリア細胞と深層ニューロンで異なるスイッチ群が活性化していることから、これらの構造を形作る異なる調節プログラムが示唆された。
主要ニューロン型における霊長類の革新
マカクのデータをヒトやマウスの類似マップと比較すると、霊長類にのみ存在するニューロンの亜クラスが見つかった。特に第4層の一部のグルタミン作動性ニューロンや、LAMP5/LHX6と呼ばれる特殊な抑制性細胞群である。これらの細胞はヒトとマカクで開いている多くの調節要素を持ち、マウスでは開いていないものも多かった。いくつかの要素は転移因子(可動性のあるDNA配列)に伴って出現したと見られ、新たな遺伝子スイッチを生み出した可能性がある。霊長類固有のスイッチはシナプス機能、神経発生、ニューロン間コミュニケーションに関与する遺伝子を制御しており、比較的最近の調節変化が霊長類特有の皮質回路の多様化、特に複雑な知覚や認知に関連する層に寄与したことを示唆している。
支持細胞と可塑性の裏側の配線
この地図は非ニューロン細胞にも光を当てる。オリゴデンドロサイト前駆細胞と成熟オリゴデンドロサイトは皮質の階層に沿って逆の分布を示した:高次領域では前駆細胞が多く、髄鞘化した成熟細胞は少なく、そこでは配線を調整する柔軟性が高いことを示唆する。これらの調節要素はこの勾配を追跡し、シナプスや視覚系遺伝子に結びついた霊長類偏向のスイッチに富んでいた。アストロサイトは上層に集中する層間(interlaminar)細胞と、深い層に分布する小胞体(protoplasmic)細胞に分かれ、それぞれ異なるスイッチと転写因子によって制御されていた。これらのパターンは、ニューロンだけでなくそれらを養い、絶縁し、再編成する細胞群も領域特異的な調節プログラムによって調整され、学習能力や損傷への脆弱性に影響を与えうることを示唆する。
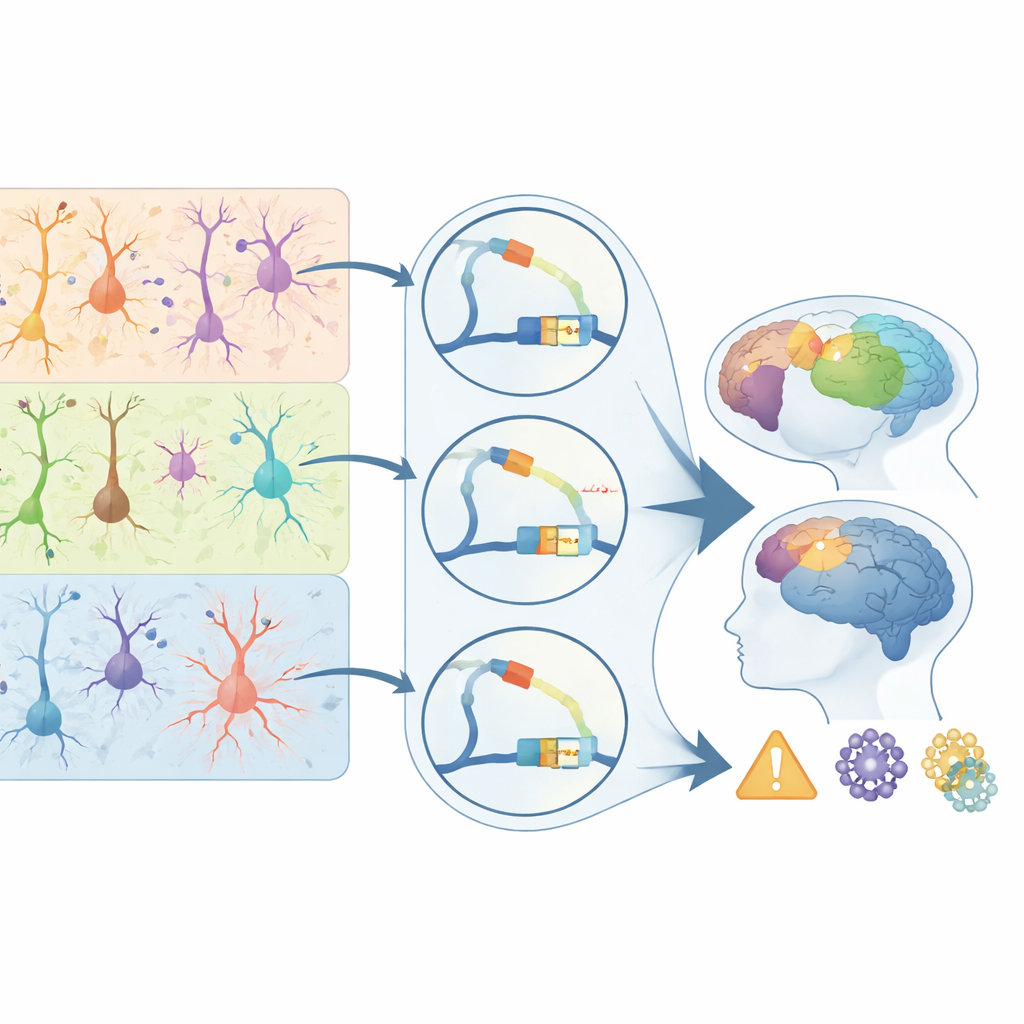
DNAスイッチと脳疾患リスクの結びつけ
彼らの霊長類アトラスをヒトの健康に結びつけるため、著者らはそれを28の脳関連疾患や形質の遺伝学研究と重ね合わせた。疾患に関連する変異は特定の細胞型で活性な調節要素に不均衡に入り込んでいることが分かった。統合失調症や双極性障害のリスク変異は上層の興奮性ニューロンで使われるスイッチに集まり、てんかんのシグナルは特定の抑制性細胞に濃縮し、アルツハイマー病のリスク変異はミクログリアの調節要素に著しく集中していた。これらの疾患関連スイッチの多くは霊長類で偏りを示し、統合失調症では特に第4層ニューロン、アルツハイマー病ではミクログリアに見られ、シナプス、免疫応答、タンパク質除去に影響する既知の遺伝子を標的にしていた。一般読者への要点は、疾患リスクは必ずしもタンパク質を直接壊すことで作用するのではなく、特定の細胞で遺伝子がいつどこでオンになるかを微妙に書き換えることで作用することが多い、ということだ。本研究は、霊長類皮質におけるそのような制御点の画期的な地図を提供し、なぜ一部の細胞型や領域が疾患のホットスポットになるのかを明らかにし、将来の治療がタンパク質部分を修正するのではなく脳の調節コードを正すことを目指すための道標を示している。
引用: Meng, J., Chen, C., Zhu, Z. et al. Single-cell spatial map of cis-regulatory elements for disease-related genes in the macaque cortex. Nat Commun 17, 4041 (2026). https://doi.org/10.1038/s41467-026-70497-x
キーワード: 単一細胞エピゲノミクス, 霊長類皮質, 遺伝子制御, 脳疾患, シス調節要素